Karbonata acido
kemia kombinaĵo
| Karbonata acido | ||
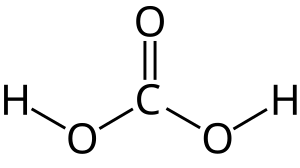 | ||
| Plata kemia strukturo de la Karbonata acido | ||
 | ||
| Tridimensia kemia strukturo de la Karbonata acido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 463-79-6 | |
| ChemSpider kodo | 747 | |
| PubChem-kodo | 767 | |
| Fizikaj proprecoj | ||
| Aspekto | senkolora gaso pli densa ol aero | |
| Molmaso | 62,024 g·mol−1 | |
| Denseco | 1,668g cm−3 | |
| Fandpunkto | −210 °C | |
| Bolpunkto | −78 °C | |
| Acideco (pKa) | 3,6 | |
| Solvebleco | Akvo:Tute solvebla | |
| Sekurecaj Indikoj | ||
| Riskoj | R36 R37 | |
| Sekureco | S25 S26 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H319 | |
| GHS Deklaroj pri antaŭgardoj | P264, P280, P305+351+338, P337+313[1] | |
(25 °C kaj 100 kPa) | ||
Karbonata acido aŭ karbonoksida acido estas malforta acido H2CO3, troviĝanta en la naturaj akvoj. Kelkaj fontoakvoj enhavas multajn karbonatajn acidojn, kiuj larĝigas la haŭtajn kapilarojn tiel helpante la sangocirkuladon kaj la koran laboron.
Ties saloj nomiĝas karbonatoj.
Sintezoj
redaktiSintezo 1
redakti- Preparado per interado de akvo kaj karbona duoksido:
Sintezo 2
redakti- Preparado per traktado de sulfata acido kaj natria karbonato:
Sintezo 3
redakti- Preparado per agado de acetila klorido kaj kalia karbonato:
Sintezo 4
redakti- Preparado hidrolizo de etila karbonato:
Sintezo 5
redakti- Preparado per traktado de kalcia karbonato kaj klorida acido:
Sintezo 6
redakti- Preparado per hidratigo de ureo sekvata per malkomponado de la amonia karbonato:
Sintezo 7
redakti- Preparado per malkomponado de oksalata acido:
Reakcioj
redaktiReakcio 1
redakti- Konvertado al kalia karbonato:
Reakcio 2
redakti- Konvertado al metila karbonato:
Reakcio 3
redakti- Konvertado al ureo:
Reakcio 4
redakti- Konvertado al HCl:
Reakcio 5
redakti- Konvertado al tiokarbonata acido:
Reakcio 6
redakti- Konvertado al peroksokarbonata acido:
Reakcio 7
redakti- Konvertado al ortokarbonata acido:

