INFOGRAFÍA
INFOGRAFÍA
Cargado por
NailetiCopyright:
Formatos disponibles
INFOGRAFÍA
INFOGRAFÍA
Cargado por
NailetiDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Copyright:
Formatos disponibles
INFOGRAFÍA
INFOGRAFÍA
Cargado por
NailetiCopyright:
Formatos disponibles
El carbono es un elemento
químico de número
atómico 6 y símbolo C. Es
sólido a temperatura
ambiente. Dependiendo de
las condiciones de
formación, puede
encontrarse en la
naturaleza en distintas
formas alotrópicas,
carbono amorfo y cristalino
en forma de grafito o
diamante. Es el pilar básico
de la química orgánica; se
conocen cerca de 10
millones de compuestos de
carbono, y forma parte de
todos los seres vivos
conocidos.
nanotubos
grafito
fullerenos
diamante
• El grafito se combina con arcilla para fabricar las minas de los lápices. Además se utiliza como
aditivo en lubricantes. Las pinturas anti-radar utilizadas en el camuflaje de vehículos y aviones
militares están basadas igualmente en el grafito, intercalando otros compuestos químicos entre sus
capas.
• El diamante Es transparente y muy duro. En su formación, cada átomo de carbono está unido de
forma compacta a otros cuatro átomos. Se originan con temperaturas y presiones altas en el
interior de la tierra. Se emplea para la construcción de joyas y como material de corte
aprovechando su dureza.
• Las propiedades químicas y estructurales de los fullerenos, en la forma de nanotubos, prometen
usos futuros en el incipiente campo de la nanotecnología.
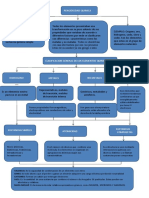
Acíclicos: Cíclicos: Aromáticos:
son compuestos de son compuestos de cadena son una amplísima y muy
cadena abierta. Cada cerrada. Si el ciclo sólo lo importante serie de
átomo de carbono de forman átomos de compuestos derivados del
estas cadenas se carbono, la serie se llama benceno.
caracteriza por el número carbocíclica, y si éstos se
de átomos de carbono a combinan con otro tipo de
que va unido, átomos (oxígeno,
denominándose primario, nitrógeno, azufre), se
secundario o terciario llama heterocíclica.
según esté unido a 1, 2 o 3
átomos de carbono.
Grupos Funcionales
Fórmula Clase de
Grupo funcional Ejemplo Descripción
estructura compuestos
Compuesto polar porque el oxígeno
Hidroxilo 𝑹 − 𝑶𝑯 Alcoholes Etanol electronegativo capta electrones de átomo
covalentes
Amino 𝑹 − 𝑵𝑯2 Aminas Aminoácido Iónico, el grupo amino actúa como base.
𝐎
Ácidos carboxílicos Iónico, el hidrógeno puede disociarse como
Carboxilo || (orgánicos)
Aminoácido
hidrogenión
𝑹 − 𝑪 − 𝑶𝑯
𝐎 Relacionado con el grupo carboxilo, pero
Estér Esteres Metilacetato tiene un grupo en lugar del hidrógeno del
||
hidroxilo; polar
𝑹−𝑪−𝑶−𝑹
𝐎 Carbono de carbonilo enlazado con al
|| Aldehídos Formaldehído
menos un átomo de hidrógeno; polar
𝑹−𝑪−𝑯
Carbonilo
𝐎 Grupo carbonilo enlazado con otros dos
|| Cetonas Acetona
átomos de carbono; polar
𝑹−𝑪−𝑹
Componente de
muchos
Metilo 𝑹 − 𝑪𝑯3 Metano No polar
compuestos
orgánicos.
𝐎
|| Forma disociada del ácido fosfórico, el ion
Fosfato 𝑹 − 𝐎 − 𝑷 − 𝑶𝑯 Fosfatos orgánicos Ester de fosfato fosfato se enlaza en forma covalente, por
| medio de uno de sus átomos de óxigeno,
con uno de los átomos de carbono; iónico.
𝐎𝐇
Ayuda a estabilizar la estructura interna
Sulfidrilo 𝑹 − 𝑺𝑯 Tioles Cisteína
de las proteínas
Por: ITZARLEIS HERNÁNDEZ
También podría gustarte
- SolucionesFormulacion 2Documento2 páginasSolucionesFormulacion 2javitiuno71% (7)
- Captura de Pantalla 2022-05-09 A La(s) 10.49.05 A.M.Documento23 páginasCaptura de Pantalla 2022-05-09 A La(s) 10.49.05 A.M.AbrahamAún no hay calificaciones
- Mapa Conceptual de Nutricion en AnimalesDocumento1 páginaMapa Conceptual de Nutricion en AnimalesIsabella Casadiegos Flórez83% (6)
- Trabajo Introducción A La Química Orgánica.Documento9 páginasTrabajo Introducción A La Química Orgánica.Nicole Herrera67% (3)
- Triptico EditableDocumento2 páginasTriptico EditableRosario de la CruzAún no hay calificaciones
- Filtros de Aire Standard Caida de PresionDocumento2 páginasFiltros de Aire Standard Caida de PresionEdgard Perez-Palma0% (1)
- Ramas de La Quimica 150408235935 Conversion Gate01Documento13 páginasRamas de La Quimica 150408235935 Conversion Gate01Erick L. Vega100% (1)
- Infografía Sobre El CarbonoDocumento1 páginaInfografía Sobre El CarbonoAnxa100% (2)
- Mapa Mental 5 ReinosDocumento4 páginasMapa Mental 5 ReinosJesus ChavezAún no hay calificaciones
- Informe de Los ReinosDocumento25 páginasInforme de Los ReinosMarvin Alexander Andrade Andrade100% (3)
- Triptico QuimicaDocumento2 páginasTriptico QuimicaMauricio Benavides100% (3)
- Mapa Mental de Relación Entre Fotosintesis y RespiracionDocumento1 páginaMapa Mental de Relación Entre Fotosintesis y Respiracionandrea romero100% (3)
- Mapa ConceptualDocumento1 páginaMapa ConceptualLorena buitragoAún no hay calificaciones
- Historia de La Clasificación TaxonómicaDocumento3 páginasHistoria de La Clasificación Taxonómicajh0% (1)
- Procesos Energeticos de Los Seres VivosDocumento17 páginasProcesos Energeticos de Los Seres Vivosysmaryrejon100% (1)
- Química Orgánica Infografía - Gianni Lucena 5to Año ADocumento5 páginasQuímica Orgánica Infografía - Gianni Lucena 5to Año AElieth Flores0% (1)
- Guía de Hidrocarburos Lineales Uesm 2023Documento11 páginasGuía de Hidrocarburos Lineales Uesm 2023Kirito 5.3Aún no hay calificaciones
- Macas Gomez Luis Portafolio Organica 2bDocumento117 páginasMacas Gomez Luis Portafolio Organica 2bGeimyAún no hay calificaciones
- Grupo 2 Tipos de CarbonoDocumento5 páginasGrupo 2 Tipos de CarbonoGoku 123Aún no hay calificaciones
- Tarea 3 - Hidrocarburos Aromaticos-Stella XiomaraDocumento23 páginasTarea 3 - Hidrocarburos Aromaticos-Stella XiomaraDiana RiveraAún no hay calificaciones
- Infografia 3Documento1 páginaInfografia 3carolinaAún no hay calificaciones
- Formas Antropológicas Del CarbonoDocumento1 páginaFormas Antropológicas Del CarbonoCarem SCAún no hay calificaciones
- Act Cyt - Sesion 02 3roDocumento2 páginasAct Cyt - Sesion 02 3rosreyesinstitucionedupeAún no hay calificaciones
- Cuarto de Secundaria Quimica OrganicaDocumento4 páginasCuarto de Secundaria Quimica OrganicakevinAún no hay calificaciones
- 2 HidrocarburosDocumento4 páginas2 HidrocarburosLynn María Del Pilar Cáceres Cabezas De ZambranoAún no hay calificaciones
- Trabajo Colaborativo Quimica - Grupo - 181 FinalDocumento59 páginasTrabajo Colaborativo Quimica - Grupo - 181 FinalWilliam Fernando Esquiivel Diaz100% (1)
- Anexo 4 Carmen Valeria CasierraDocumento12 páginasAnexo 4 Carmen Valeria CasierraChely VargasAún no hay calificaciones
- Qui U2 A2 ErdcDocumento5 páginasQui U2 A2 ErdcErika DominguezAún no hay calificaciones
- Propiedades Del Carbono: QuimicaDocumento3 páginasPropiedades Del Carbono: QuimicaAngel RamonAún no hay calificaciones
- Química Orgánica 2021-1Documento74 páginasQuímica Orgánica 2021-1Ely RamírezAún no hay calificaciones
- El Carbono Orianna Perez 5to DDocumento3 páginasEl Carbono Orianna Perez 5to DOriana PerezAún no hay calificaciones
- S15 CarbonoDocumento51 páginasS15 CarbonocarlosAún no hay calificaciones
- 1er Parcial Quimica-2Documento22 páginas1er Parcial Quimica-2Miguel AlvercaAún no hay calificaciones
- Quimica OrgánicaDocumento30 páginasQuimica OrgánicaCINTHIA YAMILETH VELÁSQUEZ PUERTO VELÁSQUEZ PUERTOAún no hay calificaciones
- Conclusion 6 MergedDocumento7 páginasConclusion 6 Mergedgsz9e274b5Aún no hay calificaciones
- Anexo 2 - Tarea 2 - Estructura y Función de Las Biomoléculas PDFDocumento25 páginasAnexo 2 - Tarea 2 - Estructura y Función de Las Biomoléculas PDFleidy yulieth garcia silvaAún no hay calificaciones
- Módulo 1 - Generales Química OrgánicaDocumento32 páginasMódulo 1 - Generales Química OrgánicaAnaika IsabelAún no hay calificaciones
- Folleto de Química VI Unidad Evelyn y Verónica 1 PDFDocumento53 páginasFolleto de Química VI Unidad Evelyn y Verónica 1 PDFMauricio GomezAún no hay calificaciones
- CarbonoDocumento2 páginasCarbonoAna Maria Ruiz MiñanAún no hay calificaciones
- 1.anexo 2 - Tarea 3 - Ludwing MantillaDocumento14 páginas1.anexo 2 - Tarea 3 - Ludwing MantillaEliana SerranoAún no hay calificaciones
- Quimica OrgánicaDocumento30 páginasQuimica OrgánicaCINTHIA YAMILETH VELÁSQUEZ PUERTO VELÁSQUEZ PUERTOAún no hay calificaciones
- HidrocarburosDocumento9 páginasHidrocarburosMIGUEL ANGEL LUDEÑA TORREAún no hay calificaciones
- s13 Deba 3 4 Recurso Cts TextoDocumento4 páginass13 Deba 3 4 Recurso Cts TextoMartín Leonardo Lacuta VaraAún no hay calificaciones
- Leccion Ii. Caracteristicas Clasificacion y Atomo Del Carbono Parte IiDocumento54 páginasLeccion Ii. Caracteristicas Clasificacion y Atomo Del Carbono Parte IiOxmar UmbaciaAún no hay calificaciones
- Anexo 2 - Tarea 3-Ramontavera-1017146784 TerminadoDocumento24 páginasAnexo 2 - Tarea 3-Ramontavera-1017146784 TerminadoRamón TaveraAún no hay calificaciones
- 14 Deba 3 Recurso Texto Cts PDFDocumento5 páginas14 Deba 3 Recurso Texto Cts PDFArminda ApazaAún no hay calificaciones
- Modulo I - Quimica Organica - CienciasDocumento68 páginasModulo I - Quimica Organica - CienciaslparedesAún no hay calificaciones
- Trabajo Esquema de David Mancilla, Hanner Monsalve y Joan GaravitoDocumento7 páginasTrabajo Esquema de David Mancilla, Hanner Monsalve y Joan GaravitoDavid Santiago Mancilla galloAún no hay calificaciones
- B-3º Act 2 Cyt Und 6Documento4 páginasB-3º Act 2 Cyt Und 6Carlos TorresAún no hay calificaciones
- Guia N9 Quimica Organica Segundo Ciclo PDFDocumento17 páginasGuia N9 Quimica Organica Segundo Ciclo PDFjesus ramirez romeroAún no hay calificaciones
- Planificacion de QuimicaDocumento4 páginasPlanificacion de QuimicaLuis Alejandro RendónAún no hay calificaciones
- QuimicaDocumento6 páginasQuimicaAriana Belen Escriba PachecoAún no hay calificaciones
- Troncal Propuesto Semana 8 (Sesiones 22 y 23) 2Documento29 páginasTroncal Propuesto Semana 8 (Sesiones 22 y 23) 2constanzazapatal2003Aún no hay calificaciones
- Presentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde Tur - 20240924 - 180000 - 0000Documento13 páginasPresentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde Tur - 20240924 - 180000 - 0000erangel.sierra7339Aún no hay calificaciones
- Vicente Mora Rey Bryan Mapas MentalesDocumento7 páginasVicente Mora Rey Bryan Mapas MentalesRey Bryan VicenteAún no hay calificaciones
- Usil S 1 Clase 1 Quima OrganicaDocumento35 páginasUsil S 1 Clase 1 Quima OrganicaMarcos MendozaAún no hay calificaciones
- Capítulo 01 CarbonoDocumento5 páginasCapítulo 01 CarbonoTeo DonairesAún no hay calificaciones
- QUIMICA 3 MEDIO SOLUCIONARIO SEMANA 6 y 7Documento4 páginasQUIMICA 3 MEDIO SOLUCIONARIO SEMANA 6 y 7Jota CidAún no hay calificaciones
- Qui U2 A3 GucvDocumento4 páginasQui U2 A3 GucvGuillermina Coba VelaAún no hay calificaciones
- Propiedades Del Carbono, EjemDocumento7 páginasPropiedades Del Carbono, EjemYUUJIN GOMEZ PEREZAún no hay calificaciones
- El AtomoDocumento2 páginasEl AtomoJavier J. Solis Capcha100% (1)
- El CarbonoDocumento2 páginasEl CarbonoMaría AcostaAún no hay calificaciones
- Presentación en Clase Identificación de Grupos FuncionalesDocumento25 páginasPresentación en Clase Identificación de Grupos FuncionalescarolinacusanguaAún no hay calificaciones
- ISLPII202224Documento19 páginasISLPII202224NailetiAún no hay calificaciones
- VATÍMETRODocumento6 páginasVATÍMETRONailetiAún no hay calificaciones
- Defensa IiiDocumento12 páginasDefensa IiiNaileti100% (1)
- Sistemas OperativosDocumento13 páginasSistemas OperativosNailetiAún no hay calificaciones
- Ejercicios Prácticos Usando Los Auxiliares Do Y DoesDocumento5 páginasEjercicios Prácticos Usando Los Auxiliares Do Y DoesNaileti100% (2)
- Teoría de Errores.Documento4 páginasTeoría de Errores.NailetiAún no hay calificaciones
- Garantía de La Igualdad Entre Las PartesDocumento3 páginasGarantía de La Igualdad Entre Las PartesNailetiAún no hay calificaciones
- Unidades Eléctricas de MedidaDocumento4 páginasUnidades Eléctricas de MedidaNailetiAún no hay calificaciones
- ISLPII20222128434285Documento14 páginasISLPII20222128434285NailetiAún no hay calificaciones
- Historia de La FísicaDocumento7 páginasHistoria de La FísicaNailetiAún no hay calificaciones
- Cuándo Se Fundó CalabozoDocumento1 páginaCuándo Se Fundó CalabozoNailetiAún no hay calificaciones
- La Épica GriegaDocumento7 páginasLa Épica GriegaNailetiAún no hay calificaciones
- Glosario FisicaDocumento12 páginasGlosario FisicaNaileti100% (3)
- Codificación Convencional en El Sistema InteramericanoDocumento13 páginasCodificación Convencional en El Sistema InteramericanoNailetiAún no hay calificaciones
- Daños Ocasionados Por Plagas y Parasitos en Los Cultivos VegetalesDocumento20 páginasDaños Ocasionados Por Plagas y Parasitos en Los Cultivos VegetalesNailetiAún no hay calificaciones
- Clases SocialesDocumento4 páginasClases SocialesNailetiAún no hay calificaciones
- Limpieza Del TerrenoDocumento3 páginasLimpieza Del TerrenoNailetiAún no hay calificaciones
- Orientaciones para Elaborar El Informe Final Del S C DefinitivoDocumento22 páginasOrientaciones para Elaborar El Informe Final Del S C DefinitivoNailetiAún no hay calificaciones
- Triptico LA PIELDocumento2 páginasTriptico LA PIELNailetiAún no hay calificaciones
- Triptico Identidad NacionalDocumento2 páginasTriptico Identidad NacionalNailetiAún no hay calificaciones
- Clasificación de Los MaterialesDocumento7 páginasClasificación de Los MaterialesNailetiAún no hay calificaciones
- NEOPLASIASDocumento14 páginasNEOPLASIASNailetiAún no hay calificaciones
- Derecho Internacional PrivadoDocumento15 páginasDerecho Internacional PrivadoNailetiAún no hay calificaciones
- Esquema para Elaborar El Informe Final Del S CDocumento8 páginasEsquema para Elaborar El Informe Final Del S CNailetiAún no hay calificaciones
- El Derecho Administrativo y Su Relación Con Las Otras Disciplinas JurídicasDocumento3 páginasEl Derecho Administrativo y Su Relación Con Las Otras Disciplinas JurídicasNailetiAún no hay calificaciones
- Obligaciones-El ContratoDocumento34 páginasObligaciones-El ContratoNailetiAún no hay calificaciones
- Seguridad CiudadanaDocumento4 páginasSeguridad CiudadanaNailetiAún no hay calificaciones
- Ingeniería GenéticaDocumento10 páginasIngeniería GenéticaNailetiAún no hay calificaciones
- Clasificacion de Las Vias en VenezuelaDocumento5 páginasClasificacion de Las Vias en VenezuelaNailetiAún no hay calificaciones
- Fuentes de Informacion de La Policia SonDocumento12 páginasFuentes de Informacion de La Policia SonNailetiAún no hay calificaciones
- Cuestionario 6 y 7Documento4 páginasCuestionario 6 y 7janssen100% (1)
- Aportes de Cientificos A La Tabla PeriodicaDocumento1 páginaAportes de Cientificos A La Tabla Periodicaluc.cosmoonAún no hay calificaciones
- Cálculo Del NSRDocumento35 páginasCálculo Del NSRcarlos moranteAún no hay calificaciones
- Ejerci Equilibrio de Solubilidad y de Iones ComplejosDocumento2 páginasEjerci Equilibrio de Solubilidad y de Iones ComplejosHomerAún no hay calificaciones
- QuimicaDocumento20 páginasQuimicaJesus Vallenas Yrigoyen0% (1)
- Formula Solucion Nutritiva para FresaDocumento2 páginasFormula Solucion Nutritiva para FresaBrayan Encina TafurAún no hay calificaciones
- Química T - HidróxidosDocumento3 páginasQuímica T - HidróxidosAllisson CordovaAún no hay calificaciones
- MSDS PremezcladosDocumento1 páginaMSDS PremezcladosCarlos PingoAún no hay calificaciones
- Req - Carpinteria MaderaDocumento9 páginasReq - Carpinteria MaderajoseAún no hay calificaciones
- Obj2. 61-86Documento12 páginasObj2. 61-86jorgeAún no hay calificaciones
- Ejemplo 1Documento4 páginasEjemplo 1xchinodanyAún no hay calificaciones
- Práctica No 7Documento3 páginasPráctica No 7VanessaAún no hay calificaciones
- Problemas Soluciones Analisis Instrumental 1Documento3 páginasProblemas Soluciones Analisis Instrumental 1Pavel FuentesAún no hay calificaciones
- CONVERTIDOR Peso-Metro y Metro-Kilo.Documento92 páginasCONVERTIDOR Peso-Metro y Metro-Kilo.Ángel PvelardeAún no hay calificaciones
- Marco Teórico - Docx111Documento3 páginasMarco Teórico - Docx111Angie Fuerte Hernandez100% (1)
- Ejercicios - EstequiometríaDocumento3 páginasEjercicios - Estequiometríaxiomara angelAún no hay calificaciones
- Complejos de WernerDocumento6 páginasComplejos de WernerEdwin Tapia0% (1)
- Nomenclatura y Mecanismos de Reacciones Quimicas InorganicasDocumento4 páginasNomenclatura y Mecanismos de Reacciones Quimicas InorganicasEdgar FernandoAún no hay calificaciones
- Taller Oxidos y SalesDocumento8 páginasTaller Oxidos y SalesMaira Alejandra TorresAún no hay calificaciones
- A Praha Mian Catalogo 2017Documento32 páginasA Praha Mian Catalogo 2017bicoboAún no hay calificaciones
- Producto Desengrasante Orden Materia Prima %: Sosa Caustica Butilglicol Nonilfenol Color Verde PiramidinaDocumento8 páginasProducto Desengrasante Orden Materia Prima %: Sosa Caustica Butilglicol Nonilfenol Color Verde Piramidinahugo alexander villalobos osorioAún no hay calificaciones
- Actividad de Puntos Evaluables - Escenario 2 Fundamentos QuimicaDocumento7 páginasActividad de Puntos Evaluables - Escenario 2 Fundamentos QuimicaYuri CuellarAún no hay calificaciones
- Guia Introduccion A Qca I 2017 GeologiaDocumento44 páginasGuia Introduccion A Qca I 2017 GeologiayesicaberthAún no hay calificaciones
- El PotasioDocumento51 páginasEl PotasioAbdel Huaman MolinaAún no hay calificaciones
- PDF Metales Segun Su Punto de Fusion y Otros FundamentosDocumento7 páginasPDF Metales Segun Su Punto de Fusion y Otros Fundamentosdnl gattoAún no hay calificaciones
- Química de Fijación IIDocumento33 páginasQuímica de Fijación IIAdolfo Antonio Ríos AlcortaAún no hay calificaciones
- Clases de MateriaDocumento6 páginasClases de MateriaJuan Gabriel ArandoAún no hay calificaciones