EJERCICIOS REPASO Z y A
EJERCICIOS REPASO Z y A
Cargado por
OPVUNION POPULARCopyright:
Formatos disponibles
EJERCICIOS REPASO Z y A
EJERCICIOS REPASO Z y A
Cargado por
OPVUNION POPULARDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Copyright:
Formatos disponibles
EJERCICIOS REPASO Z y A
EJERCICIOS REPASO Z y A
Cargado por
OPVUNION POPULARCopyright:
Formatos disponibles
EJERCICIOS REPASO . EL ÁTOMO Y SISTEMA PERIÓDICO.
2014-15
1. Indica el número de protones, neutrones y electrones de cada especie y cuáles de ellas son isótopos de
12
un mismo elemento: 6
X ;128Y ;146 Z ;199 U ;148V .
2. Completa la tabla siguiente y explica el tipo de iones estables que pueden formar.
Elemento Represen- Proto- Electro- Configuración
Símbolo A Z Neutrones
tación nes nes electrónica
Azufre
S 32 16 16 16 12 3s2 3p4
Cloro Cl 35 17 19 17 17 3s² 3p5
Calcio
Ca 40 20 20 20 18 4s²
3. Completa la tabla siguiente y responde a las cuestiones
Especia Símbolo Z A Protones Neutrones electrones
química
1 Sr 38 87 38 49 36
2 N 7 14 7 7 7
3 Bh 107 264 7 9 7
4 S 16 32 20 20 18
a) ¿Cuál es un ión negativo? Nitrogeno ion negativo -2, Azufre ion negativo -2
b) ¿Cuál es un in positivo? Estroncio es un ion positivo +2
c) ´¿Cuáles son isótopos? Bohrio con 6 cadenas de isopos
4. Dados los siguientes iones: O2- ; F- ; Ca2+; K+.
a) Indica el número de protones y de electrones de cada uno. b) Escribe la distribución electrónica.
O2- (8 protones,8 electrones); F- (9 protones,9 electrones); Ca2+(18 protones,20 electrones)
k+(19 protones,18 electrones)
( Números atómicos: O = 8 ; F = 9 ; Ca = 20 ; K = 19)
O=Oxigeno; F=Fluor ; Ca = Calcio ; K= Potasio
5. -Un átomo neutro con 12 protones pierde 2 electrones.
a) ¿En qué se transforma? ¿Sigue siendo el mismo elemento?
b) ¿Mantiene el mismo número másico?
c) Escribe la configuración electrónica, tanto del elemento como del ión formado.
6.- Un átomo neutro con 16 protones gana 2 electrones:
a) ¿En qué se transforma?
b) ¿Sigue siendo el mismo elemento? ¿Mantiene el mismo número atómico?
c) Escribe la configuración electrónica, tanto del elemento como del ión formado.
7. -Completa la siguiente tabla:
Símbolo Nombre Z A p n e
Fe Hierro 26 56 26 29 26
Na Sodio 11 23 11 12 11
S Azufre 16 32 16 16 12
Ión
Ca2+ 20 40 20 20 18
calcio
Al Aluminio 13 26 13 14 13
Cl Cloro 17 35 20 28 20
Cl- Ion- Calcio 17 35 20 28 20
Sn2+ Estaño 50 118 50 54 50
K+ Potasio 19 39 18 20 18
RTA PUNTO 5
El elemento químico es: Magnesio
Al perder dos electrones se transforma en un catión (Mg⁺²)
Sí sigue siendo el mismo elemento , sólo que su carga ya no es neutra
No. protones= 12 → Z=12→ corresponde al Magnesio (Mg)
Un átomo en estado neutro presenta igual número de protones y electrones. Sin embargo,
cuando pierde dos electrones, se convierte en catión ya que tiene más protones que
electrones:Mg ⁺²
Configuración electronica 3s2
RTA PUNTO 6
El elemento químico es: Azufre
Es un atomo con energia negativa (-)
SI, sigue siendo el mismo elemento con el mismo número Básico,
SI , mantiene el mismo numero atomico = 16 Azufre (S)
Configuración electronica:3s2 3p4
También podría gustarte
- Tema 2 Fisica y Quimica Santillana 3ºesoDocumento14 páginasTema 2 Fisica y Quimica Santillana 3ºesosenecamovil50% (4)
- Solucionario Enlace QuímicoDocumento5 páginasSolucionario Enlace QuímicoCristian CastilloAún no hay calificaciones
- Resolucion de Problemas IiDocumento5 páginasResolucion de Problemas Iimatesdemanu50% (2)
- Apuntes Física y Química 3º EsoDocumento8 páginasApuntes Física y Química 3º EsoLazaro Paez Ruiz100% (1)
- Ejercicios RESUELTOS Del Tema 4 (Estructura de La Materia)Documento3 páginasEjercicios RESUELTOS Del Tema 4 (Estructura de La Materia)MARGUSIAún no hay calificaciones
- Disoluciones Resueltos PDFDocumento5 páginasDisoluciones Resueltos PDFadolfo olmosAún no hay calificaciones
- Solucionario-Fy-Q-la Ciencia y La MedidaDocumento16 páginasSolucionario-Fy-Q-la Ciencia y La MedidafimaquiAún no hay calificaciones
- Layos ToledoDocumento1 páginaLayos Toledofran41960aguirre0% (1)
- Hidruros 3º ESO PDFDocumento2 páginasHidruros 3º ESO PDFMaribel FossatiAún no hay calificaciones
- Apuntes de Formulación y Nomenclatura 4º ESODocumento8 páginasApuntes de Formulación y Nomenclatura 4º ESOALBERTO GALLEGOAún no hay calificaciones
- ER Ajustes ReaccionesDocumento2 páginasER Ajustes ReaccionesfaltriqueraAún no hay calificaciones
- Raquel Física y Química 3º ESO Ejercicios ReaccionesDocumento3 páginasRaquel Física y Química 3º ESO Ejercicios ReaccionesJoseA.MartinezJimenezAún no hay calificaciones
- Repaso - Matematicas B. 4 ESO-SantillanaDocumento8 páginasRepaso - Matematicas B. 4 ESO-Santillananati100% (1)
- Ejercicios ATOMOS 3esoDocumento2 páginasEjercicios ATOMOS 3esoAcademy Profes100% (1)
- Control de Números Complejos Resuelto 1Documento2 páginasControl de Números Complejos Resuelto 1housegrj100% (1)
- Ud3 Refuerzo - Fyq 2eso - Parte 2Documento4 páginasUd3 Refuerzo - Fyq 2eso - Parte 2José Cuenca0% (1)
- ValenciasDocumento1 páginaValenciasTiffany LopezAún no hay calificaciones
- Evaluacion Con NomenclaturaDocumento10 páginasEvaluacion Con Nomenclaturamonica rodriguez mAún no hay calificaciones
- Geo.-Historia 3º Eso Tema 10 Liberalismo y NacionalismoDocumento58 páginasGeo.-Historia 3º Eso Tema 10 Liberalismo y NacionalismoJOEL RODRÍGUEZ PAYÁ100% (1)
- Tema 5 Problemas de Sistemas de EcuacionesDocumento4 páginasTema 5 Problemas de Sistemas de EcuacionesJimenauwu DreamgirlAún no hay calificaciones
- Sol - Diver Ii - CT - U02Documento36 páginasSol - Diver Ii - CT - U02javiervelaAún no hay calificaciones
- Tabla Periodica ColorDocumento1 páginaTabla Periodica Colorbelenmolina128Aún no hay calificaciones
- 3º-4º Eso - Formulación de HidrurosDocumento18 páginas3º-4º Eso - Formulación de Hidrurosangela_zamorano_4Aún no hay calificaciones
- Examen - Trigonometria 4 EsoDocumento1 páginaExamen - Trigonometria 4 EsoFranciscodelPinoAún no hay calificaciones
- Resumen Fórmulas CinemáticaDocumento1 páginaResumen Fórmulas Cinemáticamirpreciados50% (2)
- Tabla de Indeterminaciones PDFDocumento2 páginasTabla de Indeterminaciones PDFLuiz K RiiAño100% (1)
- Logaritmos 4 ESODocumento3 páginasLogaritmos 4 ESOPedro Delgado CorbachoAún no hay calificaciones
- Problemas Resueltos 1 MCUDocumento4 páginasProblemas Resueltos 1 MCUJavier AlonsoAún no hay calificaciones
- Examen Números Naturales (1ºESO Matemáticas)Documento2 páginasExamen Números Naturales (1ºESO Matemáticas)Hirune Auñón GarcíaAún no hay calificaciones
- Resumen UD 3 Elementos y Compuestos 3 ESO SantillanaDocumento4 páginasResumen UD 3 Elementos y Compuestos 3 ESO SantillanablueknowAún no hay calificaciones
- 2 - Atomos y Sistema Periodico PDFDocumento6 páginas2 - Atomos y Sistema Periodico PDFJennifer RamirezAún no hay calificaciones
- 3-4 Eso - Formulación ÓxidosDocumento13 páginas3-4 Eso - Formulación Óxidosangela_zamorano_4Aún no hay calificaciones
- Examen Física y Quimica 4 ESODocumento4 páginasExamen Física y Quimica 4 ESOAntonio PrietoAún no hay calificaciones
- Recubrimiento de Una Moneda 6Documento13 páginasRecubrimiento de Una Moneda 6Rodrigo CarranzaAún no hay calificaciones
- Problemas de Fuerza (Resueltos)Documento4 páginasProblemas de Fuerza (Resueltos)TamaraBlanes100% (1)
- Examen Física y Química 3ESO. - Tema 2 Átomo y Configuración ElectrónicaDocumento1 páginaExamen Física y Química 3ESO. - Tema 2 Átomo y Configuración ElectrónicaAlejandro Martin SaavedraAún no hay calificaciones
- Resumen Tema 7 La Corteza TerrestreDocumento1 páginaResumen Tema 7 La Corteza TerrestreBeatriz AlvarezAún no hay calificaciones
- Biologia Geologia Refuerzo Ampliacion Sin Soluciones 3eso PDF 17Documento1 páginaBiologia Geologia Refuerzo Ampliacion Sin Soluciones 3eso PDF 17341389.Aún no hay calificaciones
- Examen t4Documento2 páginasExamen t4uguygug50% (2)
- Comercio TransporteDocumento23 páginasComercio TransportePatata Manzana PeladaAún no hay calificaciones
- QuimicaDocumento18 páginasQuimicaPsc. Linda Cajas Edgar100% (1)
- La Puerta de Los 3 CerrojosDocumento2 páginasLa Puerta de Los 3 Cerrojosmanuel0% (2)
- Divisibilidad 2º EsoDocumento7 páginasDivisibilidad 2º EsoMaría Jesús Caballero SánchezAún no hay calificaciones
- Resumen Nomenclatura Inorganica PDFDocumento2 páginasResumen Nomenclatura Inorganica PDFAnonymous VvPU8jG44Aún no hay calificaciones
- Tema 7 Los Reinos CristianosDocumento21 páginasTema 7 Los Reinos CristianosTatiana ValeroAún no hay calificaciones
- Ejercicios Repaso Tema 2. Los Sistemas MaterialesDocumento28 páginasEjercicios Repaso Tema 2. Los Sistemas Materialesanalazos100% (2)
- Fuerzas Movimeno 3ºESO SantillanaDocumento29 páginasFuerzas Movimeno 3ºESO SantillanaPablo GilAún no hay calificaciones
- Taller Sobre Los Califatos y El Imperio MusulmanDocumento5 páginasTaller Sobre Los Califatos y El Imperio MusulmanMarleny CalderonAún no hay calificaciones
- Taller de Balanceo de Ecuaciones Por Tanteo o Simple Inspeccion Grado Decimo Sede GaviotasDocumento1 páginaTaller de Balanceo de Ecuaciones Por Tanteo o Simple Inspeccion Grado Decimo Sede Gaviotassofia fajardo100% (1)
- 3bgu Bio F2Documento162 páginas3bgu Bio F2NnjjgfgdijenfjjAún no hay calificaciones
- Taller 3 GasesDocumento5 páginasTaller 3 Gasesjose toalaAún no hay calificaciones
- Ejercicios Tema 5 Enlace Químico Física y Química 3º EsoDocumento5 páginasEjercicios Tema 5 Enlace Químico Física y Química 3º EsoGuillermo RoderoAún no hay calificaciones
- Teoría Formulación - Sales Binarias - HidrurosDocumento1 páginaTeoría Formulación - Sales Binarias - HidrurosCutrezsoAún no hay calificaciones
- Problemas de Ecuaciones ResueltosDocumento20 páginasProblemas de Ecuaciones ResueltosFabricio Leonel López AgudoAún no hay calificaciones
- Prueba 12 2016-17 - Tema 5 - ResueltaDocumento2 páginasPrueba 12 2016-17 - Tema 5 - ResueltairenetisAún no hay calificaciones
- Examen FINAL MAT ACAD - 4 ESODocumento1 páginaExamen FINAL MAT ACAD - 4 ESOAna Isabel Villarino VelosAún no hay calificaciones
- Enunciados y Ejercicios Resueltos de Campo Eléctrico - Selectividad UNEDDocumento10 páginasEnunciados y Ejercicios Resueltos de Campo Eléctrico - Selectividad UNEDIvaj El HumanoAún no hay calificaciones
- Actividades Resueltas de Formulación Inorgánica 4º ESODocumento7 páginasActividades Resueltas de Formulación Inorgánica 4º ESOalejandro100% (1)
- Quimica Taller ComplDocumento2 páginasQuimica Taller ComplZamanta Cabrera JiménezAún no hay calificaciones
- Caracterización química, morfológica y estructural de materialesDe EverandCaracterización química, morfológica y estructural de materialesAún no hay calificaciones
- Manual de FuncionamientoDocumento108 páginasManual de FuncionamientoOPVUNION POPULARAún no hay calificaciones
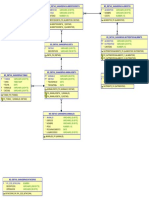
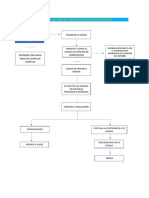
- APOYO ADMINISTRATIVO EN SALUD Flujograma Sobre El Proceso de Afiliación. GA2-230101003-AA2-EV01. Presentado Por Viery Kriss Schonewolf AÑO 2022Documento2 páginasAPOYO ADMINISTRATIVO EN SALUD Flujograma Sobre El Proceso de Afiliación. GA2-230101003-AA2-EV01. Presentado Por Viery Kriss Schonewolf AÑO 2022OPVUNION POPULARAún no hay calificaciones
- Biografia StarbucksDocumento1 páginaBiografia StarbucksOPVUNION POPULARAún no hay calificaciones
- Actividad 3 La Infancia y La Adolescencia Desde Los MicrosistemasDocumento3 páginasActividad 3 La Infancia y La Adolescencia Desde Los MicrosistemasOPVUNION POPULAR100% (2)
- Biografia StarbucksDocumento1 páginaBiografia StarbucksOPVUNION POPULARAún no hay calificaciones
- Actividad Rompe Hielo Crucigrama Sopa de LetrasDocumento1 páginaActividad Rompe Hielo Crucigrama Sopa de LetrasOPVUNION POPULARAún no hay calificaciones
- Excel Intermedio CafamDocumento5 páginasExcel Intermedio CafamOPVUNION POPULARAún no hay calificaciones
- Rocky y Su Tesoro, by Samuel CañasDocumento9 páginasRocky y Su Tesoro, by Samuel CañasOPVUNION POPULARAún no hay calificaciones
- Proyecto OpvDocumento13 páginasProyecto OpvOPVUNION POPULARAún no hay calificaciones
- Cartilla OPV DefDocumento57 páginasCartilla OPV DefOPVUNION POPULARAún no hay calificaciones
- Diseño GraficoDocumento6 páginasDiseño GraficoOPVUNION POPULARAún no hay calificaciones
- Estado de Embriaguez SancionesDocumento2 páginasEstado de Embriaguez Sancionesvictor.villarruel.cadenaAún no hay calificaciones
- Definición de Método DeductivoDocumento5 páginasDefinición de Método DeductivoShirley AbazaAún no hay calificaciones
- DPR 05 Check List Camion AljibeDocumento1 páginaDPR 05 Check List Camion AljibeCarlosChavezPonce0% (1)
- Actividad 3 JDocumento4 páginasActividad 3 JJennifer Vásquez100% (1)
- Somatotipo y SomatocartaDocumento2 páginasSomatotipo y SomatocartaArnoldo Fabra Educación Física Colegio RoraimaAún no hay calificaciones
- CX Dietas GanaderasDocumento1 páginaCX Dietas GanaderasThomas ShelbyAún no hay calificaciones
- Plan Semanal Ricardo MardelliDocumento1 páginaPlan Semanal Ricardo MardelliRicardo MardelliAún no hay calificaciones
- Prueba Ciencias Naturales Segundo BasicoDocumento12 páginasPrueba Ciencias Naturales Segundo BasicomeybuAún no hay calificaciones
- Envases y Embalaje Ventajas y DesventajasDocumento2 páginasEnvases y Embalaje Ventajas y DesventajasJoao JachoAún no hay calificaciones
- Vodka ExposicionDocumento17 páginasVodka ExposicionNohely Interian PenicheAún no hay calificaciones
- Marbete 19Documento5 páginasMarbete 19carrizoignacio45Aún no hay calificaciones
- Compuestos NitrogenadosDocumento20 páginasCompuestos NitrogenadosIvanAguilarGalvanAún no hay calificaciones
- Contaminación Del Agua (Río Llullan)Documento7 páginasContaminación Del Agua (Río Llullan)TheMoryAún no hay calificaciones
- Libro-Agricultura InteligenteDocumento126 páginasLibro-Agricultura InteligenteMeinardo BautistaAún no hay calificaciones
- Omni230 PDFDocumento19 páginasOmni230 PDFClaudio Garretón VénderAún no hay calificaciones
- Iss Manuales Final1Documento1613 páginasIss Manuales Final1Margarita Maria Gaitan VeraAún no hay calificaciones
- Protocolo de Lluvias y SismosDocumento8 páginasProtocolo de Lluvias y SismosLucas Antonio Itzep FelipeAún no hay calificaciones
- Caso Clínico de PediatríaDocumento20 páginasCaso Clínico de PediatríaJessica Pilar Arcentales VerdugoAún no hay calificaciones
- Especif Generales - PoliductoDocumento29 páginasEspecif Generales - PoliductoEduardo Calderon100% (1)
- Ficha Integradora 2do. Ante La Pandemia PDFDocumento11 páginasFicha Integradora 2do. Ante La Pandemia PDFElizabeth MuñozAún no hay calificaciones
- Enciclopedia Ogbe AteDocumento38 páginasEnciclopedia Ogbe Atecesar awo ogunda dio100% (5)
- Jga 504 704 FX EsDocumento2 páginasJga 504 704 FX EsAreli BenítezAún no hay calificaciones
- Bombas de Flujo MixtoDocumento14 páginasBombas de Flujo Mixtotoroloco100% (3)
- El Hurto Famelico en Las Decisiones de LDocumento32 páginasEl Hurto Famelico en Las Decisiones de LAlejandrina TobarAún no hay calificaciones
- Analisis Del Documental HomeDocumento2 páginasAnalisis Del Documental HomeRosalinda RodriguezAún no hay calificaciones
- Asepsia Y Control de Infecciones en La Práctica de Realizar Tatuajes Permanentes Y Perforaciones CorporalesDocumento78 páginasAsepsia Y Control de Infecciones en La Práctica de Realizar Tatuajes Permanentes Y Perforaciones CorporalesAileen Jordán SotomayorAún no hay calificaciones
- Diseño Barda PerimetralDocumento11 páginasDiseño Barda PerimetralLopmej AgusAún no hay calificaciones
- Factor ProteicoDocumento9 páginasFactor ProteicoJuan CamiloAún no hay calificaciones
- Calculos Electricos +3Documento154 páginasCalculos Electricos +3Dave ChecaAún no hay calificaciones
- Pange Lingua 1Documento1 páginaPange Lingua 1luis guerreroAún no hay calificaciones