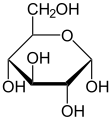
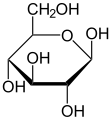
Monosacàrid
Els monosacàrids són els glúcids més simples. La fórmula empírica per tots els monosacàrids és (CH₂O)n.[1][2] Estan formats per tan sols una cadena polihidroxialdehídica o polihidroxicetònica, constituïda de 3 a 7 àtoms de carboni. Com que són els glúcids més simples no es poden hidrolitzar, és a dir, no es poden descompondre en molècules més petites.[3][4] Gràcies al grup aldehid o cetona que tenen, poden reaccionar amb alguns reactius com el reactiu de Fehling.[5]
Es denominen afegint la terminació "-osa", i segons el nombre de carbonis de la cadena es poden anomenar: trioses, tetroses, pentoses, hexoses o heptoses. D'altra banda, si el grup carbonil es troba al primer carboni es denomina grup aldehid i els monosacàrids corresponents són aldoses, com la glucosa; si el carbonil està al segon carboni s'anomena cetona i els monosacàrids corresponents cetoses. Si es combina el nombre de carbonis amb el tipus de carbonil, tenim aldopentoses, cetopentoses, aldohexoses, cetohexoses, etc.
Estructura i nomenclatura
[modifica]Amb poques excepcions (per exemple la desoxiribosa), els monosacàrids tenen aquesta fórmula química: (CH2O)x, on convencionalment x≥3. Els monosacàrids es poden classificar pel nombre x d'àtoms de carboni que contenen: triosa (3), tetrosa (4), pentosa (5) , hexosa (6), heptosa (7), etc.

La glucosa, utilitzada com a font d'energia i per a la síntesi de midó, glucogen i cel·lulosa, és una hexosa. La ribosa i la desoxirribosa (en ARN i ADN, respectivament) són sucres de pentosa. Exemples d'heptoses inclouen cetoses, manoheptulosa i sedoheptulosa. Poques vegades s'observen monosacàrids amb vuit o més carbonis, ja que són força inestables. En solucions aquoses, els monosacàrids existeixen com a anells si tenen més de quatre carbonis.
Monosacàrids de cadena lineal
[modifica]Els monosacàrids simples tenen un esquelet de carboni lineal i no ramificat amb un grup funcional carbonil (C=O) i un grup hidroxil (OH) en els carboni restants. Per tant, l'estructura molecular d'un monosacàrid simple es pot escriure com H(CHOH)n (C=O)(CHOH)mH, on n + 1 + m = x; de manera que la seva fórmula elemental és CxH2xOx. Per convenció, els àtoms de carboni es numeren de l'1 al x al llarg de l'esquelet, començant per l'extrem més proper al grup C=O. Si el carbonil és a la posició 1 (és a dir, n o m és zero), la molècula comença amb un grup formil H(C=O)− i tècnicament és un aldehid. En aquest cas s'anomena Aldosa. En cas contrari, té un grup cetona −(C=O)−; llavors és formalment una cetona, i es denomina cetosa. Les cetoses d'interès biològic solen tenir el carbonil a la posició 2. Una nomenclatura més general per a monosacàrids de cadena oberta combina un prefix grec per indicar el nombre de carbonis (tri-, tetr-, pent-, hex-, etc.) amb els sufixos "-osa" per a aldoses i "-ulosa" per a cetoses.[6] En aquest darrer cas, si el carbonil no és a la posició 2, la seva posició s'indica mitjançant un infill numèric. Aleshores, per exemple, H(C=O)(CHOH)4H és pentosa, H(CHOH)(C=O)(CHOH)3H és pentulosa i H(CHOH)2(C=O)(CHOH)2H és pent-3-ulosa.
Estereoisòmers de cadena oberta
[modifica]Dos monosacàrids amb gràfics moleculars equivalents (mateixa longitud de cadena i mateixa posició de carbonil) encara poden ser estereoisòmers diferents, les molècules dels quals difereixen en l'orientació espacial. Això succeeix només si la molècula conté un estereocentre, específicament un àtom de carboni que és quiral (connectat a quatre subestructures moleculars diferents). Aquests quatre enllaços poden tenir qualsevol de les dues configuracions a l'espai que es distingeixen per la seva lateralitat. En un monosacàrid de cadena oberta simple, tots els carbonis són quirals excepte el primer i l'últim àtom de la cadena i (a les cetoses) el carboni amb el grup ceto.
Per exemple, la tricetosa H(CHOH)(C=O)(CHOH)H (glicerona, dihidroxiacetona) no té un centre estereogènic i, per tant, existeix com un sol estereoisòmer. L'altra triosa, l'aldosa H(C=O)(CHOH)2H (gliceraldehid), té un carboni quiral, el central, el número 2, que està unit als grups −H, −OH, −C(OH)H 2 i −(C=O)H. Per tant, hi ha dos estereoisòmers les molècules dels quals són imatges especulars entre si. Els monosacàrids amb quatre o més carbonis poden contenir múltiples carbonis quirals, per la qual cosa solen tenir més de dos estereoisòmers. El nombre d'estereoisòmers diferents amb el mateix diagrama està limitat per 2c, donde c és el nombre total de carbonis quirals.
La projecció de Fischer és una forma sistemàtica de dibuixar la fórmula esqueletal d'un monosacàrid acíclic perquè la lateralitat de cada carboni quiral estigui ben especificada. Cada estereoisòmer d'un monosacàrid de cadena oberta simple es pot identificar per les posicions (dreta o esquerra) al diagrama de Fischer dels hidroxils quirals (els hidroxils units als carbonis quirals). La majoria dels estereoisòmers són en si mateixos quirals (diferents de les imatges especulars). A la projecció de Fischer, dos isòmers d'imatge especular es diferencien per tenir les posicions de tots els hidroxils quirals invertides de dreta a esquerra. Els isòmers d'imatge especular són químicament idèntics en entorns no quirals, però generalment tenen propietats bioquímiques i ocurrències naturals molt diferents.
Si bé la majoria dels estereoisòmers es poden organitzar en parells de formes d'imatge especular, hi ha alguns estereoisòmers no quirals que són idèntics a les imatges especulars, tot i tenir centres quirals. Això passa sempre que el gràfic molecular sigui simètric, com en les 3-cetopentoses H(CHOH)2(CO)(CHOH)2H, i les dues meitats són imatges especulars entre si. En aquest cas, la duplicació equival a una rotació de mitja volta. Per aquesta raó, només hi ha tres estereoisòmers de 3-cetopentosa diferents, encara que la molècula té dos carbonis quirals.
Els estereoisòmers diferents que no són imatges especulars entre si solen tenir diferents propietats químiques, fins i tot en entorns no quirals. Per tant, cada parell de miralls i cada estereoisòmer no quiral poden rebre un nom de monosacàrid específic. Per exemple, hi ha 16 estereoisòmers d'aldohexosa diferents, però el nom "glucosa" significa un parell específic d'aldohexoses d'imatge especular. A la projecció de Fischer, un dels dos isòmers de glucosa té l'hidroxil a l'esquerra a C3 ia la dreta a C4 i C5; mentre que l'altre isòmer té el patró invers. Aquests noms de monosacàrids específics tenen abreviatures convencionals de tres lletres, com "Glu" per a glucosa i "Thr" per a treosa.
Generalment, un monosacàrid amb n carbonis asimètrics té 2 n estereoisòmers. El nombre d'estereoisòmers de cadena oberta per a un monosacàrid d'aldosa és més gran en un que un monosacàrid de cetosa de la mateixa longitud. Cada cetosa tindrà 2(n −3) estereoisòmers on n > 2 és el nombre de carbonis. Cada aldosa tindrà 2 (n −2) estereoisòmers on n > 2 és el nombre de carbonis. Aquests també es coneixen com a epímers que tenen una disposició diferent dels grups -OH i -H als àtoms de carboni asimètrics o quirals (això no s'aplica als carbonis que tenen el grup funcional carbonil).
Configuració de monosacàrids
[modifica]Igual que moltes molècules quirals, els dos estereoisòmers del gliceraldehid rotaran gradualment la direcció de polarització de la llum polaritzada linealment a mesura que passa a través d'ella, fins i tot en solució. Els dos estereoisòmers s'identifiquen amb els prefixos D i L, segons el sentit de gir: D-gliceraldehid és dextrorrotatori (gira l'eix de polarització en el sentit de les agulles del rellotge), mentre que L-gliceraldehid és levorrotatori (ho gira en el sentit contrari a les agulles del rellotge).

Els prefixos D i L també s'utilitzen amb altres monosacàrids per distingir dos estereoisòmers particulars que són imatges especulars entre si. Per a aquest propòsit, es considera el carboni quiral més allunyat del grup C=O. Els seus quatre enllaços s'han de connectar amb −H, −OH, −C(OH)H i la resta de la molècula. Si la molècula es pot girar a l'espai de manera que les adreces d'aquests quatre grups coincideixin amb les dels grups anàlegs al C2 del D -gliceraldehid, llavors l'isòmer rep el prefix D-. En cas contrari, rep el prefix L-.
A la projecció de Fischer, els prefixos D- i L- especifiquen la configuració a l'àtom de carboni que és el segon des de baix: D- si l'hidroxil és al costat dret, i L- si és a la banda esquerra. Els prefixos D- i L- no indiquen la direcció de rotació de la llum polaritzada, que és un efecte combinat de la disposició a tots els centres quirals. Tot i això, els dos enantiòmers sempre rotaran la llum en direccions oposades, en la mateixa quantitat. Vegeu també sistema D/L.
Ciclació de monosacàrids (formació d'hemiciatal)
[modifica]Un monosacàrid sovint canvia de la forma acíclica (cadena oberta) a una forma composta cíclica, a través d'una reacció d'addició nucleòfila entre el grup carbonil i un dels grups hidroxil de la mateixa. molècula. La reacció crea un anell d'àtoms de carboni tancat per un àtom d'oxigen pont. La molècula resultant té un grup hemiacetal o hemicetal, depenent de si la forma lineal era una aldosa o una cetosa. La reacció s'inverteix fàcilment donant la forma original de cadena oberta.
En aquestes formes cícliques, l'anell acostuma a tenir cinc o sis àtoms. Aquestes formes es denominen furanoses i piranoses, respectivament, per analogia amb el furà i el piran, els compostos més simples amb el mateix anell carboni-oxigen (encara que manquen dels dobles enllaços d'aquestes dues molècules). Per exemple, la glucosa aldohexosa pot formar un enllaç hemiacetal entre el grup aldehid al carboni 1 i l'hidroxil al carboni 4, donant lloc a una molècula amb un anell de 5 membres, anomenada glucofuranosa. La mateixa reacció pot tenir lloc entre els carbonis 1 i 5 per formar una molècula amb un anell de 6 membres, anomenada glucopiranosa. Les formes cícliques amb un anell de set àtoms (el mateix de l'oxepà), que poques vegades es troben, es denominen heptoses.



En molts monosacàrids (inclosa la glucosa), predominen les formes cícliques, en estat sòlid i en solucions, i, per tant, s'usa comunament el mateix nom per als isòmers de cadena oberta i tancada. Així, per exemple, el terme “glucosa” pot significar glucofuranosa, glucopiranosa, la forma de cadena oberta o una barreja de les tres.
La ciclació crea un nou estereocentre al carboni que conté carbonil. El grup −OH que reemplaça l‟oxigen del carbonil pot acabar en dues posicions diferents en relació amb el pla mitjà de l‟anell. Així, cada monosacàrid de cadena oberta produeix dos isòmers cíclics (anòmers), indicats pels prefixos α- i β-. La molècula pot canviar entre aquestes dues formes mitjançant un procés anomenat mutarrotació, que consisteix en una inversió de la reacció de formació de l'anell seguida de la formació d'un altre anell.[7]
Projecció de Haworth
[modifica]L'estructura estereoquímica d'un monosacàrid cíclic es pot representar en una projecció de Haworth. En aquest diagrama, l'isòmer α de la forma piranosa d'una D-aldohexosa té el −OH del carboni anomèric per sota del pla dels àtoms de carboni, mentre que l'isòmer β té el −OH del carboni anomèric per sobre del pla. Les piranoses solen adoptar una conformació de cadira, similar a la del ciclohexà. En aquesta conformació, l'isòmer α té el −OH del carboni anomèric en posició axial, mentre que lʻisòmer β té el −OH del carboni anomèric en posició equatorial (considerant sucres D-aldohexoses).
-
α-D-Glucopiranosa
-
β-D-Glucopiranosa
Propietats
[modifica]Els monosacàrids tenen unes propietats físiques que els diferencien de la resta de glúcids. Aquestes característiques principals són les següents: són sòlids cristal·lins, de color blanc, de gust dolç i solubles en aigua a causa de l'elevada polaritat dels grups hidroxil i carbonil que estableixen interaccions amb el dipol de les molècules d'aigua.
L'abundància de grups hidroxil (OH) a la seva molècula fa que les oses siguin molt solubles en aigua. Les solucions aquoses concentrades de monosacàrids són viscoses. Els xarops de monosacàrids són molt viscosos (la cristal·lització és difícil). Això es pot facilitar mitjançant l'addició de dissolvents orgànics (metanol, etanol, etc.) i en condicions de calor (presència de calor) quan les oses són poc solubles.
Els monosacàrids tenen un poder rotatori definit (a excepció d'aquelles amb un grup cetona, com la dihidroxiacetona), cosa que proporciona una manera d'identificació per polarimetria.
Alguns moosacàrids tenen un sabor agradablement dolç, però és erroni generalitzar sobre aquesta propietat perquè altres compostos que no són monosacàrids, com la glicina o l'àcid aspàrtic (del qual deriva l'edulcorant aspartam), per exemple, tenen també un sabor dolç sense ser sucres.
Funcions
[modifica]Tots els monosacàrids tenen una funció energètica de proporcionar energia. Aquesta funció és possible gràcies a la seva capacitat d'oxidar-se, és a dir, de perdre electrons davant de substàncies que en acceptar-los, es redueixen. A més, tenen la capacitat d'associar-se amb grups amino (-NH₂) per formar aminoglúcids com ara la glucosamina.
Els monosacàrids poden unir-se entre si mitjançant l'enllaç glicosídic en què el grup hidroxil d'un monosacàrid reacciona amb el grup hidroxil d'una altra i es desprèn una molècula d'aigua; d'aquesta manera es poden formar llargues cadenes, ramificades o no, denominades polisacàrids.
Isomeria
[modifica]La majoria de monosacàrids tenen algun carboni asimètric, és a dir, un àtom de carboni que té les seves quatre valències saturades per radicals diferents. Si se situa el carbonil a dalt i ens fixem l'últim carboni asimètric, el grup -OH pot estar a la dreta o a l'esquerra; en el primer cas, es tracta d'un D-monosacàrid; en el cas que estigués a l'esquerra seria un L-monosacàrid. Cadascuna d'aquestes formes són isòmers espacials o estereoisòmers entre si i atès que són la imatge especular l'un de l'altre, s'anomenen enantiomorfs. La majoria dels monosacàrids presents als éssers vius són formes D.
Classificació
[modifica]Classifiquem els monosacàrids segons el nombre d'àtoms de carboni que hi ha a la cadena. Per anomenar-los utilitzem el nombre de carbonis i li afegim el prefix -osa. Hi ha cinc tipus de monosacàrids: trioses, tetroses, pentoses, hexoses i heptoses. Aquests tipus es diferencien depenent de si tenen un grup aldehid o una cetona.
| Fórmula | Aldoses | Cetoses | |
|---|---|---|---|
| Trioses | C₃H₆O₃ | glicerosa o gliceraldehid | dihidroxiacetona |
| Tetroses | C₄H₈O₄ | eritrosa | eritulosa |
| Pentoses | C₅H10O₅ | ribosa | ribulosa |
| Hexoses | C₆H₁₂O₆ | glucosa | fructosa |
Trioses
[modifica]Les trioses són monosacàrids formats per una cadena de tres àtoms de carboni. Aquestes cadenes són molt abundants a l'interior de la cèl·lula, ja que són metabòlits que participen en la degradació de la glucosa.
Com en els altres monosacàrids, en les trioses apareixen els grups cetona i aldehid també anomenats grups funcionals carbonil. Si tenen un grup cetona, se'ls anomena afegint el prefix ceto- i si porten un grup aldehid, s'afegeix el prefix aldo-, de manera que els compostos que tinguin un grup aldehid s'anomenaran aldotrioses (o gliceraldehids) i les cadenes que tinguin un grup cetona s'anomenaran cetotrioses (o dihidroxiacetona).
Isòmers espacials o estereoisòmers
[modifica]La isomeria espacial o estereoisomeria és l'existència de molècules amb la mateixa fórmula molecular però diferent estructura espacial, per la qual cosa tenen diferents propietats. L'estereoisomeria es produeix sempre que hi ha algun àtom de carboni asimètric, que és quan un carboni està unit a quatre radicals diferents. Tots els monosacàrids en tenen algun excepte la dihidroxiacetona que no posseeix carbonis asimètrics.
Els isòmers són compostos amb la mateixa fórmula química però diferent estructura. Es diuen isòmers òptics els estereoisòmers que tenen les mateixes propietats químiques però diferent activitat òptica. Els isòmers òptics poden ser:
- Enantiòmers o enantiomorfes: Un estereoisòmer és la imatge especular de l'altre, no superposable.
- Diastereoisòmers: Els que no són imatges especulars de l'altre.
El nombre d'isòmers òptics (o estereoisòmers) que presenta una biomolècula és igual a 2n, sent "n" el nombre de carbonis asimètrics que té.
Per exemple, el gliceraldehid té el segon àtom de carboni asimètric, a causa d'això podem distingir dos isòmers espacials o estereoisòmers. El D-gliceraldehid quan el -OH és a la dreta, i el L-gliceraldehid quan el -OH és a l'esquerra. Aquests isòmers especials són la imatge especular de l'altre, i per tant són estructures enantiomorfes, encara que girin a l'espai no podran coincidir mai, ja que són estructures diferents.
Tetroses
[modifica]Les tetroses són monosacàrids de quatre carbonis.[8] Diferenciem dos tipus: les aldoses (tenen un grup aldehid terminal en el carboni 1) i les cetoses (tenen un grup cetona en l'àtom de carboni 2). Hi ha dues aldotetroses: la treosa i l'eritrosa. Aquestes tenen dos carbonis asimètrics en els carbonis 2 i el 3. A dins d'aquest grup de les tetroses també trobem una cetotetrosa: l'eritrulosa, la qual només té un carboni asimètric, el tercer.
Quan dos glúcids només es diferencien en la posició del grup hidroxil en un carboni asimètric s'anomenen epímers. Així, per exemple, la L-eritrosa i la L-treosa són epímers, però són substàncies diferents i per tant, amb propietats diferents.
Pentoses
[modifica]Les pentoses són monosacàrids formats per una cadena de cinc àtoms de carboni. En les pentoses apareixen grups alcohols (OH).[9] A causa de la seva importància cal destacar les següents pentoses: les aldopentoses D-ribosa, en l'ARN i la D-2-desoxiribosa en l'ADN. També cal destacar la D-ribulosa, que durant la fotosíntesi reacciona amb diòxid de carboni, i gràcies a aquest procés, la matèria inorgànica passa a ser matèria orgànica.
L'estructura de les pentoses més estable, a diferència d'altres monosacàrids, no és la lineal, sinó que és la cíclica. Això és degut als enllaços que es formen entre els àtoms de carboni, ja que les cadenes tendeixen a tancar-se i formar una figura pentagonal. A aquestes pentoses cícliques les anomenem furanoses.
Per fer-ho, han de formar enllaços hemiacetals, que són la conseqüència de la reacció entre el carbonil d'un grup aldehid present en un extrem de les aldoses (o el grup cetona de l'extrem de les cetoses) i un grup hidroxil d'un alcohol de l'extrem oposat. Aquests grups donen poder reductor a la molècula i permeten identificar-los al laboratori. A conseqüència de la ciclització, el carboni del grup funcional hemiacetal (C1 de les aldohexoses i el C2 de les cetohexoses) passa a ser un nou carboni asimètric anomenat anomèric. Segons la posició del grup -OH a un costat o l'altre del pla, es distingeixen dues noves estructures: l'anòmer α que té el grup –OH a baix, i l'anòmer β que és a la part superior del pla.
Les formes cícliques poden ser representades donant-li un sentit tridimensional d'acord amb la formulació de Haworth. Com que l'anell de piranosa no és pla, pot adoptar dues conformacions en l'espai: la forma "cis" o de nau i la "trans" o cadira de muntar.
Hexoses
[modifica]Les hexoses són monosacàrids amb sis àtoms de carboni.[10] Igual que en les pentoses, a causa dels angles que formen els enllaços químics dels carbonis entre si, la seva estructura més freqüent és cíclica quan està en dissolució. Això és possible gràcies al fet que es formen enllaços hemiacetals entre els carbonis. Les hexoses que cal destacar són l'aldohexosa més abundant que és la glucosa i la cetohexosa més abundant en els vegetals és la fructosa.
La glucosa és l'únic sucre que poden cremar els mitocondris (la respiren) per obtenir energia i es pot unir per formar polímers com el glicogen, el midó i la cel·lulosa. Es considera el glúcid més important, ja que atribueix a les cèl·lules la majoria de l'energia que necessiten. Per l'altra banda, la fructosa i la galactosa són els sucres de la fruita i de la llet respectivament.
Derivats
[modifica]Hi ha una gran quantitat de monosacàrids modificats biològicament importants:
- Aminosucres com:
- Sulfosa sucres com:
- Altres com:
Funcions en els éssers vius
[modifica]Tots els monosacàrids tenen una funció energètica de proporcionar energia. Aquesta funció és possible gràcies a la seva capacitat d'oxidar-se, és a dir, de perdre electrons davant de substàncies que en acceptar-los, es redueixen. A més, tenen la capacitat d'associar-se amb grups amino (-NH₂) per formar aminoglúcids com, per exemple, la glucosamina.
Els monosacàrids es poden unir entre si mitjançant l'enllaç glicosídic en què el grup hidroxil d'un monosacàrid reacciona amb el grup hidroxil d'un altre i es desprèn una molècula d'aigua; d'aquesta manera es poden formar llargues cadenes, ramificades o no, anomenades polisacàrids.
Referències
[modifica]- ↑ «monosacàrid». Gran Enciclopèdia Catalana. [Consulta: 25 juny 2022].
- ↑ Collins, P. M.. Monosaccharides : their chemistry and their roles in natural products. Chichester ; New York : Wiley & Sons, 1995, p. 4. ISBN 978-0-471-95343-2.
- ↑ «MetaCyc a monosaccharide». biocyc.org. [Consulta: 25 juny 2022].
- ↑ «IUPAC - monosaccharides (M04021)». goldbook.iupac.org. [Consulta: 25 juny 2022].
- ↑ Hörner, Thomas G.; Klüfers, Peter «The Species of Fehling's Solution» (en anglès). European Journal of Inorganic Chemistry, 2016, 12, 4-2016, pàg. 1798–1807. DOI: 10.1002/ejic.201600168. ISSN: 1434-1948.
- ↑ «Carbohydrates». [Consulta: 10 març 2017].
- ↑ Pigman, William Ward. «Chapter 4: Mutarotations and Actions of Acids and Bases». A: Pigman and Horton. The Carbohydrates: Chemistry and Biochemistry. 2nd. San Diego: Academic Press, 1972, p. 165–194.
- ↑ «tetrosa». Gran Enciclopèdia Catalana. [Consulta: 25 juny 2022].
- ↑ «pentosa». Gran Enciclopèdia Catalana. [Consulta: 25 juny 2022].
- ↑ «hexosa». Gran Enciclopèdia Catalana. [Consulta: 25 juny 2022].