Reacció de Wittig
La reacció de Wittig és una reacció química en la que un aldehid o cetona reacciona amb un ilur de fòsfor (també anomenat fosforà) obtenint-se un alquè i òxid de trifenilfosfina com a subproducte.[1]

La reacció porta el nom del seu descobridor, Georg Wittig, premi Nobel de química l'any 1979 juntament amb Herbert C. Brown "pel desenvolupament de compostos borats i fosforats i el seu ús com a reactius en síntesi orgànica".
Aquesta és la reacció més àmpliament utilitzada en síntesi orgànica per la preparació d'alquens a partir de compostos carbonílics.
Mecanisme
[modifica]L'atac nucleofílic de l'ilur de fòsfor sobre l'espècie carbonílica condueix al zwitterió 3, anomenat betaïna. Aquesta espècie evoluciona formant l'oxafosfetà 4. La gran estabilitat de l'enllaç P=O actua de driving force de la reacció, portant finalment a l'obtenció de l'alquè i l'òxid de trifenilfosfina.

Ilurs de fòsfor
[modifica]Els ilurs de fòsfor es poden representar mitjançant dues formes ressonants. La forma neutre 1 (anomenada fosforà), i la forma zwitteriònica 2 (anomenada ilur). En aquesta última estructura ressonant es pot observar millor el caràcter electrònicament ric del carboni unit a l'àtom de fòsfor.

Preparació
[modifica]Els ilurs de fòsfor se sintetitzen en dos passos. En el primer pas es prepara la sal de fosfoni corresponent per reacció entre un halur d'alquil i trifenilfosfina (1). Posteriorment, aquesta sal de fosfoni se sotmet a un tractament bàsic obtenint-se l'ilur desitjat (2). L'acidesa del protons del carboni α-fòsfor facilita aquest últim pas.

Tipus d'ilurs. Estereoquímica
[modifica]Segons la naturalesa del substituent de l'ilur (R), aquests es poden classificar en tres tipus: estabilitzats, "semi-estabilitzats" i no estabilitzats. D'aquesta manera, el grup R determina la força de la base que s'haurà d'utilitzar per generar l'ilur, i també l'estereoquímica de l'alquè format.
- Els ilurs estabilitzats són aquells que presenten un grup R que els permet estabilitzar de manera eficient la càrrega negativa present en l'àtom de carboni de l'ilur, com per exemple els grups nitril (-CN) o èster (-CO₂R). En aquest cas, es poden utilitzar bases febles per generar l'ilur (NaOH, KOH, K₂CO₃) i s'obté de manera majoritària l'alquè E.
- Els ilurs "semi-estabilitzats" són aquells que presenten un grup R que els permet estabilitzar lleugerament la càrrega negativa, com per exemple els grups fenil (Ph) i vinil (-CH=CH₂). En aquest cas, per generar l'ilur es necessiten bases més fortes. Normalment s'utilitzen alcòxids (NaOEt, tBuOK), tot i que també s'ha descrit la utilització d'altres tipus de bases, com per exemple l'hidròxid de liti (LiOH).[2] Amb aquest tipus d'ilurs s'obtenen mescles dels productes E/Z.
- Els ilurs no estabilitzats presenten un grup R que no permet l'estabilització de la càrrega negativa, com per exemple les cadenes alquíliques o els àtoms d'hidrogen. Aquest tipus d'ilurs són molt inestables i reactius, porten a la formació majoritària de l'alquè Z, i es necessiten bases fortes per generar l'ilur, com el butil-liti (BuLi), el diisopropilamidur de liti (LDA) o l'hidrur sòdic (NaH).
Per exemple, en el cas d'utilitzar acetaldehid com a substrat, caldria esperar els següents resultats:

Tot i això, s'ha de tenir en compte que això no deixa de ser una simplificació, i que l'estereoquímica dels productes formats dependrà també de les condicions de reacció (temperatura, dissolvent).
Modificació de Schlosser
[modifica]La modificació de Schlosser és una variant de la reacció de Wittig que permet obtenir majoritàriament alquens E utilitzant ilurs no estabilitzats. 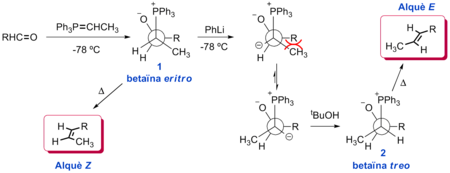 Aquest procediment es basa a fer reaccionar l'ilur amb el compost carbonílic a baixa temperatura (evitant així l'evolució cap a l'alquè perquè la betaïna és estable a baixa temperatura) i seguidament s'addiciona fenil-liti (PhLi), que és una base forta. Amb això s'aconsegueix desprotonar el carboni adjacent a l'àtom de fòsfor (que és el més àcid) de la betaïna, formant-se el β-oxidoilur eritro. Es poden utilitzar altres alquil-litis per a aquesta funció (metil-liti, butil-liti, etc.) si bé s'ha demostrat que utilitzant fenil-liti s'obté generalment millor selectivitat a favor de l'isòmer E.[3]
Aquest procediment es basa a fer reaccionar l'ilur amb el compost carbonílic a baixa temperatura (evitant així l'evolució cap a l'alquè perquè la betaïna és estable a baixa temperatura) i seguidament s'addiciona fenil-liti (PhLi), que és una base forta. Amb això s'aconsegueix desprotonar el carboni adjacent a l'àtom de fòsfor (que és el més àcid) de la betaïna, formant-se el β-oxidoilur eritro. Es poden utilitzar altres alquil-litis per a aquesta funció (metil-liti, butil-liti, etc.) si bé s'ha demostrat que utilitzant fenil-liti s'obté generalment millor selectivitat a favor de l'isòmer E.[3]
Després del tractament bàsic es deixa augmentar suaument la temperatura, de manera que el β-oxidoilur derivat de la forma eritro 1 es converteix al derivat de la forma treo, més estable (menor impediment estèric). El tractament final amb tert-butanol (tBuOH) porta a la betaïna treo 2, que augmentant la temperatura permet l'obtenció de l'alquè E.
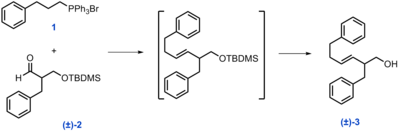
Un exemple recent de la utilització de la modificació de Schlosser és la síntesi del compost bifenílic (±)-3.[4] Utilitzant aquesta metodologia els autors aconsegueixen invertir totalment la selectivitat de la reacció, passant de tenir una relació E/Z de 12:88 a 87:13.
Aplicació
[modifica]La reacció de Wittig és sens dubte el mètode més emprat per a la síntesi d'alquens, obtenint-se bons resultats amb la majoria d'aldehids i cetones. Tot i això, la reacció sol funcionar millor amb aldehids, ja que les cetones són compostos menys electròfils. Aquest fet és especialment rellevant amb cetones impedides estèricament, observant-se disminucions importants en el rendiment d'aquestes reaccions. L'alternativa en aquests casos és la reacció de Horner-Wadsworth-Emmons.
Referències
[modifica]- ↑ Per un article de revisió sobre aquesta reacció vegeu: Maryanoff, B. E.; Reitz, A. B. Chem. Rev. 1989, 863-927. doi:10.1016/10.1021/cr00094a007
- ↑ Antonioletti, R; Bonadies, F., Ciammaichella, A.; Viglianti, A.; Tetrahedron 2008, 4644-4648. doi:10.1016/j.tet.2008.02.091
- ↑ Wang, Q.; Deredas, D.; Huynh, C.; Schlosser, M. Chem. Eur. J. 2003, 570-574.doi:10.1002/chem.200390061
- ↑ Wiktelius, D.; Berts, W.; Jenmalm Jensen, A.; Gullbo, J.; Saitton, S.; Csöregh, I.; Luthman, K. Tetrahedron 2006, 3600-3609. doi:10.1016/j.tet.2006.01.095
Bibliografia
[modifica]- Clayden, J.; Greeves, N.; Warren, S.; Wothers, P., Organic chemistry, Oxford University Press, 2001.
Enllaços externs
[modifica]- Organic-chemistry.org (anglès)
- Premi Nobel de Química 1979 (anglès)
- Mecanisme interactiu de la reacció (anglès)
