Polycaprolactam
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
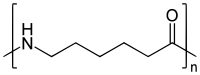
| |||||||
| Allgemeines | |||||||
| Name | Polycaprolactam | ||||||
| Andere Namen |
| ||||||
| CAS-Nummer | 25038-54-4 | ||||||
| PubChem | 32775 | ||||||
| Art des Polymers | |||||||
| Eigenschaften | |||||||
| Aggregatzustand |
fest | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Polycaprolactam (Polyamid-6, PA6, als Handelsmarke Perlon) ist ein Polymer aus der Gruppe der Polyamide. Dieses Polymer wurde von Paul Schlack (IG Farben) synthetisiert, um die Eigenschaften von Nylon 6,6 zu reproduzieren ohne das geltende Produktionspatent zu verletzen.
Herstellung
Polyamid 6 entsteht durch Ringöffnungspolymerisation von ε-Caprolactam. Die zum Kettenstart benötigte, bifunktionale ω-Aminocapronsäure wird aus der hydrolytischen Ringöffnung von ε-Caprolactam gewonnen.
Diese reagiert zusammen mit Caprolactam unter Ausbildung einer Amidbindung zum Polycaprolactam.
Verwendung
Polycaprolactam findet als Kunstfaser unter dem Namen Perlon Verwendung.[1]
Eine Vielzahl gegossener (PA6G) und extrudierter (PA6E) Bauteile werden aus Polycaprolactam (PA6) hergestellt.
Zusätzlich wird es als Trägermaterial (stationäre Phase) in der Dünnschicht- und Säulenchromatographie verwendet.[2]
Unter dem Namen "Polyamid 6" (PA6) wird es auf Grund der Zähigkeit und Verschleißfestigkeit im Maschinenbau für gering belastete Zahnräder und Schrauben, sowie wegen der guten Gleiteigenschaften für hoch belastete Gleitlager und -platten verwendet.[3]
Einzelnachweise
- ↑ Karl-Heinz Lautenschläger, Werner Schröter: Taschenbuch der Chemie, Harri Deutsch Verlag, 2007, Google Books.
- ↑ Reinhard Matissek, Gabriele Steiner, Markus Fischer: Lebensmittelanalytik. 4. Auflage. Springer, Berlin 2010, ISBN 978-3-540-92205-6.
- ↑ EUROPA Tabellenbuch Metall

