Amineptin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
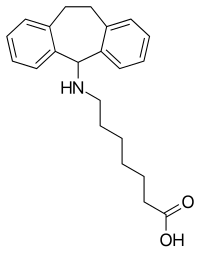
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Amineptin | |||||||||||||||||||||
| Andere Namen |
7-[(10,11-Dihydro-5H-dibenzo[a,d]-cyclohepten-5-yl)amino]heptansäure (IUPAC) | |||||||||||||||||||||
| Summenformel | C22H27NO2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 337,2 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Amineptin ist ein atypisches trizyklisches Antidepressivum, das selektiv die Wiederaufnahme von Dopamin und Noradrenalin hemmt. Es wurde 1978 vom französischen Pharmakonzern Servier unter dem Handelsnamen Survector eingeführt (in Italien auch als Maneon). Da Amineptin vorwiegend dopaminerg ist, tritt die Stimmungsaufhellung wesentlich schneller ein als bei herkömmlichen Antidepressiva, die vorwiegend serotonerg und/oder noradrenerg wirken. Die stark euphorisierende und stimulierende Wirkung hat auch zu einigen Fällen nicht-medizinischer Verwendung geführt. Im Jahr 1999 wurde das Medikament in Frankreich und Portugal aufgrund des Gebrauchs als Rauschmittel, seines Abhängigkeitspotenzials und seiner Hepatotoxizität freiwillig vom Markt genommen.[4][5] In der Folge wurde die Produktion weltweit im Jahr 2005 ganz eingestellt.
Therapeutische Indikationen
[Bearbeiten | Quelltext bearbeiten]Amineptin wurde ursprünglich zur Behandlung von schweren Depressionen entwickelt. Off-Label wurde es auch gegen die Parkinson-Krankheit und Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) eingesetzt.
Wirkmechanismus
[Bearbeiten | Quelltext bearbeiten]Amineptin bewirkt eine starke Wiederaufnahmehemmung von Dopamin, eine Wiederaufnahmehemmung von Noradrenalin und geringfügig auch anticholinerge und antihistamine Effekte.
Nichtmedizinischer Gebrauch
[Bearbeiten | Quelltext bearbeiten]Amineptin besitzt in Kombination mit anderen Arzneien ein deutliches Abhängigkeitspotential. Es entwickelt mit Kokain eine Kreuztoleranz. Im Sport wird Amineptin als Dopingmittel eingesetzt.[6]
Rechtsstatus
[Bearbeiten | Quelltext bearbeiten]In der Bundesrepublik Deutschland ist Amineptin laut Anlage II zu § 1 Abs. 1 Betäubungsmittelgesetz[7] ein verkehrsfähiges, aber nicht verschreibungsfähiges Betäubungsmittel. Der Besitz ist ohne Erlaubnis der Bundesopiumstelle beim Bundesinstitut für Arzneimittel und Medizinprodukte strafbar. In Deutschland kam Amineptin nie auf den Markt.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Amineptin-Hydrochlorid: CAS-Nr.: 30272-08-3, EG-Nr.: 250-107-3, ECHA-InfoCard: 100.045.538, PubChem: 44558536, ChemSpider: 32090, DrugBank: DBSALT000803, Wikidata: Q419643.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Amineptin-Natrium: CAS-Nr.: 68946-01-0, PubChem: 71587238, ChemSpider: 32698049, Wikidata: Q27264462.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Docket No. 02N-0101. U.S. Food and Drug Administration, 9. April 2002, abgerufen am 30. Januar 2014 (englisch): „In 1999, amineptine products were voluntarily removed from the market in France and Portugal due to risks of misuse and addiction.“
- ↑ Docket No. 03N-0015. U.S. Food and Drug Administration, 3. Februar 2003, abgerufen am 30. Januar 2014 (englisch): „It has been withdrawn from the market in France, where the drug was developed a few decades ago, for reasons of considerable hepatotoxicity and abuse.“
- ↑ Eve&Rave.
- ↑ Betäubungsmittelgesetz (BGBl. I 2001, 1187 - 1189), Anlage II; Stand 14. November 2011.