Ethan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ethan | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | C2H6 | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchloses Gas[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 30,07 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
−88,6 °C[2] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[2] | |||||||||||||||
| Dipolmoment |
0[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 10000 ml·m−3 bzw. 12500 mg·m−3[5] | |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−84,0 kJ/mol[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Ethan (veraltet auch Äthan) ist eine chemische Verbindung, die den Alkanen zugehört (gesättigte Kohlenwasserstoffe). Es hat die Summenformel C2H6 und ist ein farb- und geruchloses Gas, das vor allem zu Heiz- und Verbrennungszwecken genutzt wird. Davon abgeleitet ist der Ethyl-Rest (–C2H5). Ethan ist neben Methan ein Hauptbestandteil des Erdgases.
Konformation
[Bearbeiten | Quelltext bearbeiten]

Ethan weist zwei Konformationen auf, sie unterscheiden sich in ihrer Energie, die in diesem Fall als Torsionsenergie bezeichnet wird, um etwa 12,6 Kilojoule pro Mol. In der ekliptischen Konformation ist sie am höchsten, sie ist daher instabil. In der gestaffelten Konformation ist sie am niedrigsten, diese ist folglich energetisch bevorzugt. Die Energie aller anderen Konformationen liegt zwischen diesen beiden Extremen.
Die Torsionsenergie des Ethanmoleküls ist bei Raumtemperatur klein gegenüber der thermischen Energie, sodass es sich in konstanter Rotation um die C-C-Achse befindet. Allerdings „rastet“ es in regelmäßigen Abständen in der gestaffelten Konformation „ein“, sodass sich jeweils etwa 99 Prozent aller Moleküle nahe dem Energieminimum befinden. Der Übergang zwischen zwei benachbarten gestaffelten Konformationen dauert durchschnittlich 10−11 Sekunden (siehe auch Konformation von Ethan).
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Ethan ist ein farbloses und geruchloses Gas, es schmilzt bei −182,76 °C und siedet bei −88,6 °C. Es ist nur schlecht in Wasser löslich: 61 mg/l bei 20 °C. Zum Schmelzen werden 583 J/mol benötigt, zum Sieden 10 kJ/mol.
Festes Ethan existiert in mehreren Modifikationen.[7] Bei der Abkühlung von Ethan bei normalem Druck entsteht zunächst eine kubisch kristallisierende Form, bei der die Moleküle um ihre Längsachse rotieren können, weshalb es sich um einen plastischen Kristall handelt. Bei geringfügiger weiterer Abkühlung entsteht bei etwa 89,9 K eine metastabile Modifikation, die im monoklinen System kristallisiert.[8]
Die kritische Temperatur beträgt 32,18 °C, der kritische Druck 48,714 bar und die kritische Dichte 0,2045 g/cm³.[2] Ethan hat einen Heizwert von 64,3 MJ/m³ (47,5 MJ/kg).
Struktur
[Bearbeiten | Quelltext bearbeiten]- Bindungslängen: C-C-Bindung 154 pm, C-H-Bindung 109 pm[9]
- Bindungswinkel: C–H–C: 109,5°, H–C–H 109,5° (Tetraederwinkel)
Vorkommen und Darstellung
[Bearbeiten | Quelltext bearbeiten]| Planet | Ethananteil |
|---|---|
| Jupiter | 5,8 ± 1,5 ppm |
| Saturn | 7 ± 1,5 ppm |
| Neptun | ≈1,5 ppm |
Im Erdgas sowie Sumpfgas finden sich nicht unerhebliche Mengen von Ethan, in der Atmosphäre finden sich allerdings nur Spuren. Die verhältnismäßig großen Mengen von Methan und Ethan auf der Erde sind vor allem auf deren Lebensformen zurückzuführen bzw. der Zersetzung organischer Materie. Sie entstehen aber auch ohne das Beisein von Lebensformen in Anwesenheit von Wasserstoff und Kohlenstoff, da es sehr einfache Verbindungen sind.
Auf den Planeten Jupiter, Saturn und Neptun finden sich Spuren von Ethan. Auch auf manchen Kometen findet sich Ethan, so waren in der Koma des Kometen Hale-Bopp geringe Mengen Ethan zu finden. Die Ethanvorkommen im Weltall sind gering und viel kleiner als die des Methans. Auch auf einigen Monden findet sich Ethan: Auf dem Saturnmond Enceladus finden sich Spuren von Ethan, am 30. Juli 2008 wurde bekanntgegeben, dass der See Ontario Lacus auf Titan hauptsächlich mit Ethan gefüllt ist.[10] Auch auf dem Zwergplaneten Pluto findet sich Ethaneis.
Es kann im Labormaßstab durch Kolbe-Elektrolyse von Essigsäure beziehungsweise Kaliumacetat hergestellt werden.
Gefahren
[Bearbeiten | Quelltext bearbeiten]Ethan führt beim Einatmen zu erhöhten Atem- und Herzfrequenzen. Des Weiteren führt es beim Einatmen in größeren Mengen zu Taubheit in den Gliedern, zu Schlaflosigkeit, mentaler Verwirrung, Koordinations- und Gedächtnisverlust sowie Hyperventilation. Bei Aufnahme führt es zu Übelkeit und Erbrechen. Weil Ethan meist bei tiefen Temperaturen flüssig gelagert wird, kann es bei austretendem Ethan zu Erfrierungen kommen. Ethan ist hochentzündlich.
Zwischen einem Luftvolumenanteil von 2,7 bis 15,5 Prozent bildet es explosive Gemische, wobei das zündwilligste Gemisch einen Anteil von 6,5 Vol-% Ethan enthält. Der Flammpunkt liegt bei −135 °C, die Zündtemperatur bei 515 °C.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Ethan ist in geringen Mengen im Erdgas vorhanden. Es wird zu Heizzwecken in Feuerungsanlagen verbrannt und dient auch als Ausgangsstoff für die Synthese von Ethen, Essigsäure und anderen chemischen Verbindungen. Außerdem wird Ethan als Kältemittel (R 170) in Kälte- und Klimaanlagen verwendet.
Seit den 2010er Jahren gibt es Flüssiggas-Tankschiffe wie die Schiffe der Dragon-Klasse, deren Motoren mit Ethan betrieben werden.
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Ethan verbrennt unter Sauerstoffzugabe zu Wasser und Kohlenstoffdioxid:

Damit die vollständige Oxidation zu Kohlenstoffdioxid ablaufen kann, werden ideale Reaktionsbedingungen benötigt (Hauptkriterium: ausreichend Sauerstoff).
Ethan wird in Wasserstoff und Ethen gespalten:
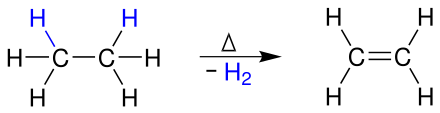
Damit die Reaktion ablaufen kann, ist eine sehr hohe Temperatur (> 700 °C) nötig.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Sicherheitsdatenblatt ( vom 1. Februar 2012 im Internet Archive) (PDF; 39 kB)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu ETHANE in der CosIng-Datenbank der EU-Kommission, abgerufen am 16. September 2021.
- ↑ a b c d e f g h i j Eintrag zu Ethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 1. Februar 2016. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Permittivity (Dielectric Constant) of Gases, S. 6-188.
- ↑ Eintrag zu Ethane im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 74-84-0 bzw. Ethan), abgerufen am 15. September 2019.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-22.
- ↑ G. J. H. van Nes, A. Vos (1978): Single-Crystal Structures and Electron Density Distributions of Ethane, Ethylene and Acetylene. I. Single-Crystal X-ray Structure Determinations of Two Modifications of Ethane. Acta Cryst., Sect. B, vol 34, S. 1947–1956 (doi:10.1107/S0567740878007037).
- ↑ Visualisierung der Kristallstruktur von Ethan als Feststoff.
- ↑ J. L. Duncan, D. C. McKean and A. J. Bruce: Infrared spectroscopic studies of partially deuterated ethanes and the r0, rz, and re structures. In: Journal of Molecular Spectroscopy. Band 74, Nr. 3. Elsevier Inc., März 1979, S. 361–374, doi:10.1016/0022-2852(79)90160-7.
- ↑ DLR: Saturnmond Titan – Ströme und Seen aus flüssigen Kohlenwasserstoffen

