DOPA
Dopa
| Lévodopa | |
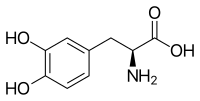
| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.000.405 |
| No CE | 200-445-2 |
| Code ATC | N04 |
| DrugBank | DB01235 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C9H11NO4 [Isomères] |
| Masse molaire[1] | 197,187 9 ± 0,009 4 g/mol C 54,82 %, H 5,62 %, N 7,1 %, O 32,46 %, |
| pKa | lévodopa : pKa1=2,32, pKa2=8,72, pKa3=9,96, pKa4=11,79 à 25 °C |
| Propriétés physiques | |
| T° fusion | 285 °C déc |
| Précautions | |
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La 3,4-dihydroxyphénylalanine (en abrégé, DOPA ou dopa) est une substance intermédiaire dans la synthèse des catécholamines. Elle possède deux isomères optiques, la L-DOPA ou L-dopa (ou lévodopa, dénomination pharmacologique internationale), lévogyre, et la D-DOPA ou D-dopa, dextrogyre.
La L-DOPA est la forme stéréo-isomérique lévogyre métabolisable par l'organisme. Sa décarboxylation par la DOPA-décarboxylase produit la dopamine.
La L-DOPA est capable de franchir la barrière hémato-encéphalique. C'est une substance qui est utilisée dans le traitement de la maladie de Parkinson en augmentant le taux de dopamine.
Dans la maladie de Parkinson
modifierLa L-DOPA s'avère supérieure aux agonistes de la dopamine dans le contrôle des symptômes, avec toutefois plus de complications motrices[2]. Elle freine l'évolution de la maladie[3] et améliore très légèrement l'autonomie du patient[4] (par rapport aux agonistes de la dopamine).
La L-DOPA reste le traitement de choix chez la personne âgée, surtout en cas de troubles cognitifs débutants[5], ces derniers pouvant constituer une contre-indication aux autres médicaments antiparkinsoniens.
L'éradication d'Helicobacter pylori améliorerait les résultats du traitement par la lévodopa[6], ce germe pouvant contribuer à la survenue de la maladie de Parkinson[7].
Mode d'administration
modifierElle se fait par voie orale, en trois prises durant les repas dans le traitement initial[5]. Les doses sont augmentées progressivement et le nombre de prises peut atteindre cinq.
Effets secondaires
modifierLes dyskinésies apparaissent dans près de 40 % des cas après quelques années de traitement[8]. Ces effets secondaires sont dépendants des dosages et sont plus fréquents lorsque la maladie de parkinson survient chez un sujet jeune[5].
Des troubles impulsifs sont décrits dans un peu plus de 10 % des patients traités[9]: addiction aux jeux, achats compulsifs...
Il existe un risque de survenue de glaucome chez les patients ayant un angle irido-cornéen fermé. Une asthénie et des nausées sont décrites[5].
Chez la femme enceinte, il ne semble pas exister un risque augmenté de malformation fœtale[10].
Microbiote intestinal
modifierEn outre sa métabolisation périphérique au niveau des entérocytes et hépatocytes principalement responsable de la majeure partie de la biodisponibilité de la L-DOPA, il est connu depuis les années 1970 que la L-DOPA est aussi métabolisée au niveau du microbiote intestinal[11]. Lorsque Marshall et Warren reçoivent un prix Nobel en 2005 pour la découverte d’Helicobacter pylori dans les ulcères de l’estomac, dites alors « infectieuses », la quadrithérapie résultante : amoxicilline, clarithromycine, métronidazole et oméprazole ont vu chez les patients Parkinsoniens traités à la L-DOPA leurs dyskinésies fortement augmentées, traduisant par conséquent un surdosage sanguin de la L-DOPA pour une même quantité administrée[12]. Ces données cliniques montraient alors une corrélation entre la prise de divers antibiotiques par voie orale et une pharmacocinétique différente de la L-DOPA, laissant par conséquent déduire que le microbiote intestinal a un impact non négligeable sur la pharmacocinétique de ce médicament. Une autre équipe de chercheurs a montré que, dans un premier temps, la L-DOPA est décarboxylée par une tyrosine décarboxylase dépendante du phosphate de pyridoxal appartenant à Enterococcus faecalis. Par la suite, des souches de Eggerthella lenta peuvent déshydroxyler, par une dopamine déshydroxylase dépendante du molybdène, la dopamine pour former de la m-tyramine (qui n'est pas connue pour avoir de conséquence biologique)[13]. En outre, l’équipe de chercheurs a soulevé la question : la carbidopa permet-elle d’inhiber la tyrosine décarboxylase d’E. faecalis en plus de la DOPA carboxylase humaine ? Leurs résultats semblent montrer que non. Ainsi, cela peut montrer que l’utilisation de la carbidopa peut ne pas nécessairement modifier les variations pharmacocinétiques intra et interindividuelles de la L-DOPA chez les patients Parkinsoniens. Cependant ces mêmes chercheurs ont toutefois identifié un dérivé de la tyrosine pouvant inhiber la tyrosine décarboxylase d’E. faecalis : la (S)-α-Fluoromethyltyrosine[13].
Divers
modifierElle fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[14].
Elle reste le traitement antiparkinsonien le moins cher[5].
Voir aussi
modifierNotes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Stowe R, Ives N, Clarke C et al. Dopamine agonist therapy in early Parkinson’s disease, Cochrane Database Syst Rev, 2009;2:CD006564
- Stanley Fahn, David Oakes, Ira Shoulson et Karl Kieburtz, « Levodopa and the progression of Parkinson's disease », The New England Journal of Medicine, vol. 351, no 24, , p. 2498–2508 (ISSN 1533-4406, PMID 15590952, DOI 10.1056/NEJMoa033447, lire en ligne, consulté le )
- PD Med Collaborative Group, Richard Gray, Natalie Ives et Caroline Rick, « Long-term effectiveness of dopamine agonists and monoamine oxidase B inhibitors compared with levodopa as initial treatment for Parkinson's disease (PD MED): a large, open-label, pragmatic randomised trial », Lancet (London, England), vol. 384, no 9949, , p. 1196–1205 (ISSN 1474-547X, PMID 24928805, DOI 10.1016/S0140-6736(14)60683-8, lire en ligne, consulté le )
- Muzerengi S, Clarke CE, Initial drug treatment in Parkinson’s disease, BMJ, 2015;351:h4669
- (en) Hashim H, Azmin S, Razlan H, Yahya NW, Tan HJ, Manaf MR, Ibrahim NM, « Eradication of Helicobacter pylori infection improves levodopa action, clinical symptoms and quality of life in patients with Parkinson's disease », PLoS One, vol. 9, no 11, , e112330. (PMID 25411976, PMCID PMC4239049, DOI 10.1371/journal.pone.0112330, lire en ligne [html])
- (en) Dr Testerman Traci, « Bacteria 'linked' to Parkinson's disease », BBC Online, consulté le 23 mai 2011.
- Ahlskog J, Muenter MD, Frequency of levodopa-related dyskinesias and motor fluctuations as estimated from the cumulative literature, Mov Disord, 2001;16:448-58
- Daniel Weintraub, Juergen Koester, Marc N. Potenza et Andrew D. Siderowf, « Impulse control disorders in Parkinson disease: a cross-sectional study of 3090 patients », Archives of Neurology, vol. 67, no 5, , p. 589–595 (ISSN 1538-3687, PMID 20457959, DOI 10.1001/archneurol.2010.65, lire en ligne, consulté le )
- M. Dostal, C. Weber-Schoendorfer, J. Sobesky et C. Schaefer, « Pregnancy outcome following use of levodopa, pramipexole, ropinirole, and rotigotine for restless legs syndrome during pregnancy: a case series », European Journal of Neurology, vol. 20, no 9, , p. 1241–1246 (ISSN 1468-1331, PMID 23083216, DOI 10.1111/ene.12001, lire en ligne, consulté le )
- B. R. Goldin, M. A. Peppercorn et P. Goldman, « Contributions of host and intestinal microflora in the metabolism of L-dopa by the rat », The Journal of Pharmacology and Experimental Therapeutics, vol. 186, no 1, , p. 160–166 (ISSN 0022-3565, PMID 4723308, lire en ligne, consulté le )
- M. Pierantozzi, A. Pietroiusti, L. Brusa et S. Galati, « Helicobacter pylori eradication and l-dopa absorption in patients with PD and motor fluctuations », Neurology, vol. 66, no 12, , p. 1824–1829 (ISSN 0028-3878 et 1526-632X, DOI 10.1212/01.wnl.0000221672.01272.ba, lire en ligne, consulté le )
- Vayu Maini Rekdal, Elizabeth N. Bess, Jordan E. Bisanz et Peter J. Turnbaugh, « Discovery and inhibition of an interspecies gut bacterial pathway for Levodopa metabolism », Science, vol. 364, no 6445, , eaau6323 (ISSN 0036-8075 et 1095-9203, DOI 10.1126/science.aau6323, lire en ligne, consulté le )
- (en) WHO Model List of Essential Medicines, 18th list, avril 2013
Liens externes
modifier- Page spécifique dans la base de données sur les produits pharmaceutiques (Canada)
- Page spécifique sur le Répertoire Commenté des Médicaments, par le Centre belge d'information pharmacothérapeutique
- Compendium suisse des médicaments : spécialités contenant DOPA
- Page spécifique sur le Vidal.fr
