Rubitecan
| Rubitecan | ||||
|---|---|---|---|---|
| Chemische structuur | ||||
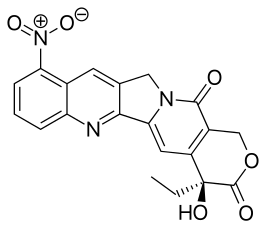
| ||||
| Gebruik | ||||
| Merknamen | Orathecin | |||
| Toediening | oraal | |||
| Databanken | ||||
| CAS-nummer | 91421-42-0 | |||
| PubChem | 11954380 | |||
| Chemische gegevens | ||||
| Molecuulformule | C20H15N3O6 | |||
| IUPAC-naam | (4S)-4-ethyl-4-hydroxy-11-nitro-1H-pyrano[3',4':6,7]indolizino[1,2-b]quinoline-3,14(4H,12H)-dion | |||
| Molmassa | 393,35 g/mol | |||
| ||||
Rubitecan (INN) is een geneesmiddel afgeleid van camptothecine (een natuurlijke plantenstof met een antikankeractiviteit). De chemische formule van rubitecan is 9-nitro-20(S)-camptothecine. Rubitecan werd ontwikkeld door Supergen Inc. uit Dublin (Californië). Zoals camptothecine is rubitecan een topo-isomerase-inhibitor. De stof is niet wateroplosbaar en wordt oraal toegediend. De merknaam van Supergen is Orathecin. Het middel was bedoeld voor de behandeling van alvleesklierkankerpatiënten, maar is niet op de markt.
De Europese Commissie kende op 10 juni 2003 de status van"weesgeneesmiddel" toe aan rubitecan,[1] voor de behandeling van patiënten met voortgezette of metastatische pancreaskanker. Op dat ogenblik waren de klinische proeven met het middel nog aan de gang. Later vond het Europees Geneesmiddelenbureau dat de resultaten van deze proeven[2] onvoldoende aantoonden dat rubitecan een hogere overlevingskans bood dan de standaardgeneesmiddelen zoals gemcitabine of 5-fluoro-uracil; daarenboven waren er talrijke en soms ernstige bijverschijnselen. De aanvrager (voor Europa was dat EuroGen Pharmaceuticals Ltd) trok daarop zijn aanvraag in en het middel kwam niet in de handel.[3]
Ook in de Verenigde Staten heeft Supergen om gelijkaardige redenen de aanvraag voor de toelating van Orathecin ingetrokken.[4][5]
- ↑ Rubitecan EMEA Summary
- ↑ Howard A. Burris, III et al. "Phase II Trial of Oral Rubitecan in Previously Treated Pancreatic Cancer Patients". The Oncologist, Vol. 10, No. 3, 183-190, March 2005 doi:10.1634/theoncologist.10-3-183
- ↑ Vragen en antwoorden over het intrekken van de aanvraag van een vergunning voor het in de handel brengen van Orathecin. EMEA, 2007
- ↑ SuperGen's Orathecin disappoints in Phase II trial. Fierce Biotech, 25 april 2006.
- ↑ SuperGen Announces Withdrawal of Orathecin(TM) NDA PR Newswire, 3 januari 2005
