Azotna kiselina
Azotna kiselina je veoma jaka neorganska kiselina molekulske formule HNO3. To je bezbojna, izuzetno kaustična i otrovna supstanca. Lako isparava, a pri koncentracijama većim od 86% često se naziva pušljiva azotna kiselina. U koncentrovanom obliku izuzetno je jako oksidaciono sredstvo. Prvi ju je sintetisao alhemičar Jabir ibn Hajan oko 9. veka nove ere. Soli ove kiseline nazivaju se nitrati.
| Azotna kiselina | |||
|---|---|---|---|
| |||
 |
 | ||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 7697-37-2 | ||
| PubChem[1][2] | 944 | ||
| ChemSpider[3] | 919 | ||
| UNII | 411VRN1TV4 | ||
| EINECS broj | |||
| UN broj | 2031 | ||
| KEGG[4] | |||
| MeSH | |||
| ChEBI | 48107 | ||
| ChEMBL[5] | CHEMBL1352 | ||
| RTECS registarski broj toksičnosti | QU5775000 | ||
| Gmelin Referenca | 1576 | ||
| 3DMet | B00068 | ||
| Jmol-3D slike | Slika 1 Slika 2 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | HNO3 | ||
| Molarna masa | 63.01 g mol−1 | ||
| Agregatno stanje | bezbojna tečnost | ||
| Gustina | 1,5129 g cm−3 | ||
| Tačka topljenja |
-42 °C, 231 K, -44 °F | ||
| Tačka ključanja |
83 °C, 356 K, 181 °F (68% rastvor ključa na 121 °C) | ||
| Rastvorljivost u vodi | Potpuno se meša | ||
| pKa | -1,4[6] | ||
| Indeks prelamanja (nD) | 1,397 (16,5 °C) | ||
| Dipolni moment | 2,17 ± 0,02 D | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
−207 kJ·mol−1[7] | ||
| Standardna molarna entropija S |
146 J·mol−1·K−1[7] | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | ICSC 0183 PCTL Safety Website | ||
| EU-klasifikacija | |||
| EU-indeks | 007-004-00-1 | ||
| NFPA 704 | |||
| R-oznake | R8 R35 | ||
| S-oznake | (S1/2) S23 S26 S36 S45 | ||
| Tačka paljenja | Nezapaljiva | ||
| Srodna jedinjenja | |||
| Drugi anjoni | Azotasta kiselina | ||
| Drugi katjoni | Natrijum nitrat Kalijum nitrat Amonijum nitrat | ||
| Srodna jedinjenja | Azot-pentoksid | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Hemijske osobine
urediAzotna kiselina u vodenom rastvoru u potpunosti disosuje do NO3- anjona i slobodnog protona koji se vezuje sa molekulima vode iz rastvora gradeći hidronijum jon (H3O+).[8][9][10]
Jako je oksidaciono sredstvo. Može da izreaguje čak i sa površinskim slojem plementih metala, zbog čega se koristi u spremanju carske vode, koja može da rastvara zlato i platinu. Na sobnoj temparaturi to je bezbojna tečnost koja lako isparava, pogotovu pri većim koncentracijama, odavajući žuta do crvenih isparenja.
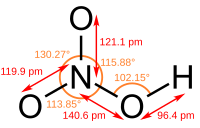
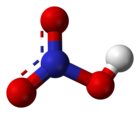
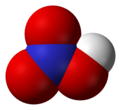
Azotna kiselina gradi veliki broj soli - nitrata - koji su veoma velika i važna grupa jedinjenja. Većina je polarna, te vrlo dobro rastvorna u polarnim rastvaračima, prvenstveno vodi i etanolu. Veze između azota i kiseonika (kako u kiselini tako i u nitratnoj grupi) su sve jednake dužine, sa sp2 hibridizovanim atomom azota, i uglom između veza od 120°, što odgovara planearnom obliku nitratne (nitro) grupe.
Dobijanje
urediAzotna kiselina se može dobiti mešanjem azot (IV)-oksida sa vodom pri čemu se dobija smeša azotne i azotaste kiseline. Prečišćavanje ove smeše se najčešće vrši destilacijom sa sumpornom kiselinom, koja je higroskopna supstanca, pri čemu se povećava udeo azotne kiseline u rastvoru. Azotna kiselina industrijske jačine varira između 50-68%. U laboratoriji se može dobiti i dejstvom koncentrovane sumporne kiseline (H2SO4) na kalijum nitrat (KNO3), i naknadnom destilacijom na temperaturi ključanja nitratne kiseline (83 °C), pri čemu se izdvaja tzv. crvena pušljiva azotna kiselina (u gasnoj fazi) koju je moguće prevesti u konvencionalnu (belu) azotnu kiselinu. Pritom, u destilacionoj posudi ostaje kristalizovan kalijum hidrogensulfat (KHSO4)
Na industrijskom nivou, dobija se Ostvaldovim procesom, nazvanim po Vilhelmu Ostvaldu, oksidacijom amonijaka.
Upotreba
urediU laboratoriji, azotna kiselina je veoma važan reagens, dok je njena upotreba u industriji još značajnija. Koristi se u procesima dobijanja eksploziva (kao nitroglicerin, trinitrotoluen), veštačkih đubriva (amonijum nitrat), prečišćavanja metala u metalurgiji kao i u nekim organskim sintezama.
Bela pušljiva azotna kiselina (koja je praktično anhidrirana kiselina, teoretske ili približne jačine) koristi se kao oksidant u raketama na tečno gorivo.
U kontaktu sa kožom izaziva teške hemijske opekotine karakteristične žute boje, koja je proizvod reakcije kiseline sa jednim od proteina u koži - keratinom.
Izvori
uredi- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Bell, R. P. (1973), The Proton in Chemistry (2nd izd.), Ithaca, NY: Cornell University Press
- ↑ 7,0 7,1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. str. A22. ISBN 978-0-618-94690-7.
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. 0-8493-0487-3.
- ↑ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0-911910-13-1.
Literatura
uredi- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed.. Houghton Mifflin Company. str. A22. ISBN 978-0-618-94690-7.
Vanjske veze
uredi- NIOSH Pocket Guide to Chemical Hazards
- National Pollutant Inventory – Nitric Acid Fact Sheet
- Calculators: surface tensions Arhivirano 2020-02-22 na Wayback Machine-u, and densities, molarities and molalities Arhivirano 2020-02-22 na Wayback Machine-u of aqueous nitric acid
