Kalcijum-karbid
Appearance
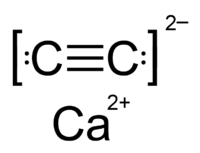
| |

| |
| Nazivi | |
|---|---|
| IUPAC naziv
Calcium Carbide
| |
| Identifikacija | |
| ECHA InfoCard | 100.000.772 |
| Svojstva | |
| CaC2 | |
| Molarna masa | 64,099 g/mol |
| Agregatno stanje | Beli prah ili sivo/crni kristali |
| Gustina | 2,22 g/cm³ |
| Tačka topljenja | 2.160 °C (3.920 °F; 2.430 K) |
| Tačka ključanja | 2.300 °C (4.170 °F; 2.570 K) |
| razlaže se | |
| Struktura | |
| Kristalna rešetka/struktura | Tetragonal[3] |
| Kristalografska grupa | D174h, I4/mmm, tI6 |
| Geometrija molekula | 6 |
| Opasnosti | |
| NFPA 704 | |
| Tačka paljenja | 305 °C (581 °F; 578 K) (acetilen) |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Kalcijum karbid je hemijsko jedinjenje hemijske formule CaC2. Kalcijum karbid je bledih boja, ali većina uzorka imaju boje koje variraju od crne do sivo-bele, zavisno od vrste. Glavna uloga mu je u industrijskoj proizvodnji acetilena i kalcijum cijanida.[5]
Proizvodnja
[uredi | uredi izvor]
Kalcijum karbid se industrijski proizvodi u električnim pećima sjedinjavanjem živog kreča i koksa na temperaturi od 2000 °C. Ovaj metod dobijanja kalcijum karbida se nije promenio još od 1888. kada je pronađen:
- CaO + 3C → CaC2 + CO
Reference
[uredi | uredi izvor]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Massalimov, I. A.; Kireeva, M. S.; Sangalov, Yu. A. (2002). „Structure and Properties of Mechanically Activated Barium Peroxide”. Inorganic Materials. 38: 363. doi:10.1023/A:1015105922260.
- ^ NFPA Hazard Rating Information for Common Chemicals. Northeastern University
- ^ Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. ISBN 978-0-07-049439-8. Pristupljeno 6. 6. 2009.
Literatura
[uredi | uredi izvor]- Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. ISBN 978-0-07-049439-8. Pristupljeno 6. 6. 2009.

