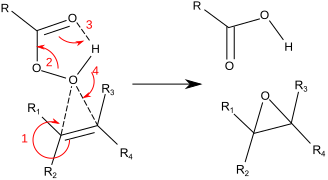Epoksid

Epoksid je ciklični etar sa tročlanim prstenom. Ovaj prsten približno definiše ekvilateralni trougao, iz kog razloga je visoko napregnut. Napregnutost prstena čini epokside reaktivnijim od drugih etara. Jednostavni epoksidi se imenuju po jedinjenju iz kog su izvedeni, etilen oksid ili oksiran, kao u hlorometiloksiran. Kao funkcionalna grupa, epoksidi se označavaju sa epoksi prefiksom, npr. 1,2-epoksicikloheptan, koji se isto tako naziva ciklohepten epoksid, ili jednostavno ciklohepten oksid.[1][2][3]

Polimer koji sadrži neizreagovane epoksidne jedinice se naziva poliepoksid ili epoksi. Epoksi smole se koriste kao adhezivi i strukturni materijali. Polimerizacija epoksida daje polietar, npr. etilen oksid se polimerizuje da formira polietilen glikol, takođe poznat kao polietilen oksid.
Sinteza
[уреди | уреди извор]Industrijski najzastupljeniji epoksidi su etilen oksid i propilen oksid, koji se proizvode u količinama od oko 15 i 3 miliona tona respecktivno.[4] Epoksidacija etilena je katalitička reakcija s kiseonikom koja ima sledeću stehiometriju:
- 7 H2C=CH2 + 6 O2 → 6 C2H4O + 2 CO2 + 2 H2O
Direktna reakcija kiseonika i alkena je korisna samo za ovaj epoksid. Drugi alkeni ne reaguju uspešno. To važi čak i za propilen.
Olefinska peroksidacija
[уреди | уреди извор]Većina epoksida se generiše tretiranjem alkena sa reagensima koji sadrže peroksid, koji donira jedan atom kiseonika. Tipični peroksidni reagensi su vodonik-peroksid, peroksikarboksilna kiselina (generisana in-situ ili pri-formirana), i alkil hidroperoksidi. U specijalnim slučajevima, drugi reagensi koji sadrže peroksid se koriste, npr dimetildioksiran.
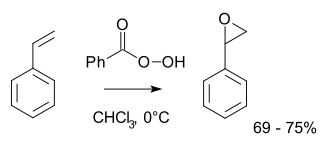
Ovaj pristup nalazi primenu u proizvodnji propilen oksida iz propilena koristeći bilo t-butil hidroperoksid ili etilbenzen hidroperoksid.[5] U laboratorijskim uslovima se češće koristi Prilezhaeva reakcija.[6][7] U ovoj reakciji dolazi do oksidacije alkena peroksikiselinom kao što je m-CPBA. Jedan od primera je epoksidacija stirena perbenzoinskom kiselinom do stiren oksida:[8]
Ova reakcija ima takozvani „mehanizam leptira“.[9] Peroksid deluje kao elektrofil, a alken kao nukleofil.
Hidroperoksidi se takođe koriste u katalitičkoj enantioselektivnoj epoksidaciji, kao što su Šarples epoksidacija i Jakobsenova epoksidacija. U tim slučajevima, kiseonik se prenosi sa metalnog oksida ili peroksida. Zajedno sa Ši epoksidacijom, te reakcije su korisne za enantioselektivnu sintezu hiralnih epoksida. Oksaziridinski reagensi se isto takom mogu koristiti za generisanje epoksida iz alkena.
Intramolekulska SN2 supstitucija
[уреди | уреди извор]Ovaj metod je varijanta Viliamsonove sinteze etara. U ovom slučaju, alkoksidni jon zamenjuje atom hlora unutar istog molekula. Prekursorska jedinjenja su halohidrini. Na primer, sa 2-hloropropanolom se formira propilen oksid:[10]
Približno, polovina proizvedenog propilen oksida nastaje ovim putem.[5] Reakcija intramolekularnog formiranja epoksida je jedan od ključnih koraka u Darzensovoj reakciji.
Nukleofilna epoksidacija
[уреди | уреди извор]Elektron-deficitarni olefini, poput enona i akrilnih derivata mogu da budu epoksidovani upotrebom nukleofilnih jedinjenja kiseonika (npr. peroksida). Ta reakcija ima dvostepeni mehanizam. Prvo kiseonik vrši nukleofilnu konjugovanu adiciju da formira stabilizovani karbanjon. Taj karbanjon zatim napada isti atom kiseonika, zamenjujući njegovu odlazeću grupu, i zatvarajući epoksidni prsten.
Asimetrična epoksidacija
[уреди | уреди извор]Ugljenikovi atomi epoksida su približno sp3-hibridizovani, tako da mogu da budu stereogene pozicije. U zavisnosti od reakcionog mehanizma i geometrije alkenskog početnog materijala, cis i/ili trans epoksidni diastereomeri se mogu formirati. Ako postoje drugi stereocentri u početnom materijalu, oni mogu da utiču na relativnu stereohemiju epoksidacije. Ta diastereoselektivnost je oblik „supstratne kontrole“ reakcije. Epoksidacioni agensi koji poseduju stereogene strukture mogu da utiču na stereohemiju epoksidnog produkta („reagensna kontrola“ reakcije).
Reakcije
[уреди | уреди извор]Tipične epoksidne reakcije su naveden ispod.
- Nukleofilna adicija na epoksid može bude katalisana bazom ili kiselinom.

- U kiseloj sredini, nukleofil napada ugljenik koji formira najstabilniji karbokatjon. U baznoj sredini, nukleofil napada najmanje supstituisani ugljenik, u saglasnosti sa standardnim SN2 reakcionim procesom nukleofilne adicije.
- Hidroliza epoksida u prisustvu kiselog katalizatora generiše glikol. Proces hidrolize epoksida se može smatrati nukleofilnom adicijom vode do epoksida pod kiselim uslovima.
- Redukcija epoksida litijum aluminijum hidridom i vodom generiše alkohol. Taj redukcioni proces se može smatrati nukleofilnom adicijom hidrida (H-) na epoksid pod baznim uslovima.
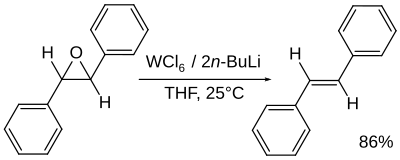
- Redukcija sa volfram heksahloridom i n-butil litijumom generiše alkene. To je reakcija de-epokidacije:[11]
- Reakcija sa NH grupom amina. Formiranje ove kovalentne veze se koristi kod epoksi lepaka, sa npr. trietilentetraminom (TETA) kao stvrdnjivačem.
Reference
[уреди | уреди извор]- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ Morrison Robert Thornton; Boyd Robert Neilson (2006). Organic chemistry. Engelwood Cliffs, New Jersey: Prentice Hall. ISBN 8120307658.
- ^ Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- ^ Rebsdat, Siegfried; Mayer, Dieter (2001). „Ethylene Oxide”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. ISBN 978-3-527-30385-4. doi:10.1002/14356007.a10_117.
- ^ а б Dietmar Kahlich, Uwe Wiechern, Jörg Lindner “Propylene Oxide” in Ullmann's Encyclopedia of Industrial Chemistry, 2002 by Kahlich, Dietmar; Wiechern, Uwe; Lindner, Jörg (2000). „Propylene Oxide”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. ISBN 3-527-30673-0. doi:10.1002/14356007.a22_239.Article Online Posting Date: June 15, 2000
- ^ March, Jerry. 1985. Advanced Organic Chemistry, Reactions, Mechanisms and Structure. 3rd ed. John Wiley & Sons. ISBN 978-0-471-85472-2.
- ^ Nikolaus Prileschajew (1909). „Oxydation ungesättigter Verbindungen mittels organischer Superoxyde”. Berichte der Deutschen Chemischen Gesellschaft. 42 (4): 4811—4815. doi:10.1002/cber.190904204100.
- ^ Harold Hibbert and Pauline Burt (1941). „Styrene Oxide”. Org. Synth.; Coll. Vol., 1, стр. 494
- ^ Bartlett Rec. Chem. Prog 1950, 11 47.
- ^ Koppenhoefer, B.; Schurig, V. (1993). „(R)-Alkyloxiranes of High Enantiomeric Purity from (S)-2-Chloroalkanoic Acids via (S)-2-Chloro-1-Alkanols: (R)-Methyloxirane”. Org. Synth.; Coll. Vol., 8, стр. 434
- ^ K. Barry Sharpless; Martha A. Umbreit; Marjorie T. Nieh; Thomas C. Flood (1972). „Lower valent tungsten halides. New class of reagents for deoxygenation of organic molecules”. J. Am. Chem. Soc. 94 (18): 6538—6540. doi:10.1021/ja00773a045.