製藥產業

製藥產業(英語:Pharmaceutical industry)從事藥物,或是醫療藥品的發現、開發、生產、和銷售的工作,交由醫療衛生提供者施用於患者(或是患者自行給藥),目的在做治癒、預防(透過接種疫苗)、或者是減輕疾病的症狀。[1][2]製藥公司可能也會生產通用名藥物(或稱學名藥,仿製藥)、或是品牌藥、以及醫療器械。這個產業受到各式與專利、測試、安全性、功效、和合法藥物銷售相關法律和規定的規範。
歷史
[編輯]1800年代中期至1945年:從植物性藥物到首度化學合成藥物
[編輯]現代製藥產業起源於早期的地方性藥劑師,他們從傳統的植物性藥物(例如嗎啡和奎寧)的分銷,擴展到1800年代中期的大量生產,以及由應用研究所產生的新發現。德國藥劑師助手弗里德里希·瑟圖納率先有目的的由植物中作藥物發現,他在1803年至1805年間從鴉片中分離出嗎啡(一種鎮痛藥和安眠藥劑),並以希臘夢之神摩耳甫斯為此化合物命名。[3]到1880年代後期,德國染料製造商已把從焦油和其他礦產提煉出純化單體有機化合物的的技術臻於完善,建立起初期的有機化學合成方法。[4]化學合成讓科學家能有系統地改變化學物質的結構,而新興藥理學的發展,也讓科學家更能評估這些變化所造成的生物作用。
腎上腺素、去甲腎上腺素、和苯丙胺
[編輯]到1890年代,腎上腺的提取物對不同組織的深遠影響被發現,引發對化學信號傳導機制的探索,並利用這些發現開發新藥。腎上腺萃取物在血壓升高和血管收縮的作用,特別引起外科醫師的興趣,而將其用作止血劑和休克治療劑,許多公司開發出以腎上腺提取物為基底的產品,各自有不同純度的活性物質。到1897年,約翰·霍普金斯大學醫學院的約翰·阿貝爾確定提取物中的有效成分為腎上腺素,但是他只能萃取出不純的物質。日本籍工業化學家高峰讓吉後來開發一種萃取純淨腎上腺素的方法,並將技術授權給位於美國底特律的藥廠帕克-戴維斯。帕克-戴維斯以「Adrenalin」的商品名稱銷售這種藥物用腎上腺素。注射用腎上腺素在哮喘的急性治療護理特別有效,有一種吸入劑在美國銷售到2011年才停止(商品名Primatene Mist)。[5][6]到1929年,腎上腺素又被調製成吸入劑,用於治療鼻塞。腎上腺素雖然很有效,但注射本身讓使用受到限制,因此業者開始尋求口服的衍生物。日本化學家在一種叫麻黃的植物找到一種結構與腎上腺素相似的化合物麻黃鹼(實際上與去甲腎上腺素更相似),由禮來公司出售,用作治療哮喘的口服藥。化學家和藥理學家Gordon Alles接續英國公司(Burroughs, Wellcome & Co)的Henry Dale和George Barger兩位先生在20世紀初的研究工作成果[7],在1929年合成出苯丙胺(又稱安非他命),並在哮喘患者身上作測試,這種藥僅有中度的抗哮喘作用,但會產生興奮和心悸的感覺。苯丙胺是美國藥廠Smith, Kline & French研發,用於抗鼻塞的藥劑,商品名為苯丙胺吸入劑。苯丙胺最終被用於治療發作性嗜睡病、腦炎後帕金森症候群、以及升高罹患抑鬱症和其他精神疾病患者的情緒之用。苯丙胺被美國醫學協會列入1937年的非公定新藥集(New and Nonofficial Remedy)之中[8],作抗抑鬱症之用,到1960年代因三環類抗抑鬱藥問世而被取代。[6]
巴比妥類藥物發現及開發
[編輯]
1903年,赫爾曼·埃米爾·費歇爾和約瑟夫·馮·梅林披露他們發現-由甲基丙二酸、三氯氧磷、和尿素的反應形成的二乙基丙二酸(diethylbarbituric acid),可導致狗睡眠。這項發現獲得專利,並授權拜耳公司生產,拜耳公司於1904年開始以商品名Veronal作為睡眠輔助劑銷售。拜耳公司對這項藥物做結構變化,然後系統性的研究過其效力和作用時間,在1911年發現苯巴比妥,又在1912年發現苯巴比妥具有有效的抗癲癇活性。到1970年代,苯巴比妥是用於治療癲癇最廣泛的藥物之一,截至2014年,它仍列在世界衛生組織(WHO)的基本藥物清單之內。[9][10](WHO在2019年第21版的基本藥物清單(第5頁)仍包含有此藥物[11])在1950年代和1960年代,人們對巴比妥類藥物和苯丙胺的成癮性和濫用潛力有更多的了解,因而加上更多的使用限制,政府對開立處方人員的監督也日益嚴格。如今,苯丙胺已被廣泛用於治療注意力不足過動症,而苯巴比妥則用於治療癲癇。[12][13]
胰島素
[編輯]從1800年代末期到1900年代初期間所做的一系列實驗顯示出糖尿病是由於缺乏由胰臟所產生的某種物質引起。1869年,奧斯卡·閔可夫斯基和約瑟夫·馮·梅林發現,狗在胰臟被手術切除後,會誘發糖尿病。1921年,加拿大教授弗雷德里克·班廷和他的學生查爾斯·赫伯特·貝斯特重複這項研究,發現注射胰臟萃取物可逆轉胰臟切除後所產生的症狀。很快的,這種萃取物被證明也可用於人體,由於生產足夠數量的萃取物不易,而且純度不足,導致利用胰島素作為常規醫療用途受到耽誤。由於禮來公司具有大規模純化生物材料的經驗,研究人員向其尋求協助以及合作。禮來公司的化學家喬治·沃爾登發現,透過仔細調節萃取物的pH值就可產出相對純淨的胰島素。但由於有多倫多大學的壓力,以及獨立開發出類似純化方法學術界會提出專利挑戰,最後達成由幾家公司共同生產,而非由獨家生產胰島素的協議。在胰島素被發現和廣泛用於治療之前,糖尿病患者的預期壽命通常只剩幾個月。[14]
早期對於抗感染研究:阿斯凡納明、百浪多息、青黴素、和疫苗
[編輯]早期在醫學的研究和開發,重點是找出用於治療感染疾病的藥物。在1900年,肺炎、肺結核、和腹瀉是美國人的頭三大死亡原因,這些疾病造成出生後第一年死亡率超過10%。[15][16]
1911年,柏林實驗療法研究所(德國聯邦保羅·埃爾利希研究所的前身)的保羅·埃爾利希和化學家艾爾弗雷德·伯特共同開發出阿斯凡納明,是第一種合成的抗感染藥物。藥物的商品名為灑爾佛散。[17]埃爾利希注意到砷的一般毒性,和細菌對某些染料會作選擇性吸收,並假設在治療細菌性感染時,可利用具有類似被選擇性吸收特性的含砷染料。合成這類化合物過程中,阿斯凡納明被發現具有部分選擇性的毒性。往後的事實證明阿斯凡納明是首度有效治療梅毒的藥物,在此藥物出現之前,梅毒無法治癒,患者在患病過程中有嚴重的皮膚潰瘍、神經系統損害,最終導致死亡。[18]
埃爾利希系統性改變合成化合物的結構,並測量這些變化對生物活性的影響,這種方法被多位工業科學家,包括在拜耳工作的科學家如Josef Klarer、Fritz Mietzsch、和格哈德·多馬克廣泛採用。由於德國染料產業提供的化合物參與測試,促成百浪多息被開發出,這項產品是磺酰胺類抗生素的首項代表。與阿斯凡納明相比,磺酰胺類藥物具有更廣的活性範圍,而且毒性低得多,可用於治療由鏈球菌屬等病原體引起的感染。[19]多馬克因開發出百浪多息而在1939年獲得諾貝爾生理學或醫學獎。[20][21]但是第二次世界大戰之前人類因為傳染病而死亡人數的急劇下降,主要還是由於公共衛生措施,例如清潔用水和較不擁擠的住房,抗感染藥物和疫苗主要是在第二次世界大戰之後才開始產生明顯的影響。[22][23]
亞歷山大·弗萊明在1928年發現青黴素(也稱為盤尼西林)的抗菌作用,但這種藥物需等到能大規模生產和純化後,才開始用於治療人類疾病。而這些是由美國和英國政府領導的藥廠聯盟在第二次世界大戰期間達成。[24]
在此期間,預防疾病疫苗的開發有初期的進展,主要是透過學術和政府資助的基礎研究進行,這些研究的目的是找出引發常見傳染疾病的病原體。 1885年,路易·巴斯德和皮埃爾·保羅·埃米爾·魯製造出世界首項狂犬病疫苗。世界首項白喉疫苗是在1914年由白喉毒素和白喉抗毒素(從被病菌接種過動物的血清中產生)的混合物製成,由於接種的安全性小,因此並未得到廣泛使用。美國在1921年有206,000例白喉病例記錄,死亡的有15,520人。1923年,巴斯德研究所的加斯頓·拉蒙和惠康研究實驗室(後來併入葛蘭素史克)的亞歷山大·格蘭尼平行分別工作,發現用甲醛處理白喉毒素,可讓疫苗更安全。[25]1944年,在百時美施貴寶前身之一的Squibb Pharmaceuticals工作的莫里斯·希勒曼開發出第一種日本腦炎疫苗。[26]希勒曼後來轉往默克藥廠工作,他在研發針對麻疹、流行性腮腺炎、水痘、風疹、A型肝炎、B型肝炎、和腦膜炎的疫苗開發方面發揮關鍵的作用。
不安全藥物和早期產業法規
[編輯]
在20世紀之前,藥物通常是由小規模的藥廠所生產,雖然當時確有相關的法令,但是對製造的監管控制,以及對藥廠在安全性和功效的聲明,執行並不嚴格。在美國,由於受到污染的天花疫苗和白喉抗毒素接種後所導致的破傷風案例暴發和死亡,促使對於疫苗和其他生物藥物的生產管理得以加強。[27]1902年通過的《生物製劑控制法案》要求聯邦政府為每種生物藥物以及生產此類藥物的過程和設施實施上市前核准。隨後在1906年通過《乾淨食品和藥物法》,法案禁止在州際販售摻假或貼有錯誤訊息標籤的食品和藥品。如果某種藥物含有酒精、嗎啡、鴉片、古柯鹼、或其他幾種有潛在危險或成癮性藥物中的任何一種,而標籤上未註明此類成分的數量或比例,則被視為商標錯誤。政府試圖透過法律,針對藥廠這種標榜無根據功效的行為起訴,但功效被最高法院的一項判決給削弱,這項判決將聯邦政府的執法權限於除非能證明業者為蓄意,否則不能以詐欺罪名起訴。[28]
1937年,有100多人因為攝入由田納西州S.E. Massengill公司生產的"磺胺酏劑"後死亡。這項產品採用具有高毒性溶劑-二甘醇配製而成(目前二甘醇被廣泛用作防凍劑)。[29]根據當時的法律,這個產品僅被處以金額不大的罰款,因為技術上說,在產品上用了"elixir"的字,表示產品含有乙醇溶液,但事實上的溶液是二甘醇,而當時對於二甘醇所含毒性,並未廣為人知(請參考磺胺酏劑中,英文版#History部分)。針對這一事件,美國國會在1938年通過《聯邦食品、藥品和化妝品法案》,首度要求在藥物出售前要有安全性證明,並明確禁止虛假的治療主張。[30][31]
戰後1945年至1970年
[編輯]抗感染研究進一步演進
[編輯]第二次世界大戰之後,在新型抗生素的發現有爆炸式的成長[32],包括有頭孢菌素(由禮來公司根據朱塞佩·布羅祖和愛德華·亞伯拉罕兩位開創性研究成果而開發)、[33][34]鏈黴素(在默克藥廠資助的賽爾曼·A·瓦克斯曼實驗室中發現[35]、四環黴素[36](在Lederle實驗室發現,Lederle後來併入輝瑞公司)、紅黴素(在禮來公司發現)[37],及後來擴展到更為廣泛的細菌病原體抗感染產品。鏈黴素是第一種有效治療結核病的藥物。在發現之時,單獨收容結核病感染者的療養院已普遍存在於已開發國家的城市中,入院後5年內的死亡率高達50%。[35][38]
在1958年發布的聯邦貿易委員會報告,把抗生素的開發對美國公共衛生的影響作量化。報告發現,在1946年至1955年期間,抗生素可治療的疾病發生率下降42%,而不能用抗生素治療的疾病發生率僅下降20%。報告的結論是:"看來,抗生素的使用,加上早期診斷和其他因素,疫情的傳播得以控制,因此疾病的發生率也受到限制"。這項研究對於抗生素可有效治療的八種常見疾病(梅毒、結核病、痢疾、猩紅熱、百日咳、腦膜炎、和肺炎)的死亡率,在同一時期下降56%。[39]其中結核病死亡人數下降75%,成果相當突出。[40]
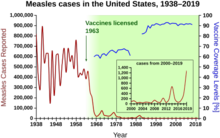
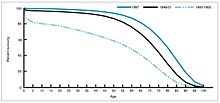
在1940年至1955年期間,美國的死亡率下降速度從每年2%增快到每年8%,然後又回復到每年2%的歷史速度。戰後期間的急劇下降歸因於這些年對於傳染病的新療法和疫苗的快速發展。[22][23]疫苗的開發繼續加速,這一時期最顯著的成就是喬納斯·索爾克在非營利性出生缺陷基金會的資助下,於1954年開發出小兒麻痺疫苗。疫苗的開發從未取得專利,而是轉給藥廠製造出低成本的通用名藥物。1960年,默克藥廠的莫里斯·希勒曼發現SV40病毒,這種病毒後來被證明可引起許多哺乳動物物種的腫瘤。後來確定,SV40是小兒麻痺疫苗製造批次中的一種污染物,當時美國有90%的兒童受過這種疫苗接種。[41][42]污染似乎起源於原始細胞原種,以及起源於用在生產疫苗的猴子組織。2004年,美國國家癌症研究所宣布,SV40與人類癌症無關。[43]
同一時期其他值得注意的新疫苗有麻疹疫苗(1962年,由波士頓兒童醫院的約翰·富蘭克林·恩德斯開發。後來由默克藥廠的莫里斯·希勒曼精製)、風疹(又稱德國麻疹)疫苗(1969年,希勒曼,默克開發)、和腮腺炎疫苗(1967年,希勒曼,默克開發)[44]在美國人廣泛接種疫苗後不久,在風疹、先天性風疹症候群、麻疹、和腮腺炎的發病率下降超過95%。[45]在美國,接受麻疹疫苗接種之後的前20年,估計能降低5,200萬發病例,減少17,400智力受損病例,還有5,200的死亡病例。[46]
抗高血壓藥開發與行銷
[編輯]高血壓是產生人體動脈粥樣硬化、[47]心臟衰竭、[48]冠狀動脈疾病、[49][50]中風、[51]腎病變、[52][53]、和周邊動脈阻塞[54][55]的危險因子,並且也是已開發國家在心血管疾病方面,發病率和死亡率中最主要的危險因子。[56]在1940年之前,年齡在50歲以上的人群中約有23%的死亡歸因於高血壓。嚴重的高血壓須利用手術治療。[57]
早期治療高血壓的方式包括使用季銨鹽交感神經系統阻滯劑,但由於當時尚未確定高血壓對健康產生的長期後果,加上這類化合物有嚴重的副作用,又必須通過注射給藥,而未廣泛使用。
1952年,汽巴精化的研究人員發現第一種口服血管舒張劑肼屈嗪 。[58]使用肼屈嗪的單一療法的主要缺點是有效性會隨時間下降(快速耐受性)。1950年代中期,默克藥廠的Karl H. Beyer、James M. Sprague、John E. Baer、和Frederick C. Novello四位發現並開發出氯噻嗪,氯噻嗪是當今使用最廣泛的降血壓藥。[59]這種進展與高血壓患者的死亡率大幅下降有關。[60]發明人因"挽救無數人的生命,並減輕數以百萬計高血壓患者的痛苦"而獲得1975年公共衛生的拉斯克獎。[61]
在2009年,國際性醫學非政府組織考科藍發表的評論,結論是噻嗪類降血壓藥可降低高血壓患者的死亡風險(相對風險 0.89)、中風(相對風險 0.63)、心臟病(相對風險 0.84)、和心血管狀況(相對風險 0.70)。[62]在隨後的年份中,有其他類別的降血壓藥被開發出,並在組合療法中受到廣泛使用,包括環利尿劑( 呋塞米,商品名Lasix,德國藥廠Hoechst Pharmaceuticals,1963年)、[63]β受體阻滯劑(帝國化學工業,1964年)、[64]血管緊張肽I轉化酶抑制劑(ACE抑制劑)、和血管緊張素II受體拮抗劑。 無論患者是否患有高血壓,ACE抑制劑可降低糖尿病患者新發腎病的風險(相對風險 0.71)以及死亡(相對風險 0.84)。[65]。
口服避孕藥
[編輯]第二次世界大戰之前,許多國家都禁止生育控制,在美國,甚至有關避孕方法的討論有時也會導致依據康斯托克法律而提起訴訟。因此,口服避孕藥的發展歷史,與美國節育運動以及其中激進主義者山額夫人、瑪麗·丹內特、和艾瑪·高德曼三位等的努力息息相關。基於格雷戈里·平卡斯的基礎研究,以及美國藥廠Laboratorios Syntex SA的卡爾·傑拉西和藥廠G.D. Searle&Co.(現為輝瑞公司旗下的品牌)的Frank Colton兩位開發的孕酮合成方法,G.D. Searle&Co.開發出世界第一種口服避孕藥-異炔諾酮(商品名Enovid),這藥物在1960年獲得FDA批准。最初的配方中含有過量的激素,會引起嚴重的副作用。但是到1962年,已有120萬名美國婦女服用過此藥,到1965年,數字已增至650萬。[66][67][68][69]便利形式的臨時避孕藥的出現,導致美國社會習俗發生巨大變化,包括婦女擴大的生活方式選擇,減少婦女依賴男性做的避孕措施,女性晚婚、婚前同居因此增加。[70]
沙利度胺和基福弗-哈里斯修正案
[編輯]在美國,田納西州參議員基福弗於1959年主持的國會聽證會中推動對《聯邦食品、藥品和化妝品法案》的修訂。這項聽證會涉及廣泛的政策議題,包括廣告濫用、引起疑慮的藥物療效、以及產業需要更多的監管。雖然改革動力在長時間的辯論中暫時受到阻撓,但由於當時一項事件,突顯全面監管更有需要,為新法律的通過提供助力。

1960年9月12日,在辛辛那提的藥廠William S. Merrell公司提交沙利度胺(商品名Kevadon)的新藥申請,這項鎮靜劑從1956年開始在歐洲銷售,William S. Merrell是在美國的授權銷售廠商。負責複審這項化合物的FDA醫務人員,弗朗西斯·奧爾德姆·凱爾西認為有關沙利度胺安全性的數據不完整。但公司持續向凱爾西和FDA施加壓力,直到1961年11月這項藥物因與嚴重的先天性障礙有關聯而從德國市場退出。歐洲和其他地區受到沙利度胺的畸形危害的新生兒達到數千名。在未經FDA批准的情況下,William S. Merrell以研究用途為幌子將Kevadon分發給1,000多名醫生。在這項 "研究 ",有超過20,000名美國人接受沙利度胺治療,其中包括624名孕婦,並且約有17名已知受害嬰兒的案例。[71]
沙利度胺事件把遲滯不前的加強藥品監管法案救活,促成基福弗-哈里斯修正案於1962年10月10日成為法律。藥廠此後必須向FDA證明其藥物既有效又安全之後才能上市。FDA取得規範處方藥廣告和建立良好生產規範的權限。法律要求在1938年至1962年之間上市的藥物必須受到管轄。一項由FDA和美國國家科學院的合作研究顯示有近40%的產品並無效果。十年後,對於非處方藥也做了一次相似的詳盡研究。[72]
1970至1980年代
[編輯]他汀類藥物
[編輯]1971年,在日本藥廠第一三共前身之一的三共株式會社工作的生物化學家遠藤章發現黴菌橘青黴產生的一種分子甲伐他汀(ML-236B)是HMG-CoA還原酶的抑制劑,HMG-CoA還原酶是一種人體重要的用來產生膽固醇的酶。在動物試驗時顯示出與臨床試驗一樣,有良好的抑制作用,但是對狗進行的長期研究中發現高劑量時會有毒性作用,因此,甲伐他汀被認為對人類而言毒性太大。甲伐他汀因為會對腫瘤,肌肉退化有不良影響,甚至有時會導致實驗犬的死亡,而未上市。
P. Roy Vagelos是默克藥廠首席科學家(後來擔任首席執行官),他對甲伐他汀很感興趣,並從1975年開始多次前往日本。到1978年,默克藥廠從黴菌土麴黴中分離出「洛伐他汀(mevinolin,MK803)」,這項產品於1987年首度上市,商品名為Mevacor。[73][74][75]
1994年4月,一項由默克藥廠贊助的研究(名為斯堪的納維亞辛伐他汀生存研究發布成果。研究人員對4,444名高膽固醇和心臟病患者進行辛伐他汀的測試。五年後,研究的結論是患者的膽固醇降低35%,因心臟病而亡的機會降低42%,辛伐他汀後來被默克藥廠以Zocor商品名販售。[76]1995年,Zocor和Mevacor兩項藥物為默克藥廠產生的收入超過10億美元。遠藤章獲得2006年的日本國際獎,並於2008年以其"開創性的新型分子研究"而"降低膽固醇",而獲得頒發拉斯克臨床醫學研究獎。 [77][78]
研究與開發
[編輯]藥物發現是潛在藥物被發現或是被設計出的過程。過去,大多數藥物是從傳統藥物中分離出活性成分,或者是意外發現而得。現代的生物技術通常側重理解與疾病狀態或者是病原體有關的代謝途徑,並利用分子生物學或生物化學來操縱這些途徑。傳統上,大量的早期藥物發現是由大學和研究機構所產生。
藥物開發是指找出具有成為藥物潛力的化合物後,確定其適合用作藥物的活動。藥物開發的目的是決定合適的配方和劑量,以及確立安全性。在此領域的研究通常由「體外研究」、「體內研究」、和臨床試驗組合而成。後期開發,因為成本龐大,通常是由大型藥廠來完成。[79]
大型跨國公司通常會作垂直整合,參與廣泛的藥物發現、開發、製造和品質控制、市場行銷、販售、和分銷。而較小的機構通常專注於特定領域,例如找出候選藥物或者開發配方。通常,研究機構與大型藥廠之間會簽訂合作協議,以探索新藥物的潛力。最近,跨國公司越來越依賴受託研究機構來處理藥物開發事項。[80]
創新成本
[編輯]藥物發現和開發,成本非常高昂;在應用於人類的化合物中,在大多數的國家裡最終只有一小部分可得到政府相關機構或委員會的核准,新藥必須獲得核准之後才能銷售。 2010年,有18種NME(新分子實體(New Molecular Entities),以及3種生物藥物獲得美國FDA的核准,總數為21種,低於2009年的26種,也低於2008年的24種,和2006年的22種。自2001年以來,FDA的藥品評估與研究中心平均每年核准22.9種藥物。[81]藥物的核准通常是在臨床前開發和臨床試驗階段會投入大量資金,以及做持續臨床試驗安全性監控的承諾之後才能獲得。在過程中失敗的藥物通常有高昂的成本,卻沒有任何收益。如果把這些失敗藥物的成本列入考慮,開發成功的新藥(新化學實體,NCE)成本估計約為13億美元[82](不包括行銷費用)。但是,Donald Light和Joel Lexchin兩位教授在2012年的報告中指出,幾十年來,新藥的核准率一直相對穩定,平均每年為15至25種。[83]
2009年,整個製藥產業的研究和投資達到創紀錄的653億美元。[84]在1995年至2010年期間,美國的研究和投資約為342億美元,但收入增長得更快(同期收入為2,004億美元)。[83]
貝恩策略顧問發表的一項研究報告說,藥廠的發現、開發、和推出新藥(包括行銷和其他業務費用)的成本(連同預期失敗的藥物)在五年內(到2003年)上升到將近17億美元。[85]據《富比士》雜誌報導,到2010年,每種藥物的開發成本在40億美元至110億美元之間。[86]
其中一些估算還把收入實現之前多年所投入資本的機會成本包括在內(請參閱金錢的時間價值)。由於藥物的發現、開發、和核准需要很長時間,因此這些費用可能累積達到總費用的接近一半。這情況在製藥產業價值鏈中造成的直接後果是,大型跨國藥廠傾向於將與基礎研究相關的風險外包出去,這在某種程度上重塑產業的生態系統,其中生物技術公司扮演著越來越重要的角色,並且整體策略也順應被重新定義。[87]一些就現有活性成分重新配製而被核准的藥物(也稱為產品系列擴充),開發的成本會便宜許多。
產品核准
[編輯]在美國,新藥物必須是既安全又有效,而且要經過FDA核准。核准過程要提出試驗中新藥申請,附有足夠的臨床前數據,以支持進行人體試驗。這項申請被核准後,再進行逐步擴大的三階段人體臨床試驗。第一階段通常用於健康的志願者,研究藥物的毒性。第二階段研究患者的藥物代謝動力學和劑量,第三階段是藥物在預期患者群體的功效,這是一項大型研究。在成功完成第三階段測試後,藥廠提出新藥申請。FDA對數據做審查,如果產品被視為具有正面的效益風險評估結果,就會給予在美國銷售的核准。[88]
即使最大的臨床試驗也不容易預測到罕見副作用的發生率,因此通常也需要做核准後的第四階段監測,上市後監督可密切監控藥物的安全性。在某些情況下,可能僅需要監控特定的患者群組,而有些藥物也會完全從市場中撤出。
FDA會在具有治療等效性評估後批准藥物(或稱為橙皮書(Orange Book ))的網頁中把核准藥品的資訊披露。。[89]
在英國,藥品和醫療衛生產品監管局(MHRA)負責評估以及核准藥物。通常英國和其他歐洲國家/地區的核准會晚於美國。然後是英格蘭和威爾士的國家醫療衛生卓越研究所(NICE)會決定是否以及如何允許國民保健署(NHS)使用(及付費)。《英國國家處方集》是藥劑師和臨床醫生的核心指南。
在許多美國以外的西方國家,在新技術在准用之前需要經過成本效益分析(被稱為'第四障礙')的測試。著重點在於新技術的'功效和價格比較'(例如,每個質量調整壽命年(QALY)的成本)。在英格蘭和威爾士,NICE決定是否以及在何種情況之下讓NHS提供新藥物和新技術,與此同時,蘇格蘭的蘇格蘭醫學聯合會和澳大利亞的藥品福利諮詢委員會也有類似的安排。要獲得核准,產品必須通過成本效益的門檻。治療必須是'物有所值',和對社會產生淨收益。[90]
孤兒藥
[編輯]美國的1983年孤兒藥法案,對某些罕見病有特殊的規定。例如,在美國涉及少於200,000名患者的疾病(在另外一些情況下會涉及更多的人)均受前述《孤兒藥法案》的約束。[91]由於此類藥物在研發所投入資金的回報並不明朗,因此針對製造這種藥物的公司,無論藥物是否受到專利的保護,都可獲得減免稅費,及擁有市場獨占性(為期七年)的獎勵。
全球銷售
[編輯]| 公司名 | 營收 (美金百萬元) |
|---|---|
| 輝瑞 |
45,083 |
| 葛蘭素史克 |
40,156 |
| 賽諾菲 |
38,555 |
| 羅氏 |
27,290 |
| 阿斯利康製藥 |
26,475 |
| 強生公司 |
23,267 |
| 諾華 |
22,576 |
| 默克藥廠 |
20,375 |
| 惠氏 |
16,884 |
| 禮來公司 |
15,691 |
| 百時美施貴寶 |
13,861 |
| 勃林格殷格翰 |
13,860 |
| 安進 |
13,858 |
| 美國雅培 |
12,395 |
| 拜耳 |
10,162 |
| 武田藥品 |
8,716 |
| 先靈葆雅 |
8,561 |
| 梯瓦 |
7,821 |
| 基因泰克 |
7,640 |
| 安斯泰來製藥 |
7,390 |
| 諾和諾德 |
7,087 |
| 第一三共 |
6,790 |
| 百特國際 |
6,461 |
| 默克集團 |
5,643 |
| 衛材 |
4,703 |
在2011年,處方藥在歐洲和北美的銷售增長有所放緩,但全球的支出仍高達9,540億美元。美國占全球藥物市場的三分之一以上,年銷售額為3,400億美元,其次是歐盟和日本。[93]新興市場中例如中國、俄羅斯、韓國、和墨西哥,增長率達到81%,超過前面所述的市場。[94]
在2013年世界最暢銷的十大藥物的銷售額總計為7,560億美元,其中消炎藥阿達木單抗(商品名Humira)是全球銷售額最高的藥物,金額為107億美元。排名第二和第三位的分別是Etanercept(商品名恩博(Enbrel))和英利昔單抗(商品名Remicade)。[95]同年,美國最暢銷的三大藥物是阿立哌唑(商品名Abilify,63億美元)、埃索美拉唑(商品名Nexium,60億美元)、和阿達木單抗(54億美元)。[96]輝瑞公司有史以來最暢銷的藥物阿托伐他汀(商品名Lipitor(立普妥)的平均年收入為130億美元,這項藥品的專利在2011年11月到期,在專利到期前的總銷售額為1,410億美元。
醫療衛生產業資訊服務公司IMS Health所發表對2007年製藥產業預期趨勢的分析說,雖然產業中有些公司的專利到期,但大多數業者的利潤都在增加,新的「重磅炸彈級」藥物(請參考藥品#Blockbuster drug)也即將出現。[97]
專利藥和通用名藥物
[編輯]出於多種考量,一家公司會為藥物本身,或其生產的過程申請專利,有了專利,就擁有通常是20年的排他性權利。[98]但是,只有經過嚴格的研究和測試(平均需要10到15年),公司才能獲得政府核准,再透過市場行銷來販售這項藥物。[99]專利讓擁有者可透過品牌藥的高利潤率來收回研發成本。當藥物的專利保護期滿時,通常會由別家公司開發和銷售仿製藥(通用名藥物)。仿製藥的開發和核准的成本較低,因此可用較低的價格出售。通常,品牌藥的所有者會在專利到期之前自行引入仿製藥,以搶佔仿製藥市場的先機。[100]因此,在1990年代製藥產業的"黃金時代"所推出的產品專利到此時即將到期,而公司又未能開發出足夠的新重磅炸彈級產品來彌補失去的收入,這兩種因素的推動,讓產業內常發生重新組合的現象。[101]
處方藥
[編輯]在美國,從1995年到2006年期間,處方藥的零售金額從720億美元增長250%,達到2,500億美元,而處方藥的平均價格則從30美元增長兩倍多,達到68美元。[102]
市場行銷
[編輯]為藥物在醫療衛生期刊以及眾多主流媒體中做廣告,情況很普遍。在某些國家/地區,尤其是美國,藥廠可以直接對大眾做廣告。藥廠通常會僱用業務人員(通常稱為'藥物代表',或舊稱為'事務人員')直接向醫生和其他醫療衛生提供者推銷產品。在某些國家,尤其是美國,藥廠還僱用製藥產業遊說人員來影響政界人士。在美國,處方藥的銷售受到1987年處方藥販售法的約束。
關於醫事人員
[編輯]由英國醫生及作者Ben Michael Goldacre撰寫的邪惡的製藥業一書,其中也討論到藥物代表的影響、藥廠如何利用捉刀者代為撰寫論文以供學者發表、學術期刊的獨立性問題、藥廠如何為醫生的進修深造提供資金、以及患者團體通常受到產業資助。[103]
直接對消費者做廣告
[編輯]自1980年代以來,直接對消費者推銷處方藥的方法開始變得重要。FDA在1999年制定醫藥產業直接對消費者做廣播廣告指南(FDA Guidance for Industry on Consumer-Directed Broadcast Advertisements)之後,這種廣告方式變成合法。
爭議
[編輯]藥物行銷和遊說
[編輯]圍繞藥物行銷及其影響的爭議不斷增加。透過藥物代表對醫生和其他醫事人員產生影響的指責和發現,包括不斷向醫事人員提供行銷'禮物'和偏頗的資訊、 [104]盛行在期刊和會議上的廣告、資助獨立的醫療組織和健康促進運動、對醫生和政界人士遊說(高於美國其他任何行業的遊說活動[105])、贊助醫學院校或護士訓練、贊助醫事人員進修深造、影響課程教材、 [106]並在醫療諮詢委員會聘用醫師作為有償顧問。
一些倡導團體,例如「沒白吃的午餐 」和「登記所有試驗和公開結果」,在市場推廣活動對醫生的影響方面有所批評,他們說,即使其他藥物可能對患者會更便宜或更有利,醫生也會開立推銷中的藥物。[107]
相關的指控還有藥廠的行為像販售疾病[108](過度用藥),以擴大藥物市場。2006年,關於這項主題的首次會議在澳大利亞舉行。[109]2009年,由政府資助的非營利機構國家處方服務局謹慎用藥啟動"查證據-分辨炒作"計劃[110],向一般科醫師提供有關對藥物作獨立分析的知識。[111]
根據綜合分析的結果顯示,藥廠贊助的精神病學研究,呈陽性結果的可能性會高出好幾倍,而且如果藥廠員工涉入其中,則呈現陽性結果的程度甚至會更高。[112][113][114]藥廠的影響力還擴展到在醫學院學習的醫生和護士,這情況正被改正中。
有人會說《精神疾病診斷與統計手冊》(DSM)的設計和擴展,代表藥廠對精神病學的影響,它推動人性的用藥化,或者就是藥廠在"販售疾病"。[115],由於選擇和定義「DSM手冊有關精神疾病部分」的作者裡面有相當多人與製藥產業有過,或是曾經有過財務關係,這可能是導致正面利益衝突可能性升高的部分原因。[116][117]
在美國,從2013年開始,根據《醫師財務透明度報告》(《醫生付款陽光法案》中的條款),聯邦醫療保險和聯邦醫療補助服務中心(CMS)必須從相關的製造商和團購組織收集資訊,以便把它們與醫生和醫院之間的財務關係列入報告,然後在CMS的網站上公開。期望醫生與製藥產業之間的關係因此變得完全透明。[118]
專注在選舉和公共政策的遊說和金錢事項的非營利組織Center for Responsive Politics發布的一份報告說,在2017年有1,100多名遊說者以某種身份為製藥產業工作。2017年第一季度,健康產品和製藥產業在美國國會的遊說人員身上花費7,800萬美元。[119]
藥物定價
[編輯]有人爭辯,藥物的價格正逐漸成為醫療系統中一項重大的挑戰。[120]
監管問題
[編輯]邪惡的製藥業一書的作者Ben Goldacre認為,監管機構(例如英國的藥品和醫療衛生產品監管局(MHRA),或美國的FDA),由於監管機構與產業之間人員的旋轉門問題,以及監管機構與產業的員工之間建立起友誼的緣故,[121]反而會促進藥廠的利益,而非公眾的利益。他說,監管機構不要求新藥比較現有藥物有改善,甚至不會要求新藥要特別有效。[121]
其他人則認為,過度監管會把治療創新給壓抑,而監管機構當前要求的臨床試驗所產生的成本,對充分利用新的遺傳以及生物學知識做人類疾病治療會有妨礙。總統辦公室的科學技術顧問委員會在2012年的一份報告提出幾項重要建議,以減輕新藥開發的監管負擔,其中包括:1)擴大使用FDA加速核准程序; 2)為用在少數群體中的藥物建立快速核准途徑; 3)為評估新的適應性藥物核准程序,實施試行計劃,以研究可行性。[122]
藥物詐欺
[編輯]藥物詐欺涉及欺騙,為藥廠帶來經濟利益。受到影響的有個人、公眾、以及私人保險公司。製藥產業中幾種特有的詐欺模式[123]包括:違反良好生產規範(GMP)、市場推廣標籤外功效(請參考標籤外使用)、最佳價格詐欺(藥廠提供不實最低價格,以降低給予聯邦醫療補助(Medicaid)較低的回扣)[124]、醫事人員進修深造(CME)欺詐[125]、醫療補助價格報告(藥房出售藥品給消費者,向Medicaid申請報銷,然後從藥廠或者批發商獲得回扣)[126]、和調製合成藥物(藥房自行大量調製合成藥物,不當跨入製藥產業行為)[125]。[127]對於這類詐欺,美國在2010財務年度透過《虛假申報法》追回25億美元。這類案件例子包括葛蘭素史克30億美元的和解、輝瑞23億美元的和解、以及默克藥廠6.5億美元的和解。詐欺造成的損害可以通過《虛假申報法》來追討,最常見的是根據《分享的訴訟》的規定,該規定會對"吹哨人"或告發人提供獎勵。[128]
出售抗精神病藥的每家主要藥廠-百時美施貴寶、禮來公司、輝瑞、阿斯利康、和強生公司-都曾因《虛假申報法》而繳納數億美元和解費,或接受詐欺的調查。在被提起非法行銷的訴訟案件,其中兩個曾在當年創下有史以來最大的刑事罰款記錄。其中一個涉及禮來的抗精神病藥奧氮平(商品名Zyprexa),另一個涉及非類固醇消炎藥Valdecoxib(商品名Bextra)。在Bextra案中,政府還指控輝瑞公司非法行銷另一種抗精神病藥齊拉西酮(商品名Geodon);輝瑞公司以3.01億美元為齊拉西酮案作和解,但不承認有任何不當行為。[129]
2012年7月2日,葛蘭素史克對刑事指控表示認罪,並同意以30億美元為這項當時美國史上最大的醫療詐欺案作和解,也是當時一家藥廠支付的最大一筆金額。[130]該和解與公司非法行銷處方藥、未能報告安全數據[131]、賄賂醫生、以及倡導藥物未經許可的用途。而藥物包括帕羅西汀(商品名Paxil)、安非他酮(商品名Wellbutrin)、丙酸氟替卡松/沙美特羅(商品名Advair)、拉莫三嗪(商品名Lamictal)、和昂丹司瓊(商品名Zofran),則涉入標籤外使用(未核准的用途)。前面的藥物加上舒馬曲坦(商品名Imitrex)、阿洛司瓊(商品名Lotronex)、丙酸氟替卡松(商品名Flovent)、和伐昔洛韋(商品名Valtrex)等,都涉入不當回扣。[132][133][134]
以下是1991年至2012年間四個最大的藥廠和解案,按和解金額規模排序。在過去的二十年中,針對製藥產業的法律訴訟原因各有不同,包括聯邦醫療保險和聯邦醫療補助詐欺、標籤外行銷、以及不完備的生產方式。[135][136]
| 公司名稱 | 和解金額 | 罪名 | 年份 | 產品 | 根據法律 |
|---|---|---|---|---|---|
| 葛蘭素史克[137] | 30億美元 | 標籤外行銷/ 未提出安全數據 |
2012 | 羅格列酮/安非他酮/帕羅西汀 | 虛假申報法/聯邦食品、藥品和化妝品法案 |
| 輝瑞[138] | 23億美元 | 標籤外行銷/不法回扣 | 2009 | Valdecoxib/齊拉西酮/ 利奈唑胺/普瑞巴林 |
虛假申報法/聯邦食品、藥品和化妝品法案 |
| 美國雅培[139] | 15億美元 | 標籤外行銷 | 2012 | 丙戊酸 | 虛假申報法/聯邦食品、藥品和化妝品法案 |
| 禮來公司[140] | 14億美元 | 標籤外行銷 | 2009 | 奧氮平 | 虛假申報法/聯邦食品、藥品和化妝品法案 |
臨床試驗
[編輯]由於在一些藥廠所進行或資助的臨床試驗中,持續的發現到正面的報導僅會給予它們偏好的藥物,因此引起獨立團體和政府機構對這個產業的嚴重關切。[141]
針對藥廠贊助的研究有不利數據但不報導的特定情況,美國藥學研究與製造商協會發布新指南,敦促公司對所有發現都必須報告,並限制藥廠對於研究人員有財務牽涉。[142]美國國會通過一項法案,要求在國家衛生院的網站Clinicaltrials.gov上把臨床試驗第二期和第三期的贊助者註冊登記(請參考臨床試驗期別)。[143]
非藥廠直接僱用的研究人員經常會期望藥廠給予獎金,而公司經常希望研究人員讓它們的產品看起來更有利。研究人員會得到製藥公司的獎勵,例如為其會議/座談會提供財務支持。實際上,學術研究人員的演講稿,甚至是在期刊上發表的文章,可能是藥廠在後"代為捉刀"而產生。[144]
非營利機構ProPublica所做的一項調查發現,自2009年以來,藥廠至少為21位醫生提供演講和諮詢服務的報酬,金額超過50萬美元,其中收費最高的一半人員是在精神醫學研究的領域,美國為類似服務而支付給醫生的總額約為20億美元。阿斯利康製藥、強生公司、和禮來在聯邦和解協議中支付數十億美元的和解費,而受到的指控是他們付錢給醫生,用來推廣藥物在未經許可的用途上。此後,一些著名的醫學院加強管制教師接受藥廠金錢饋贈的規定。[145]
與前述觀點相反,2015年5月在《新英格蘭醫學雜誌》上發表的一篇文章和相關社論,強調製藥產業與醫師之間的互動對於開發新療法的重要性,並指出,對產業不法行為的道義憤怒已導致許多人不合理地過分強調經濟利益衝突所造成的問題。文章指出,主要的醫療衛生組織,例如美國國家衛生院所屬的國家推進轉化科學中心、總統辦公室的科學技術顧問委員會(Council of Advisors on Science and Technology)、世界經濟論壇、比爾及梅琳達·蓋茨基金會、惠康基金會、和FDA都鼓勵醫生與產業之間加強互動,以為患者帶來更大的利益。[146][147]
2020年對冠狀病毒疫情反應
[編輯]國際組織無國界醫生警告說,藥物、檢驗、和疫苗的高價和壟斷會延長這次2019冠狀病毒病疫情的流行期間,更多生命受到摧毀。他們敦促各國政府仿效如加拿大、智利、厄瓜多爾、德國、和以色列所做的,有必要就該使用強制許可的措施,以防止藥廠獲取暴利的行為。[148]
2020年2月20日,有46名美國立法者呼籲美國政府在動用來自人民繳稅的公共資金,提供給任何冠狀病毒疫苗和治療做開發和生產時,不要給予壟斷權,以避免讓私人藥廠擁有完全控制價格的能力。[149]

2月26日,美國衛生與公共服務部部長(前藥廠首席執行官)亞歷克斯·阿扎在眾議院能源和商業委員會上作證。阿扎在會議上一再拒絕說所有美國人都可受到2019冠狀病毒疫苗接種或治療,而不僅是有經濟能力者才能享有,詢問的議員批評他的立場。幾個小時後,據說對這位部長的處理能力持懷疑態度的川普總統突然將處理這次瘟疫的責任轉移給副總統邁克·彭斯。總統隨後對新聞界解釋,阿扎仍將繼續擔任衛生和公共服務部部長;報導說,川普總統在危機期間為保住顏面而未將他解職。[150][151]
3月2日,眾議員簡·夏科夫斯基寫信給阿扎,說:「您必須了解,如果用納稅人的錢來開發2019冠狀病毒(COVID-19)疫苗,眾議院將無法接受隨後把生產和銷售疫苗的專有許可權移交給藥廠,不對價格或接種條件有所規定,而讓這家公司用任何價格出售給社會大眾,因為事實上開發的經費是由社會大眾所提供。」 [152][153]

2020年3月6日由川普總統簽署的《2020年冠狀病毒防備和應對補充撥款法案》,法案最初允許美國政府在價格過高的情況下可採取強制許可。但經過藥廠遊說之後,這條款被刪除,而另外增加一條,美國政府不得因為可負擔性的問題而採取行動,導致疫苗或者可用性受到延緩。對於這項法案是否會幫助或是阻礙到可負擔性,觀察者之間的意見並不一致。[154]
再生元製藥與美國政府的生物醫學高級研究與開發局之間的協議,由政府預備資助這家公司開發和生產COVID-19治療藥物費用的80%,藥廠保留定價和控制生產的權利。這筆交易在《紐約時報》上受到批評。對於美國製藥產業的常規開發業務而言,這種交易並非罕見。[149]
美國藥廠吉利德科學於2020年3月23日向FDA申請,而為瑞德西韋取得孤兒藥的資格。孤兒藥規定的目的是把合法壟斷權加強以及延長,用來鼓勵藥廠開發藥物,提供給罹患特殊疾病的小眾美國人(單一病症患者不到200,000人),同時給予免除稅費的優惠。[155][156]瑞德西韋是一種治療COVID-19的候選藥物;瑞德西韋在獲得這一資格的時候,只有不到200,000的美國人受到COVID-19的侵害,但是隨著大流行的產生,染病人數迅速超過200,000人的門檻。[155][156]瑞德西韋的開發,獲得美國政府的資助,超過7,900萬美元[156]。吉利德科學於2020年5月宣布,它將免費向聯邦政府提供940,000劑藥物。[157]面對公眾的強烈反應,吉利德科學於3月25日把藥物的"孤兒藥"地位放棄。[158]吉利德科學在70多個國家/地區擁有20年的專利。[148]2020年5月,該公司進一步宣布,正在與數家通用名藥物公司進行討論,以提供為發展中國家的生產權利,並與聯合國支持的藥品專利池進行討論,以提供更廣泛的通用名藥物查詢和資料取得。 [159]
美國診斷測試儀器製造商Cepheid Inc獲得FDA緊急使用授權,准予使用名為Xpert Xpress SARS-CoV-2的測試COVID-19儀器。使用的機器與通常用於測試結核病和人類免疫缺陷病毒(HIV)以及其他疾病的機器相同,可在45分鐘內得出結果,比其他測試更快。Cepheid宣布,他們為發展中國家的測試,每次收取19.80美元的費用。無國界醫生說,在每天生活費不足兩美元的國家之中,人們無力負擔這種價格。他們估計,Cepheid的成本只有3美元,所以這樣的收費建議是牟取暴利,因此要求只收取5美元,賺取較為適度的利潤。[148]美國倡議組織治療行動小組(TAG)稱這項測試的開發,購買和全球部署都是通過公共資金完成,對於無國界醫生降價的建議予以附議,而Cepeid在2019年利潤是30億美元。TAG還啟動"是只花費5美元的時候了"的廣告系列。[160]C型肝炎病毒(與Convid-19類似,是另一種核糖核酸病毒)的測試,成本從50美分(血清中抗體測試,需時五分鐘)到5美元(與Cepheid的複雜基因組測試類似)。這類廉價的廣泛測試對消除埃及的C型肝炎有舉足輕重的地位,[161][162][162],類似的大規模測試技術已成功在義大利的沃鎮運作,用於對抗COVID-19。[163]
發展中國家
[編輯]專利
[編輯]藥物專利受到發展中國家的批評,因為專利被認為會降低獲得既有藥物的機會。[164]在藥物的專利和普遍獲得之間要達到協調,需要有有效的國際價格分歧政策。此外,根據世界貿易組織的與貿易有關的知識產權協定(TRIPS),各國必須允許藥物獲得專利。在2001年,WTO通過《杜哈TRIPS協定與公共衛生宣言》,宣言指出,應以公共衛生為目標來理解TRIPS協議,並允許一些規避藥物壟斷的方法:甚至在專利到期之前,利用強制許可或平行進口貨品來達到目的。[165]
2001年3月,有40家跨國製藥公司因為南非的《1997年藥品法》而對該國提起訴訟,南非的這項法律允許仿製用於治療HIV的抗反轉錄病毒藥物 (ARV),而這些藥物已有專利保護。[166]在南非,愛滋病一直是一種流行病,當時患者每年需要的ARV治療費用在10,000至15,000美元之間。對於大多數南非公民來說,他們無力負擔,因此南非政府承諾提供ARV,而收費又接近人們所能承受。為此,他們得無視藥品專利而在國內生產仿製藥物(經過強制許可),或者從國外進口。在國際社會發動支持公共衛生權利的抗議活動(包括無國界醫生組織收集到的25萬個簽名)之後,幾個已開發國家的政府(包括荷蘭、德國、法國、和後來的美國)支持南非政府,這個訴訟案在當年4月被撤銷。[167]
2016年,葛蘭素史克(當時全球第六大製藥公司)宣布放棄在貧窮國家的專利,以允許獨立的公司在這些地區生產和銷售它們的藥物,公眾的取得途徑得以擴大。[168]葛蘭素史克發布一份名單,列出不再運用專利保護的50個國家,全球受惠於這種措施的人數達到10億。
慈善計劃
[編輯]2011年,前20大公司的慈善捐贈中有4個,前30大公司慈善捐贈中有8個,都是來自製藥公司。公司慈善捐贈的大部分(截至2012年為69%)是透過非現金的方式進行,其中非現金的大部分是來自製藥公司。 [169]
製藥公司的慈善計劃,以及藥物發現與開發工的作包括:
- "默克藥廠的禮物",其中有捐贈給非洲價值數十億美元的河盲症藥物[170]
- "輝瑞的禮物",在南非提供免費/打折的氟康唑和其他抗愛滋病藥物[171]
- 葛蘭素史克承諾向WHO提供免費的阿苯達唑片劑,直至淋巴絲蟲病在世界上絕跡為止。
- 2006年,諾華承諾在全球實施7.55億美元的企業公民[172]倡議,特別是通過其「獲得藥品」項目來改善發展中國家對藥品的獲取,包括捐贈藥物(給受到麻風病、結核病、和瘧疾影響的患者), 伊馬替尼(商品名Glivec,治療癌症口服藥)援助計劃,以及對有緊急醫療需要的人道主義組織提供援助。[173]
參見
[編輯]參考文獻
[編輯]- ^ McGuire, John L.; Hasskarl, Horst; Bode, Gerd; Klingmann, Ingrid; Zahn, Manuel. Ullmann's Encyclopedia of Industrial Chemistry. 2007. ISBN 978-3527306732. doi:10.1002/14356007.a19_273.pub2.
- ^ Bozenhardt, Erich H.; Bozenhardt, Herman F. Are You Asking Too Much From Your Filler?. Pharmaceutical Online (Guest column) (VertMarkets). 2018-10-18 [2018-10-30]. (原始內容存檔於2020-11-17).
The core mission of the pharmaceutical industry is to manufacture products for patients to cure them, vaccinate them, or alleviate a symptom, often by manufacturing a liquid injectable or an oral solid, among other therapies.
- ^ Multinational corporations including Merck, Hoffman-La Roche, Burroughs-Wellcome (now part of Glaxo Smith Kline), Abbott Laboratories, Eli Lilly and Upjohn (now part of Pfizer) began as local apothecary shops in the mid-1800s.
- ^ Top Pharmaceuticals: Introduction: EMERGENCE OF PHARMACEUTICAL SCIENCE AND INDUSTRY: 1870-1930. (原始內容存檔於2018-11-10).
- ^ Sneader, Walter. Drug Discovery: A History. John Wiley & Sons. 2005-10-31: 155–156 [2020-11-20]. ISBN 978-0-470-01552-0. (原始內容存檔於2020-09-13).
- ^ 6.0 6.1 Rasmussen, Nicolas. Making the First Anti-Depressant: Amphetamine in American Medicine, 1929-1950. J Hist Med Allied Sci. 2006, 61 (3): 288–323. PMID 16492800. S2CID 24974454. doi:10.1093/jhmas/jrj039.
- ^ Medicines and men: Burroughs, Wellcome & Co, and the British drug industry before the Second World War. Royal Society of Medicine Press. 2002 Aug [2020-10-18].
- ^ New and Nonofficial Remedies, 1937: Containing Description of the Articles Which Stand Accepted by the Council on Pharmacy and Chemistry of the ... on January 1, 1937. FDA. 1937-01-01 [2020-10-26].
- ^ Yasiry Z, Shorvon SD. How phenobarbital revolutionized epilepsy therapy: the story of phenobarbital therapy in epilepsy in the last 100 years. Epilepsia. December 2012,. 53 Suppl 8: 26–39. PMID 23205960. doi:10.1111/epi.12026.
- ^ López-Muñoz F, Ucha-Udabe R, Alamo C. The history of barbiturates a century after their clinical introduction. Neuropsychiatr Dis Treat. December 2005, 1 (4): 329–43. PMC 2424120
 . PMID 18568113.
. PMID 18568113.
- ^ World Health Organization Model List of Essential Medicines (PDF). WHO. [2021-03-23]. (原始內容存檔 (PDF)於2021-04-05).
- ^ Drug Abuse Control Amendments of 1965. NEJM. 1965-11-25, 273 (22): 1222–1223. doi:10.1056/NEJM196511252732213.
Officers of the Food and Drug Administration, aware of the seriousness of the problem, estimate that approximately half the 9,000,000,000 barbiturate and amphetamine capsules and tablets manufactured annually in this country are diverted to illegal use. The profits to be gained from the illegal sale of these drugs have proved an attraction to organized crime, for amphetamine can be purchased at wholesale for less than $1 per 1000 capsules, but when sold on the illegal market, it brings $30 to $50 per 1000 and when retailed to the individual buyer, a tablet may bring as much as 10 to 25 cents.
- ^ Sedative-Hypnotic Drugs — The Barbiturates — I. NEJM. 1956, 255 (24): 1150–1151. doi:10.1056/NEJM195612132552409.
THE barbiturates, introduced into medicine by E. Fischer and J. von Mering1 in 1903, are certainly among the most widely used and abused drugs in medicine. Approximately 400 tons of these agents are manufactured each year; this is enough to put approximately 9,000,000 people to sleep each night for that period if each were given a 0.1-gm. dose
- ^ Rosenfeld L. Insulin: discovery and controversy. Clin. Chem. December 2002, 48 (12): 2270–88. PMID 12446492. doi:10.1093/clinchem/48.12.2270.
- ^ 15.0 15.1 (PDF) https://www.cdc.gov/nchs/data/nvsr/nvsr47/nvs47_28.pdf. (原始內容存檔 (PDF)於2020-10-25). 缺少或
|title=為空 (幫助) - ^ cdc.gov (PDF). (原始內容存檔 (PDF)於2020-12-13).
- ^ Sepkowitz KA. One hundred years of Salvarsan. N. Engl. J. Med. July 2011, 365 (4): 291–3. PMID 21793743. doi:10.1056/NEJMp1105345.
- ^ Williams, KJ. The introduction of 'chemotherapy' using arsphenamine – the first magic bullet. Journal of the Royal Society of Medicine. 2009-08-01, 102 (8): 343–348. ISSN 0141-0768. PMC 2726818
 . PMID 19679737. doi:10.1258/jrsm.2009.09k036.
. PMID 19679737. doi:10.1258/jrsm.2009.09k036.
- ^ Aminov RI. A brief history of the antibiotic era: lessons learned and challenges for the future. Front Microbiol. 2010, 1: 134. PMC 3109405
 . PMID 21687759. doi:10.3389/fmicb.2010.00134.
. PMID 21687759. doi:10.3389/fmicb.2010.00134.
- ^ Hager, Thomas. The demon under the microscope : from battlefield hospitals to Nazi labs, one doctor's heroic search for the world's first miracle drug 1st. New York: Harmony Books. 2006. ISBN 978-1-4000-8213-1.
- ^ Nobel Prize Facts. nobelprize.org. [2016-05-19]. (原始內容存檔於2018-08-15).
- ^ 22.0 22.1 Cutler, David; Meara, Ellen. Changes in the Age Distribution of Mortality Over the 20th Century (PDF). NBER Working Paper No. 8556. October 2001 [2020-11-20]. doi:10.3386/w8556. (原始內容存檔 (PDF)於2020-07-30).
- ^ 23.0 23.1 Klein, Herbert. A Population History of the United States. Cambridge University Press. 2012: 167.
- ^ Parascandola, John. The History of antibiotics: a symposium. American Institute of the History of Pharmacy No. 5. 1980. ISBN 978-0-931292-08-8.
- ^ Diphtheria — Timelines — History of Vaccines. (原始內容存檔於2016-05-14).
- ^ Ii, Thomas H. Maugh. Maurice R. Hilleman, 85; Scientist Developed Many Vaccines That Saved Millions of Lives - Los Angeles Times. Los Angeles Times. 2005-04-13. (原始內容存檔於2015-04-05).
- ^ Significant Dates in U.S. Food and Drug Law History. (原始內容存檔於2013-03-06).
- ^ FDAReview.org, a project of The Independent Institute. (原始內容存檔於2015-12-02).
- ^ Sulfanilamide Disaster. (原始內容存檔於2017-07-22).
- ^ FDA History - Part II. (原始內容存檔於2018-01-01).
- ^ Part II: 1938, Food, Drug, Cosmetic Act. FDA. [2020-10-26]. (原始內容存檔於2020-12-07).
- ^ Zaffiri L, Gardner J, Toledo-Pereyra LH. History of antibiotics. From salvarsan to cephalosporins. J Invest Surg. April 2012, 25 (2): 67–77. PMID 22439833. S2CID 30538825. doi:10.3109/08941939.2012.664099.
- ^ Hamilton-Miller JM. Development of the semi-synthetic penicillins and cephalosporins. Int. J. Antimicrob. Agents. March 2008, 31 (3): 189–92. PMID 18248798. doi:10.1016/j.ijantimicag.2007.11.010.
- ^ Abraham EP. Cephalosporins 1945-1986. Drugs. 1987,. 34 Suppl 2 (Supplement 2): 1–14. PMID 3319494. S2CID 12014890. doi:10.2165/00003495-198700342-00003.
- ^ 35.0 35.1 Kingston W. Streptomycin, Schatz v. Waksman, and the balance of credit for discovery. J Hist Med Allied Sci. July 2004, 59 (3): 441–62. PMID 15270337. S2CID 27465970. doi:10.1093/jhmas/jrh091.
- ^ Nelson ML, Levy SB. The history of the tetracyclines. Ann. N. Y. Acad. Sci. December 2011, 1241 (1): 17–32. Bibcode:2011NYASA1241...17N. PMID 22191524. doi:10.1111/j.1749-6632.2011.06354.x.
- ^ ERYTHROMYCIN. Br Med J. November 1952, 2 (4793): 1085–6. PMC 2022076
 . PMID 12987755. doi:10.1136/bmj.2.4793.1085.
. PMID 12987755. doi:10.1136/bmj.2.4793.1085.
- ^ Anderson, Rosaleen. Antibacterial agents chemistry, mode of action, mechanisms of resistance, and clinical applications. Oxford: WiBlackwell. 2012. ISBN 9780470972458.
- ^ Federal Trade Commission Report of Antibiotics Manufacture, June 1958 (Washington D.C., Government Printing Office, 1958) pages 98-120
- ^ Federal Trade Commission Report of Antibiotics Manufacture, June 1958 (Washington D.C., Government Printing Office, 1958) page 277
- ^ SWEET BH, HILLEMAN MR. The vacuolating virus, S.V. 40. Proc. Soc. Exp. Biol. Med. November 1960, 105 (2): 420–7. PMID 13774265. S2CID 38744505. doi:10.3181/00379727-105-26128.
- ^ Shah K, Nathanson N. Human exposure to SV40: review and comment. Am. J. Epidemiol. January 1976, 103 (1): 1–12. PMID 174424. doi:10.1093/oxfordjournals.aje.a112197.
- ^ Studies:No Evidence That SV40 is Related to Cancer - National Cancer Institute. [2020-11-20]. (原始內容存檔於2014-10-28).
|url-status=和|dead-url=只需其一 (幫助) - ^ History of Vaccines — A Vaccine History Project of The College of Physicians of Philadelphia. (原始內容存檔於2020-12-06).
- ^ Prevention of Measles, Rubella, Congenital Rubella Syndrome, and Mumps, 2013. (原始內容存檔於2014-11-10).
- ^ Bloch AB, Orenstein WA, Stetler HC, et al. Health impact of measles vaccination in the United States. Pediatrics. 1985, 76 (4): 524–32. PMID 3931045.
- ^ Insull W. The pathology of atherosclerosis: plaque development and plaque responses to medical treatment. The American Journal of Medicine. January 2009, 122 (1 Suppl): S3–S14. PMID 19110086. doi:10.1016/j.amjmed.2008.10.013.
- ^ Gaddam KK, Verma A, Thompson M, Amin R, Ventura H. Hypertension and cardiac failure in its various forms. The Medical Clinics of North America. May 2009, 93 (3): 665–80 [2009-06-20]. PMID 19427498. doi:10.1016/j.mcna.2009.02.005. (原始內容存檔於2020-03-28).
- ^ Agabiti-Rosei E. From macro- to microcirculation: benefits in hypertension and diabetes. Journal of Hypertension. September 2008, 26 (Suppl 3): S15–21. PMID 19363848. doi:10.1097/01.hjh.0000334602.71005.52.
- ^ Murphy BP, Stanton T, Dunn FG. Hypertension and myocardial ischemia. The Medical Clinics of North America. May 2009, 93 (3): 681–95 [2009-06-20]. PMID 19427499. doi:10.1016/j.mcna.2009.02.003. (原始內容存檔於2020-03-28).
- ^ White WB. Defining the problem of treating the patient with hypertension and arthritis pain. The American Journal of Medicine. May 2009, 122 (5 Suppl): S3–9. PMID 19393824. doi:10.1016/j.amjmed.2009.03.002.
- ^ Truong LD, Shen SS, Park MH, Krishnan B. Diagnosing nonneoplastic lesions in nephrectomy specimens. Archives of Pathology & Laboratory Medicine. February 2009, 133 (2): 189–200 [2009-06-20]. PMID 19195963. doi:10.1043/1543-2165-133.2.189 (不活躍 2020-08-23).
- ^ Tracy RE, White S. A method for quantifying adrenocortical nodular hyperplasia at autopsy: some use of the method in illuminating hypertension and atherosclerosis. Annals of Diagnostic Pathology. February 2002, 6 (1): 20–9. PMID 11842376. doi:10.1053/adpa.2002.30606.
- ^ Aronow WS. Hypertension and the older diabetic. Clinics in Geriatric Medicine. August 2008, 24 (3): 489–501, vi–vii [2009-06-20]. PMID 18672184. doi:10.1016/j.cger.2008.03.001. (原始內容存檔於2020-03-28).
- ^ Gardner AW, Afaq A. Management of Lower Extremity Peripheral Arterial Disease. Journal of Cardiopulmonary Rehabilitation and Prevention. 2008, 28 (6): 349–57. PMC 2743684
 . PMID 19008688. doi:10.1097/HCR.0b013e31818c3b96.
. PMID 19008688. doi:10.1097/HCR.0b013e31818c3b96.
- ^ Novo S, Lunetta M, Evola S, Novo G. Role of ARBs in the blood hypertension therapy and prevention of cardiovascular events. Current Drug Targets. January 2009, 10 (1): 20–5 [2009-06-20]. PMID 19149532. doi:10.2174/138945009787122897. (原始內容存檔於2020-03-28).
|url-status=和|dead-url=只需其一 (幫助) - ^ Craig WM. Surgical Treatment of Hypertension. Br Med J. 1939, 2 (4120): 1215–9. PMC 2178707
 . PMID 20782854. doi:10.1136/bmj.2.4120.1215.
. PMID 20782854. doi:10.1136/bmj.2.4120.1215.
- ^ Sneader, Walter. Drug Discovery. A History. New York: Wiley. 2005: 371.
- ^ Beyer KH. Chlorothiazide. How the thiazides evolved as antihypertensive therapy. Hypertension. 1993, 22 (3): 388–91. PMID 8349332. doi:10.1161/01.hyp.22.3.388.
- ^ BORHANI NO, HECHTER HH. Recent Changes in CVR Disease Mortality in California: An Epidemiologic Appraisal. Public Health Rep. 1964, 79 (2): 147–60. JSTOR 4592077. PMC 1915335
 . PMID 14119789. doi:10.2307/4592077.
. PMID 14119789. doi:10.2307/4592077.
- ^ The Lasker Foundation - Awards. (原始內容存檔於2015-12-23).
- ^ Wright, James M.; Musini, Vijaya M.; Gill, Rupam. First-line drugs for hypertension. The Cochrane Database of Systematic Reviews. 2018-04-18, 4: CD001841. ISSN 1469-493X. PMC 6513559
 . PMID 29667175. doi:10.1002/14651858.CD001841.pub3.
. PMID 29667175. doi:10.1002/14651858.CD001841.pub3.
- ^ Stason WB, Cannon PJ, Heinemann HO, Laragh JH. Furosemide. A clinical evaluation of its diuretic action. Circulation. November 1966, 34 (5): 910–20. PMID 5332332. S2CID 886870. doi:10.1161/01.cir.34.5.910.
- ^ Black JW, Crowther AF, Shanks RG, Smith LH, Dornhorst AC. A new adrenergic betareceptor antagonist. The Lancet. 1964, 283 (7342): 1080–1081. PMID 14132613. doi:10.1016/S0140-6736(64)91275-9.
- ^ Lv J, Perkovic V, Foote CV, Craig ME, Craig JC, Strippoli GF. Antihypertensive agents for preventing diabetic kidney disease. Cochrane Database Syst Rev. 2012, 12: CD004136. PMID 23235603. doi:10.1002/14651858.CD004136.pub3.
- ^ A brief history of the birth control pill - The pill timeline | Need to Know | PBS. 2010-05-07. (原始內容存檔於2020-11-11).
- ^ Why the Oral Contraceptive Is Just Known as "The Pill". smithsonianmag.com. (原始內容存檔於2020-11-09).
- ^ BBC News | HEALTH | A short history of the pill. (原始內容存檔於2020-11-13).
- ^ FDA's Approval of the First Oral Contraceptive, Enovid. (原始內容存檔於2017-07-23).
- ^ Cafe, Rebecca. BBC News - How the contraceptive pill changed Britain. BBC News. 2011-12-04. (原始內容存檔於2019-06-16).
- ^ The History Of Drug Regulation In the United States, Centennial Edition 2006. FDA. [2020-10-30]. (原始內容存檔於2019-12-14).
- ^ Brochure: The History of Drug Regulation in the United States. (原始內容存檔於2017-07-23).
- ^ Tobert, Jonathan A. Lovastatin and beyond: the history of the HMG-CoA reductase inhibitors. Nature Reviews Drug Discovery. July 2003, 2 (7): 517–526. ISSN 1474-1776. PMID 12815379. S2CID 3344720. doi:10.1038/nrd1112.
- ^ Endo A. The discovery and development of HMG-CoA reductase inhibitors. Journal of Lipid Research. 1992-11-01, 33 (11): 1569–82 [2020-11-20]. PMID 1464741. (原始內容存檔於2010-02-14).
- ^ Endo, Akira. The origin of the statins. International Congress Series. 2004, 1262: 3–8. doi:10.1016/j.ics.2003.12.099.
- ^ Scandinaviansimvastatinsurvival. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet. November 1994, 344 (8934): 1383–9. PMID 7968073. S2CID 5965882. doi:10.1016/S0140-6736(94)90566-5.
- ^ National Inventors Hall of Fame Honors 2012 Inductees. PRNewswire. [2014-05-11]. (原始內容存檔於2019-04-26).
- ^ How One Scientist Intrigued by Molds Found First Statin. Wall Street Journal. [2014-05-11]. (原始內容存檔於2022-02-24).
- ^ Annual Impact Report. Tufts Center for the Study of Drug Development. [2020-11-20]. (原始內容存檔於2020-04-07).
- ^ Outsourcing-Pharma.com. Pfizer teams with Parexel and Icon in CRO sector's latest strategic deals. Outsourcing-Pharma.com. [2020-11-20]. (原始內容存檔於2020-05-08).
- ^ How Many New Drugs Did FDA Approve Last Year?. pharmalot.com. [2011-04-23]. (原始內容存檔於2011-05-08).
|url-status=和|dead-url=只需其一 (幫助) - ^ Research. [2006-11-24]. (原始內容存檔於2011-07-20).
|url-status=和|dead-url=只需其一 (幫助) - ^ 83.0 83.1 Perry, Susan. Donald Light and Joel Lexchin in BMJ 2012;345:e4348, quoted in: Big Pharma's claim of an 'innovation crisis' is a myth, BMJ authors say. MinnPost. 2012-08-08 [2012-08-08]. (原始內容存檔於2020-07-30).
- ^ About PhRMA - PhRMA. [2011-04-23]. (原始內容存檔於2013-01-04).
|url-status=和|dead-url=只需其一 (幫助) - ^ Has the Pharmaceutical Blockbuster Model Gone Bust?. bain.com. [2016-05-19]. (原始內容存檔於2018-05-04).
- ^ Harper, Matthew. The Truly Staggering Cost Of Inventing New Drugs. Forbes. 2012-02-10 [2020-11-20]. (原始內容存檔於2020-12-09).
- ^ IMS Health. Are European biotechnology companies sufficiently protected?. Portal of Competitive Intelligence. 2015-06-18 [2015-06-27]. (原始內容存檔於2015-06-30).
|url-status=和|dead-url=只需其一 (幫助) - ^ Liberti L, McAuslane JN, Walker S. Standardizing the Benefit-Risk Assessment of New Medicines: Practical Applications of Frameworks for the Pharmaceutical Healthcare Professional. Pharm Med. 2011, 25 (3): 139–46 [2011-10-18]. S2CID 45729390. doi:10.1007/BF03256855. (原始內容存檔於2012-02-06).
|url-status=和|dead-url=只需其一 (幫助) - ^ Electronic Orange Book. U.S. Food and Drug Administration. [2007-05-31]. (原始內容存檔於2020-04-07).
- ^ Access to new medicines in the English NHS. The King's Fund. 2020-10-28 [2020-10-30]. (原始內容存檔於2020-11-16).
- ^ The Orphan Drug Act (as amended). U.S. Food and Drug Administration. [2007-09-24]. (原始內容存檔於2020-04-07).
- ^ Gad, Shayne C. (編), Drug Development Process and Global Pharmaceutical Marketplace, Pharmaceutical Sciences Encyclopedia, 2010, doi:10.1002/9780470571224.pse127
- ^ (PDF) http://www.vfa.de/download/SHOW/en/statistics/pharmaceuticalmarket/vfastat_30_en_fa_mt.pdf/vfastat_30_en_sw_mt.pdf. [2008-03-24]. 缺少或
|title=為空 (幫助)[失效連結] - ^ The World's Ten Best-Selling Drugs. Forbes. 2006-03-22 [2020-10-28]. (原始內容存檔於2020-11-09).
- ^ Kollewe, Julia. World's 10 bestselling prescription drugs made $75bn last year. the Guardian. 2014-03-27 [2020-11-20]. (原始內容存檔於2020-04-07).
- ^ Top 100 Drugs for 2013 by Sales - U.S. Pharmaceutical Statistics. [2020-11-20]. (原始內容存檔於2014-03-31).
- ^ IMS Health Forecasts 5 to 6 Percent Growth for Global Pharmaceutical Market in 2007. Business Wire. 2006-10-24 [2020-10-28]. (原始內容存檔於2020-11-17).
- ^ Frequently Asked Questions (FAQs). [2020-11-20]. (原始內容存檔於2013-02-25).
- ^ New Drug Approvals in 2006 (PDF). March 2007 [2008-02-23]. (原始內容存檔 (PDF)於2008-02-28).
- ^ Assessment of Authorized Generics in the U.S (PDF). IMS Consulting. June 2006 [2008-02-23]. (原始內容存檔 (PDF)於2008-02-28).
- ^ Sanofi Laying Off 1,700 in US. Drug Discovery & Development. [2020-11-20]. (原始內容存檔於2011-09-11).
- ^ 2007 Health and Nutrition - Census (PDF). U.S. Census Bureau. [2016-05-19]. (原始內容存檔 (PDF)於2020-07-31).
- ^ Goldacre, Ben. Bad pharma : how drug companies mislead doctors and harm patients First American Paperback. 2014. ISBN 9780865478060.
- ^ Kaufman, Marc. Merck CEO Resigns as Drug Probe Continues. Washington Post. 2005-05-06 [2007-05-23]. (原始內容存檔於2020-11-09).
- ^ Drug Lobby Second to None: How the pharmaceutical industry gets its way in Washington. publicintegrity.org. 2005-07-07 [2007-05-23]. (原始內容存檔於2007-06-09).
|url-status=和|dead-url=只需其一 (幫助) - ^ Moynihan, R. Drug company sponsorship of education could be replaced at a fraction of its cost. BMJ. 2003-05-29, 326 (7400): 1163. PMC 1126044
 . PMID 12775595. doi:10.1136/bmj.326.7400.1163.
. PMID 12775595. doi:10.1136/bmj.326.7400.1163.
- ^ Dr. No Free Lunch. Mother Jones. [2016-05-19]. (原始內容存檔於2020-11-16).
- ^ Moynihan, Ray; Cassels, Alan. Selling Sickness: How the Drug Companies are Turning Us All into Patients. Crows Nest, N.S.W.: Allen & Unwin. 2005. ISBN 978-1-74114-579-3.
- ^ A Collection of Articles on Disease Mongering. Public Library of Science. [2007-05-23]. (原始內容存檔於2007-06-07).
- ^ Finding Evidence — Recognising Hype. National Prescribing Service Limited. [2020-10-29]. 原始內容存檔於2010-03-17.
- ^ Pharmaceutical Market Research, Trends And Analysis Reports. literated.com. [2016-01-17]. (原始內容存檔於2016-01-19).
|url-status=和|dead-url=只需其一 (幫助) - ^ Buchkowsky, SS; Jewesson, PJ. Industry sponsorship and authorship of clinical trials over 20 years. Ann Pharmacother. Apr 2004, 38 (4): 579–85. PMID 14982982. S2CID 43544256. doi:10.1345/aph.1D267.
- ^ Perlis RH, Perlis CS, Wu Y, Hwang C, Joseph M, Nierenberg AA. Industry sponsorship and financial conflict of interest in the reporting of clinical trials in psychiatry. Am J Psychiatry. October 2005, 162 (10): 1957–60. PMID 16199844. doi:10.1176/appi.ajp.162.10.1957.
- ^ Tungaraza, T; Poole, R. Influence of drug company authorship and sponsorship on drug trial outcomes. Br J Psychiatry. Jul 2007, 191 (1): 82–3. PMID 17602130. doi:10.1192/bjp.bp.106.024547.
- ^ Healy, D. The Latest Mania: Selling Bipolar Disorder. PLOS Med. 2006, 3 (4): e185. PMC 1434505
 . PMID 16597178. doi:10.1371/journal.pmed.0030185.
. PMID 16597178. doi:10.1371/journal.pmed.0030185.
- ^ Cosgrove, Lisa; Krimsky, Sheldon; Vijayaraghavan, Manisha; Schneider, Lisa. Financial Ties between DSM-IV Panel Members and the Pharmaceutical Industry. Psychotherapy and Psychosomatics. 2006, 75 (3): 154–160. PMID 16636630. S2CID 11909535. doi:10.1159/000091772.
- ^ Financial ties between DSM-IV panel members and the pharmaceutical industry. National Library of Medicine, National Center for Biotechnology Information. [2020-10-26]. (原始內容存檔於2020-11-15).
- ^ Open Payments. February 2019 [2020-11-20]. (原始內容存檔於2020-12-19).
- ^ Lipton, Eric; Thomas, Katie. Drug Lobbyists' Battle Cry Over Prices: Blame the Others. New York Times. 2017-05-29 [2017-05-30]. (原始內容存檔於2020-11-20).
- ^ Pricing of pharmaceuticals is becoming a major challenge for health systems. [2020-11-20]. (原始內容存檔於2020-11-27).
- ^ 121.0 121.1 Goldacre, Ben. Bad pharma : how drug companies mislead doctors and harm patients First American Paperback. 2014: 123–124. ISBN 9780865478060.
- ^ (PDF) http://www.whitehouse.gov/sites/default/files/microsites/ostp/pcast-fda-final.pdf. (原始內容存檔 (PDF)於2013-10-16). 缺少或
|title=為空 (幫助) - ^ Financial Crimes to the Public Report 2006. FBI. 2006 [2020-11-20]. (原始內容存檔於2016-05-29).
- ^ What is Best Price Fraud?. Berger Montague. [2020-10-29]. (原始內容存檔於2020-11-17).
- ^ 125.0 125.1 Understanding Pharmaceutical Fraud. LawsuitLegal.com. [2020-10-29]. (原始內容存檔於2020-11-14).
- ^ Whistleblower Cases Involving Medicaid Price Reporting. Nolan Auerbach & White. [2020-10-29]. (原始內容存檔於2020-11-09).
- ^ FBI-Health Care Fraud. FBI. [2020-11-20]. (原始內容存檔於2016-07-02).
- ^ Department of Justice. Department of Justice. 2015-03-19 [2020-11-20]. (原始內容存檔於2014-11-09).
- ^ Wilson, Duff. Side Effects May Include Lawsuits. New York Times. 2010-10-02 [2020-11-20]. (原始內容存檔於2017-06-23).
- ^ GlaxoSmithKline. BBC News. 2012-07-04 [2020-11-20]. (原始內容存檔於2020-11-17).
- ^ GlaxoSmithKline Agrees to Pay $3 Billion in U.S. Drug Settlement. Bloomberg. 2012-07-02 [2020-11-20]. (原始內容存檔於2014-05-14).
- ^ Mogul, Fred. NY to Get Millions in GlaxoSmithKlein Settlement. WNYC. 2012-07-02 [2012-07-02]. (原始內容存檔於2013-04-19).
|url-status=和|dead-url=只需其一 (幫助) - ^ BBC News -GlaxoSmithKline to pay $3bn in US drug fraud scandal. BBC Online. 2012-07-02 [2012-07-02]. (原始內容存檔於2020-11-17).
- ^ Thomas, Katie & Schmidt, Michael S. Glaxo Agrees to Pay $3 Billion in Fraud Settlement. The New York Times. 2012-07-02 [2012-07-03]. (原始內容存檔於2017-03-02).
- ^ Rapidly Increasing Criminal and Civil Penalties Against the Pharmaceutical Industry: 1991-2010. citizen.org. [2016-05-19]. (原始內容存檔於2016-05-16).
|url-status=和|dead-url=只需其一 (幫助) - ^ Thomas, Katie; Schmidt, Michael S. GlaxoSmithKline Agrees to Pay $3 Billion in Fraud Settlement. The New York Times. 2012-07-02 [2020-11-20]. (原始內容存檔於2020-11-12).
- ^ GlaxoSmithKline to Plead Guilty and Pay $3 Billion to Resolve Fraud Allegations and Failure to Report Safety Data. 2012-07-02 [2020-11-20]. (原始內容存檔於2014-09-09).
- ^ JUSTICE DEPARTMENT ANNOUNCES LARGEST HEALTH CARE FRAUD (PDF). US department of Justice. [2016-05-19]. (原始內容存檔 (PDF)於2020-12-02).
- ^ Abbott Labs to Pay $1.5 Billion to Resolve Criminal & Civil Investigations of Off-label Promotion of Depakote. 2012-05-07 [2020-11-20]. (原始內容存檔於2014-08-21).
- ^ #09-038: Eli Lilly and Company Agrees to Pay $1.415 Billion to Resolve Allegationsof Off-label Promotion of Zyprexa (2009-01-15). [2020-11-20]. (原始內容存檔於2016-03-13).
- ^ Bhandari M, Busse JW, Jackowski D, Montori VM, Schunemann H, Sprague S, Mears D, Schemitsch EH, Heels-Ansdell D, Devereaux PJ. Association between industry funding and statistically significant pro-industry findings in medical and surgical randomized trials. Canadian Medical Association Journal. 2004-02-17, 170 (4): 477–480. PMID 4. doi:10.1016/0006-291x(75)90506-9.
- ^ Moynihan, R. Who pays for the pizza? Redefining the relationships between doctors and drug companies. 2: Disentanglement. BMJ. 2003-05-29, 326 (7400): 1193–1196. PMC 1126054
 . PMID 12775622. doi:10.1136/bmj.326.7400.1193.
. PMID 12775622. doi:10.1136/bmj.326.7400.1193.
- ^ Hogan & Hartson Update on Pharmaceutical Trial Registration (PDF). 2008-03-03 [2008-06-02]. (原始內容存檔 (PDF)於2008-06-25).
|url-status=和|dead-url=只需其一 (幫助) - ^ Barnett, Antony. Revealed: how drug firms 'hoodwink' medical journals. the Guardian. 2003-12-07 [2016-05-19]. (原始內容存檔於2020-12-19).
- ^ Ornstein, Tracy Weber, Charles. Dollars for Docs Mints a Millionaire. ProPublica. 2013-03-11 [2016-05-19]. (原始內容存檔於2020-12-20).
- ^ Drazen, Jeffrey M. Revisiting the Commercial–Academic Interface — NEJM. New England Journal of Medicine. 2015, 372 (19): 1853–1854. PMID 25946285. doi:10.1056/NEJMe1503623.
- ^ Rosenbaum, Lisa. Reconnecting the Dots — Reinterpreting Industry–Physician Relations — NEJM. New England Journal of Medicine. 2015, 372 (19): 1860–1864. PMID 25946288. doi:10.1056/NEJMms1502493.
- ^ 148.0 148.1 148.2 No profiteering on COVID-19 drugs and vaccines, says MSF. Médecins Sans Frontières (MSF) International. [2020-11-20]. (原始內容存檔於2020-12-11) (英語).
- ^ 149.0 149.1 Mazzucato, Mariana; Momenghalibaf, Azzi. Drug Companies Will Make a Killing From Coronavirus. The New York Times. 2020-03-18 [2020-11-20]. (原始內容存檔於2020-11-23).
- ^ Johnson, Jake. 'An Outrage': HHS Chief Azar Refuses to Vow Coronavirus Vaccine Will Be Affordable for All, Not Just the Rich. Common Dreams. [2020-11-20]. (原始內容存檔於2020-11-30) (英語).
- ^ Olorunnipa, Toluse; Dawsey, Josh; Abutaleb, Yasmeen. Trump downplays risk, places Pence in charge of coronavirus outbreak response. Washington Post. [2020-11-20]. (原始內容存檔於2020-12-14) (英語).
- ^ Lerner, Sharon. Big Pharma Prepares to Profit From the Coronavirus. The Intercept. 2020-03-13 [2020-11-20]. (原始內容存檔於2020-12-13).
- ^ Schakowsky, Jan. Letter to Alex Azar. [2020-11-20]. (原始內容存檔於2020-12-05).
- ^ Karlin-Smith, Sarah. How the drug industry got its way on the coronavirus. POLITICO. [2020-11-20]. (原始內容存檔於2020-12-13) (英語).
- ^ 155.0 155.1 Lupkin, Sydney. FDA Grants Experimental Coronavirus Drug Benefits For Rare Disease Treatments. NPR. 2020-03-24 [2020-03-24]. (原始內容存檔於2020-12-14).
- ^ 156.0 156.1 156.2 Conley, Julia. 'This Is a Massive Scandal': Trump FDA Grants Drug Company Exclusive Claim on Promising Coronavirus Drug. Common Dreams. 2020-03-24 [2020-11-20]. (原始內容存檔於2020-12-08) (英語).
- ^ Boodman, Eric. Gilead ups its donation of the Covid-19 drug remdesivir for U.S. hospitals. statnews.com. 2020-05-18 [2020-07-19]. (原始內容存檔於2020-12-20).
- ^ Lawson, Alex. Don't Let Big Pharma Make a Killing by Profiteering Off COVID-19 Treatments. Common Dreams. 2020-03-25 [2020-11-20]. (原始內容存檔於2020-11-09) (英語).
- ^ 存档副本. [2020-11-20]. (原始內容存檔於2020-12-11).
- ^ Treatment Action Group Statement on the High Price of Cepheid's Xpert Test for COVID-19. Treatment Action Group. [2020-11-20]. (原始內容存檔於2020-11-09).
- ^ Haseltine, William A. Tests For COVID-19 Are Expensive, But They Don't Have To Be. Forbes. [2020-11-20]. (原始內容存檔於2020-12-13) (英語).
- ^ 162.0 162.1 Omran, Dalia; Alboraie, Mohamed; Zayed, Rania A; Wifi, Mohamed-Naguib; Naguib, Mervat; Eltabbakh, Mohamed; Abdellah, Mohamed; Sherief, Ahmed Fouad; Maklad, Sahar; Eldemellawy, Heba Hamdy; Saad, Omar Khalid; Khamiss, Doaa Mohamed; El Kassas, Mohamed. Towards hepatitis C virus elimination: Egyptian experience, achievements and limitations. World Journal of Gastroenterology. 2018-10-14, 24 (38): 4330–4340. ISSN 1007-9327. PMC 6189850
 . PMID 30344418. doi:10.3748/wjg.v24.i38.4330.
. PMID 30344418. doi:10.3748/wjg.v24.i38.4330.
- ^ Crisanti, Andrea; Cassone, Antonio. In one Italian town, we showed mass testing could eradicate the coronavirus. The Guardian. 2020-03-20 [2020-11-20]. (原始內容存檔於2020-03-23).
- ^ See for example: 't Hoen, Ellen. "TRIPS, Pharmaceutical Patents, and Access to Essential Medicines: A Long Way from Seattle to Doha". Chicago Journal of International Law, 27(43), 2002; Musungu, Sisule F., and Cecilia Oh. "The Use of Flexibilities in TRIPS by Developing Countries: Can They Provide Access to Medicines?" Commission on Intellectual Property Rights, Innovation and Public Health, The World Health Organization, 2005.
- ^ Declaration on the TRIPS agreement and public health. World Trade Organization. [2016-05-19]. (原始內容存檔於2020-12-08).
- ^ Pharmaceutical Manufacturer's Association v. The President of South Africa (PMA), 2002 (2) SA 674 (CC) (S. Africa).
- ^ Helfer, Laurence R.; Austin, Graeme W. Human Rights and Intellectual Property: Mapping the Global Interface. Cambridge University Press. 2011-03-07: 145–148 [2020-11-20]. ISBN 978-1-139-49691-9. (原始內容存檔於2020-11-16).
- ^ GlaxoSmithKline to 'drop patents in poor countries for better drug access'. BBC News. [2016-05-19]. (原始內容存檔於2020-11-09).
- ^ Bumper Year for Corporate Donations Reveals Profit Motives. corpwatch.org. [2020-11-20]. (原始內容存檔於2017-11-11).
- ^ Merk. [2006-08-30]. (原始內容存檔於2006-08-26).
|url-status=和|dead-url=只需其一 (幫助) - ^ Pfizer Will Donate Fluconazole to South Africa. [2006-08-30]. (原始內容存檔於2010-10-24).
|url-status=和|dead-url=只需其一 (幫助) - ^ Corporate Citizenship. Investopedia. 2020-08-21 [2020-10-29]. (原始內容存檔於2020-11-27).
- ^ Corporate Responsibility: Novartis. novartis.com. [2016-05-19]. (原始內容存檔於2017-09-01).
外部連結
[編輯]- Global Medicines Use in 2020. IMS Institute for Healthcare Informatics. November 2015 [2020-11-20]. (原始內容存檔於2020-11-28).
- The pharmaceutical industry and global health - Facts & figures 2017 (PDF). International Federation of Pharmaceutical Manufacturers & Associations. February 2017 [2020-11-20]. (原始內容存檔 (PDF)於2020-12-12).
- The Pharmaceutical Industry in Figures - Key Data 2018 (PDF). European Federation of Pharmaceutical Industries and Associations. [2020-11-20]. (原始內容存檔 (PDF)於2020-11-12).
