Histidine
L'histidine (abréviations IUPAC-IUBMB : His et H), du grec ancien ἱστός, ἱστίον (« mât de navire », « métier à tisser », « voile de navire »[5])[6], est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, l'un des 9 acides aminés essentiels et fait partie des acides aminés glucoformateur. Elle est encodée sur les ARN messagers par les codons CAU et CAC. Elle est caractérisée par la présence d'un cycle imidazole qui confère une nature basique aux résidus d'histidine dans les protéines. Son rayon de van der Waals est égal à 118 Å.
| Histidine | |
 L ou S(–)-histidine 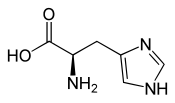 D ou R(+)-histidine |
|
| Identification | |
|---|---|
| Nom UICPA | acide 2-amino-3-(1H-imidazol-4-yl)propanoïque |
| Synonymes |
H, His |
| No CAS | (racémique) (L) ou S(–) (D) ou R(+) |
| No ECHA | 100.000.678 |
| No CE | 200-745-3 206-513-8 (D) |
| FEMA | 3694 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C6H9N3O2 [Isomères] |
| Masse molaire[1] | 155,154 6 ± 0,006 6 g/mol C 46,45 %, H 5,85 %, N 27,08 %, O 20,62 %, |
| pKa | 1,70 6,04 9,09 |
| Propriétés physiques | |
| T° fusion | 287 °C |
| Propriétés biochimiques | |
| Codons | CAU, CAC |
| pH isoélectrique | 7,59[2] |
| Acide aminé essentiel | oui |
| Occurrence chez les vertébrés | 2,9 %[3] |
| Précautions | |
| SIMDUT[4] | |
Produit non contrôlé |
|
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Biosynthèse
modifierContrairement aux micro-organismes et aux plantes qui sont capables de synthétiser l'histidine, les animaux en sont incapables. Leur seul moyen de s'en procurer se situe dans leur alimentation. Qualifiée chez l'humain adulte, comme étant un acide aminé semi-indispensable, il devient cependant indispensable chez l'enfant car l'histidine intervient dans les processus de croissance biologique[7].
Fonction dans les protéines
modifierL'histidine est un acide aminé qui remplit des fonctions importantes dans la structure et la fonction des protéines. Le noyau imidazole de l'histidine dispose d'un atome d'azote pouvant capter un proton, avec un pKa proche de la neutralité (pKa~6.8) et donc des conditions physiologiques. Cette propriété est cruciale pour la fonction de certaines protéines :
- elle permet à certains résidus d'histidine présents dans les sites actifs d'enzymes d'intervenir dans des réactions de transfert de proton, dans les conditions physiologiques du cytoplasme (pH~7) ;
- dans l'hémoglobine, les histidines présentes dans la protéine participent au maintien du pH sanguin en agissant comme molécule tampon.
L'azote du cycle imidazole des histidines peut également former des liaisons de coordination avec des ions métalliques comme Zn2+, Co2+, Fe2+ ou Ni2+. Ces liaisons sont importantes pour la fixation de ces ions dans des métalloprotéines, où la complexation du métal est requise pour l'activité de la protéine. On trouve par exemple une histidine comme ligand axial du fer dans la myoglobine et l'hémoglobine et deux histidines dans la complexation du zinc présent dans la collagénase, une protéase qui dégrade le collagène.
Autres rôles
modifierPurification par chromatographie d'affinité métallique
modifierLa propriété de fixation des ions métalliques par l'histidine est à la base d'une technologie de purification des protéines recombinantes appelée chromatographie d'affinité pour ions métalliques immobilisés ((en) IMAC, pour immobilized metal affinity chromatography).
Le principe de cette méthode est le suivant : par génie génétique, on ajoute à la protéine une séquence contenant au moins six histidines consécutives (étiquette polyhistidine). Cette étiquette est capable d'interagir fortement avec des ions métalliques. On utilise cette propriété pour fixer la protéine ainsi étiquetée sur une résine chromatographique sur laquelle est chélaté un ion métallique. Après lavage des protéines non retenues, la protéine est ensuite éluée par une solution d'imidazole qui déplace la protéine de l'ion métallique par compétition.
Dérivés de l'histidine
modifierPar méthylation de l'histidine en 1, ou en 3, on obtient des acides aminés méthylés présents dans l'urine de l'homme. Cet acide aminé également est un précurseur de la biosynthèse de l'histamine (vasodilatateur) et de la carnosine.
Présence dans le corps humain
modifierEn mesure BDC (Binary coded decimal ) un taux normal d'Histidine dans le corps est compris entre 391 et 547 selon la méthode turbidimétrique réalisée sur Olympus AU640[8]
Propriétés chimiques et physiques
modifierEn utilisant le sel d'histidine comme exemple, une interaction anion-anion du type anion carboxylate-tétroxyde a été découverte pour la première fois[9].
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Francis A. Carey, « Table of pKa and pI values », sur Département de chimie de l'université de Calgary, (consulté le ).
- (en) M. Beals, L. Gross, S. Harrell, « Amino Acid Frequency », sur The Institute for Environmental Modeling (TIEM) à l'université du Tennessee (consulté le ).
- « Histidine (l-) » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Abrégé du dictionnaire grec-français A. Bailly, p. 441.
- Terminologie médicale, par Georges Dolisi
- (en) Joanna Moro, Daniel Tomé, Philippe Schmidely et Tristan-Chalvon Demersay, « Histidine: A Systematic Review on Metabolism and Physiological Effects in Human and Different Animal Species », Nutrients, vol. 12, no 5, , p. 1414 (ISSN 2072-6643, PMID 32423010, PMCID PMC7284872, DOI 10.3390/nu12051414, lire en ligne, consulté le )
- laboratoire d'analyses CEIA Bruxelles
- (en) Anton P. Novikov, Alexey V. Safonov, Konstantin E. German et Mikhail S. Grigoriev, « What kind of interactions we may get moving from zwitter to “dritter” ions: C–O⋯Re(O4) and Re–O⋯Re(O4) anion⋯anion interactions make structural difference between L-histidinium perrhenate and pertechnetate », CrystEngComm, (ISSN 1466-8033, DOI 10.1039/D3CE01164J, lire en ligne, consulté le )