Peroxyde de calcium
| Peroxyde de calcium | |
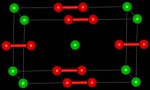
| |
| Identification | |
|---|---|
| Nom UICPA | Peroxyde de calcium |
| Synonymes |
E930 |
| No CAS | |
| No ECHA | 100.013.764 |
| No RTECS | EW3865000 |
| PubChem | |
| ChEBI | 48233 |
| SMILES | |
| InChI | |
| Apparence | solide blanc ou jaunâtre |
| Propriétés chimiques | |
| Formule | CaO2 |
| Masse molaire[1] | 72,077 ± 0,005 g/mol Ca 55,6 %, O 44,4 %, 72.0768 g/mol |
| pKa | 12.5 |
| Propriétés physiques | |
| T° fusion | ~200 °C (decomp.) |
| Solubilité | dans l'eau : non miscible |
| Masse volumique | 2,91 g/cm3 |
| Cristallographie | |
| Système cristallin | Tétragonal |
| Symbole de Pearson | |
| Classe cristalline ou groupe d’espace | D174h, I4/mmm |
| Propriétés optiques | |
| Indice de réfraction | 1.895 |
| Écotoxicologie | |
| DL50 | >5000 mg/kg (oral, rat) >10000 mg/kg (peau, rat) |
| Composés apparentés | |
| Autres cations | Peroxyde de baryum Peroxyde de magnésium Peroxyde de potassium Peroxyde de sodium Peroxyde de strontium (en) |
| Autres anions | Oxyde de calcium |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le peroxyde de calcium (CaO2) est un peroxyde solide de couleur blanche ou jaunâtre. Ce composé est insoluble dans l'eau, mais se dissout dans les acides en formant du peroxyde d'hydrogène. Au contact de l'eau et de l'humidité, il se décompose immédiatement en libérant de l'oxygène.
Préparation
[modifier | modifier le code]Le peroxyde de calcium est créé en faisant interagir du sel de calcium et du peroxyde de sodium, ce qui provoque une cristallisation.
L’octa-hydrate est synthétisé par la réaction entre l'hydroxyde de calcium avec du peroxyde d'hydrogène dilué.
Applications
[modifier | modifier le code]Le peroxyde de calcium est utilisé en industrie et en agriculture. En agriculture il est utilisé comme engrais apportant de l'oxygène et comme prétraitement des semis de riz. Il est utilisé en aquaculture pour oxygéner et désinfecter l’eau et dans l’industrie écologique pour le traitement des sols. Il est utilisé de manière similaire au peroxyde de magnésium dans les programmes de restauration environnementaux. Il est utilisé pour traiter les sols et les eaux souterraines contaminés par les dérivés du pétrole en stimulant la dégradation microbienne aérobie des contaminants lors du processus appelé Enhanced In-Situ Bioremediation.
Il a, en tant qu'additif alimentaire, le numéro E E930 et il est utilisé comme agent de blanchiment et agent de traitement des farines.
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Calcium peroxide » (voir la liste des auteurs).

