Limoneno
| Limoneno Alerta sobre risco à saúde | |
|---|---|
|

|
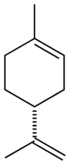
| Nome IUPAC | 1-methyl-4-prop-1-en-2-yl-cyclohexene |
| Outros nomes | 4-isopropenyl-1-methylcyclohexene Racemic: DL-limonene; dipentene |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C10H16 |
| Massa molar | 136.24 g/mol |
| Densidade | 0.8411 g/cm3
Optical Rotation = 87° - 102° |
| Ponto de fusão |
-74.35 °C |
| Ponto de ebulição |
176 °C |
| Riscos associados | |
| Frases R | R10 R38 R43 R35 |
| Frases S | S2 S24 S37 S60 S61 |
| Ponto de fulgor | 50 °C |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O Limoneno (IUPAC: 1-metil-4-(prop-1-en-2-il)ciclohex-1-eno) é uma substância química, orgânica, natural, pertencente à família dos terpenos, classe dos monoterpenos, de fórmula molecular C10H16, encontrada em frutas cítricas (sendo o principal componente do óleo das cascas de limões e laranjas), volátil e, por isso, responsável pelo cheiro que essas frutas apresentam.
Industrialmente é utilizado para produzir para-cimeno por desidrogenação catalítica. Nos últimos anos a sua demanda tem aumentado muito devido ao seu uso em solventes biodegradáveis.
Por possuir um centro quiral, concretamente um carbono assimétrico, apresenta isomeria óptica. Portanto, existem dois isômeros ópticos: o D-limoneno e o L-limoneno. A nomenclatura IUPAC correta é R-limoneno e S-limoneno, porém se emprega com mais frequência os prefixos D e L ou alfa e beta.
Química
[editar | editar código-fonte]
O limoneno é um terpeno relativamente estável e pode ser destilado sem decomposição, embora a elevadas temperaturas ele seja "craqueado" formando isopreno.[1] Ele oxida-se facilmente em ar úmido produzindo carvol [en] e carvona.[2] Com enxofre, ele sofre desidrogenação e é convertido em p-cimeno.
Usos
[editar | editar código-fonte]Nos últimos anos tem adquirido uma importância fundamental devido a sua demanda como solvente biodegradável, e como combustível sustentável. Além disto também apresenta aplicações como componente aromático e é usado amplamente na síntese de novos compostos.[3]
Por ser um derivado dos cítricos, o limoneno pode ser considerado um agente de transferência de calor limpo e ambientalmente inócuo, pelo qual é utilizado em muitos processos farmacêuticos e de alimentos.
O limoneno é usado, por exemplo, em dissolventes de resinas, pigmentos, tintas, na fabricação de adesivos, etc. Também é usado como combustível duas vezes mais eficiente do que derivados do petróleo e pelas indústrias farmacêuticas e alimentícias como componente aromático e para dar sabor (flavorizantes), na obtenção de sabores artificiais de menta e na fabricação de doces e chicletes.[4]
Referências
- ↑ H. Pakdela, D. Panteaa and C. Roy (2001). «Production of dl-limonene by vacuum pyrolysis of used tires». J Anal Appl Pyrolysis. 57 (1): 91–107. doi:10.1016/S0165-2370(00)00136-4
- ↑ Source: European Chemicals Bureau.
- ↑ AZAMBUJA, W. Óleos Essenciais. Disponível em: <http://www.oleosessenciais.org/>. Acesso em 23 ago. 2011.
- ↑ «Combustível feito com casca de limão». Portal Aprendiz. 14 de março de 2007. Consultado em 13 de junho de 2020
Ligações externas
[editar | editar código-fonte]- Limoneno; FCT - www.dq.fct.unl.pt/
