Poliovirüs
| Poliovirüs | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||
 Bir tip 3 poliovirüs kapsidi, renkli protein yan zincirleri | |||||||||||||||||||||
| Virüs sınıflandırması | |||||||||||||||||||||
| |||||||||||||||||||||
| Serotipler | |||||||||||||||||||||
| |||||||||||||||||||||
Çocuk felcinin (poliomyelit olarak da bilinir) etkeni olan poliovirüs veya çocuk felci virüsü, Picornaviridae ailesinde yer alan Enterovirüs C türünün bir serotipidir.[1] Üç poliovirüs serotipi vardır: tip 1, 2 ve 3.
Poliovirüs bir RNA genomu ve bir protein kapsidinden oluşur. Genom, yaklaşık 7500 nükleotit uzunluğunda tek sarmallı pozitif anlamlı bir RNA (+ssRNA) genomudur.[2] Viral partikül yaklaşık 30 nm çapındadır ve ikozahedral simetriye sahiptir. Kısa genomu ve basit bileşimi (sadece RNA ve onu saran zarfsız ikozahedral protein kabuğu) nedeniyle, poliovirüs yaygın olarak en basit önemli virüs olarak kabul edilir.[3]
Poliovirüs ilk olarak 1909 yılında Karl Landsteiner ve Erwin Popper tarafından izole edilmiştir.[4] Virüsün yapısı ilk olarak 1958 yılında Birkbeck College'da Rosalind Franklin liderliğindeki bir ekip tarafından X-ışını kırınımı kullanılarak aydınlatılmış[5][6] ve çocuk felci virüsünün ikozahedral simetriye sahip olduğu gösterilmiştir.[7]
1981 yılında poliovirüs genomu iki farklı araştırmacı ekibi tarafından yayınlandı: MIT'den Vincent Racaniello ve David Baltimore[8] ile Stony Brook Üniversitesinden Naomi Kitamura ve Eckard Wimmer.[9]
Poliovirüsün üç boyutlu yapısı 1985 yılında Scripps Araştırma Enstitüsünde James Hogle tarafından X-ışını kristalografisi kullanılarak belirlenmiştir.[10]
Poliovirüs en iyi karakterize edilmiş virüslerden biridir ve RNA virüslerinin biyolojisini anlamak için yararlı bir model sistem haline gelmiştir.
Çoğalma döngüsü
[değiştir | kaynağı değiştir]
Poliovirüs, hücre yüzeyindeki immünoglobulin benzeri bir reseptör olan CD155'e (poliovirüs reseptörü veya PVR olarak da bilinir)[12][13] bağlanarak insan hücrelerini enfekte eder.[14] Poliovirüs ve CD155'in etkileşimi, viral giriş için gerekli olan viral partikülün geri dönüşü olmayan bir konformasyonel değişimini kolaylaştırır.[15][16] Konak hücre membranına bağlanmanın ardından viral nükleik asidin girişinin iki yoldan biriyle gerçekleştiği düşünülmüştür: plazma membranında bir por oluşumu yoluyla RNA'nın konak hücre sitoplazmasına "enjekte edilmesi" veya reseptör aracılı endositoz yoluyla virüs alımı.[17] Son deneysel kanıtlar ikinci hipotezi desteklemekte ve poliovirüsün CD155'e bağlandığını ve endositoz yoluyla alındığını göstermektedir. Partikülün içselleştirilmesinden hemen sonra viral RNA serbest kalır.[18]
Poliovirüs pozitif sarmallı bir RNA virüsüdür. Bu nedenle, viral partikül içinde bulunan genom, haberci RNA olarak kullanılabilir ve konak hücre tarafından hemen transle edilebilir. Virüs hücreye girdiğinde hücrenin çeviri mekanizmasını ele geçirerek virüse özgü protein üretimi lehine hücresel protein sentezinin engellenmesine neden olur.[19]
Konak hücrenin mRNA'larının aksine, poliovirüs RNA'sının 5' ucu son derece uzundur - 700 nükleotidin üzerinde - ve oldukça yapılandırılmıştır. Viral genomun bu bölgesi iç ribozom giriş bölgesi (IRES) olarak adlandırılır. Bu bölge birçok ikincil yapı ve 3 veya 4 alandan oluşur. Alan 3, iki dört yönlü bağlantı ile birbirine bağlanan çeşitli sabit kök döngülerinde korunmuş yapısal motifler içeren, kendi kendine katlanan bir RNA elementidir. IRES birçok alandan oluştuğu için, bu alanların kendileri de ribozomları kaçırarak 5' uç kapağı olmadan değiştirilmiş çeviriye katkıda bulunan birçok döngüden oluşur. Alan 3'ün etkileşim döngüsü GNRA tetraloop olarak bilinir. GUAA tetraloopundaki A180 ve A181 adenozin kalıntıları, sırasıyla C230/G242 ve G231/C241 reseptörlerinin baz çiftleriyle kanonik olmayan baz eşleştirme etkileşimleri yoluyla hidrojen bağları oluşturur.[20] Bu bölgedeki genetik mutasyonlar viral protein üretimini engeller.[21][22][23] Keşfedilen ilk IRES poliovirüs RNA'sında bulunmuştur.[24]
Poliovirüs mRNA'sı uzun bir polipeptit olarak çevrilir. Bu polipeptit daha sonra dahili proteazlar tarafından yaklaşık 10 ayrı viral proteine otomatik olarak ayrılır. Tüm bölünmeler aynı verimlilikte gerçekleşmez. Bu nedenle, polipeptit bölünmesi ile üretilen protein miktarları değişiklik gösterir: örneğin, kapsit proteinleri VP1-4'ten daha az miktarda 3Dpol üretilir.[25][26] Bu bireysel viral proteinler şunlardır:[3][27]

- 3Dpol, işlevi viral RNA genomunun birden fazla kopyasını oluşturmak olan bir RNA bağımlı RNA polimeraz
- 2Apro ve 3Cpro/3CDpro, viral polipeptidi parçalayan proteazlar
- VPg (3B), viral RNA'yı bağlayan ve viral pozitif ve negatif iplik RNA sentezi için gerekli olan küçük bir protein
- Virüs replikasyonu için gerekli protein kompleksini oluşturan 2BC, 2B, 2C (bir ATPaz),[11] 3AB, 3A, 3B proteinleri.
- VP2 ve VP4, VP1 ve VP3'e bölünen VP0, viral kapsidin proteinleri
Tek bir süreci içeren translasyon, transkripsiyon ve genom replikasyonundan sonra (+) RNA sentezi gerçekleşir. Enfekte eden (+) RNA'nın kopyalanabilmesi için (-) RNA'nın birden fazla kopyasının kopyalanması ve ardından (+) RNA sentezi için şablon olarak kullanılması gerekir.
Bir şablon RNA ve değişen uzunlukta birkaç büyüyen RNA'dan oluşan RNA moleküllerinin bir birliği olan replikatif ara ürünler (RI'ler), hem (-) RNA'lar hem de (+) RNA'lar için replikasyon komplekslerinde görülür. Her bir negatif iplikçikli ve pozitif iplikçikli RNA'ların sentezi için poliovirüsteki VPg proteini bir primer olarak çalışır.
Poliovirüsün RNA'ya bağımlı RNA polimerazı, negatif iplikçikli antijenomik RNA'nın sentezi için bir model olarak +ssRNA genomunun 3′-ucundaki poli(A) kuyruğunu kullanarak VPg proteinine iki urasil nükleotidi (UU) ekler. Bu -ssRNA sentezini başlatmak için VPg'nin tirozin hidroksiline ihtiyaç vardır. Ancak pozitif iplikçikli RNA sentezinin başlatılması için CRE'ye bağlı VPg uridilasyonuna ihtiyaç vardır. Bu da VPg'nin bir kez daha primer olarak kullanıldığı anlamına gelir, ancak bu sefer şablon olarak bir cis-etkili replikasyon elementi (CRE) kullanarak iki üridin trifosfat ekler.[28][29]
Poliovirüsün CRE'si, ulaşılmamış baz eşli bir kök ve 61 nt'den oluşan bir son döngü olarak tanımlanır. CRE enterovirüslerde bulunur. Yüksek oranda korunmuş bir ikincil RNA yapısal elemanıdır ve genomun poliprotein kodlama bölgesinde yer alır.
Kompleks, genomun kodlama aktivitesi olmayan 5' bölgesine, başlangıç konumundan en az 3,7 kb uzakta yer değiştirebilir. Bu süreç, aktiviteyi olumsuz etkilemeden gerçekleşebilir. CRE kopyaları replikasyonu olumsuz etkilemez.
CRE'de gerçekleşen VPg'nin üridilasyon süreci, bir RNA bağlayıcı protein olan 3CDpro'nun varlığına ihtiyaç duyar. CRE'ye doğrudan ve spesifik olarak bağlanır. Varlığı sayesinde VPg CRE'ye düzgün bir şekilde bağlanabilir ve primer üretim sorunsuz bir şekilde ilerler.[30]
(+) RNA moleküllerinin bazıları daha ileri (-) RNA sentezi için şablon olarak kullanılır, bazıları mRNA olarak işlev görür ve bazıları da yavru virionların genomları olmaya adaydır.[25]
Yeni virüs partiküllerinin birleştirilmesinde (yani, progen genomunun konak hücre dışında hayatta kalabilen bir prokapsit içine paketlenmesi), sırasıyla:[31]
- N terminalleri ve VP4 kapsidin iç yüzeyini oluşturan VP0, VP3 ve VP1'in her birinin beş kopyası bir 'pentamer' halinde birleşir ve 12 pentamer bir prokapsid oluşturur. (Kapsidin dış yüzeyi VP1, VP2, VP3'ten oluşur; VP1 ve VP3'ün C terminalleri her bir köşenin etrafındaki kanyonları oluşturur; bu sırada VP0'ın 60 kopyası VP4 ve VP2'ye ayrılır).
- Her bir prokapsid virüs genomunun bir kopyasını alır ve VPg hala 5' ucuna bağlıdır.
Tamamen bir araya gelmiş poliovirüs, kültürlenmiş memeli hücrelerinde enfeksiyonun başlamasından 4 ila 6 saat sonra lizis yoluyla konakçı hücresinin sınırlarını terk eder.[32][33] Hücreden viral salınım mekanizması belirsizdir,[2] ancak ölen her hücre 10.000 kadar polio virionu salabilir.[33]
Poliovirüsün çoklu reaktivasyona uğrayabildiğini gösterilmiştir.[34] Yani, poliovirüsler UV ışığınamaruz kaldığında ve konak hücrelerin birden fazla enfeksiyon geçirmesine izin verildiğinde, tek enfeksiyonlarda virüsü inaktive eden UV dozlarında bile canlı döller oluşabilir. Poliovirüs, aynı konak hücrede en az iki viral genom bulunduğunda genetik rekombinasyona uğrayabilir. Kirkegaard ve Baltimore,[34] RNA'ya bağımlı RNA polimerazın (RdRP) rekombinasyonu, RdRP'nin negatif iplik sentezi sırasında (+) ssRNA şablonları arasında geçiş yaptığı bir kopya seçim mekanizması ile katalize ettiğine dair kanıt sunmuştur. RNA virüslerinde rekombinasyon, genom hasarını onarmak için uyarlanabilir bir mekanizma gibi görünmektedir.[35][36]
Köken ve serotip
[değiştir | kaynağı değiştir]Poliovirüs yapısal olarak diğer insan enterovirüslerine (koksakivirüsler, ekovirüsler ve rinovirüsler) benzemektedir ve bunlar da konakçı hücreleri tanımak ve onlara girmek için immünoglobulin benzeri moleküller kullanmaktadır.[13] Poliovirüsün RNA ve protein dizilerinin filogenetik analizi, kapsit içindeki bir mutasyonla ortaya çıkan bir C kümesi Koksaki A virüs atasından evrimleşmiş olabileceğini düşündürmektedir.[37] Poliovirüsün farklı türleşmesi muhtemelen C-kümesi Coxsackie A virüsleri tarafından kullanılan hücreler arası adezyon molekülü-1'den (ICAM-1) CD155'e hücresel reseptör özgüllüğündeki bir değişikliğin sonucu olarak meydana gelmiştir; bu da patojenitede bir değişikliğe yol açmış ve virüsün sinir dokusunu enfekte etmesine izin vermiştir.
Virüsteki mutasyon oranı, 1,0 x 10-2 sübstitüsyon/site/yıl eşanlamlı sübstitüsyon oranı ve 3,0 x 10-4 sübstitüsyon/site/yıl eşanlamlı olmayan sübstitüsyon oranı ile bir RNA virüsü için bile nispeten yüksektir.[38] Genom içindeki baz dağılımı rastgele değildir; adenozin 5' ucunda beklenenden daha az yaygındır ve 3' ucunda daha yüksektir.[39] Kodon kullanımı rastgele değildir, adenozin ile biten kodonlar tercih edilirken sitozin veya guanin ile bitenlerden kaçınılır. Kodon kullanımı üç genotip arasında farklılık gösterir ve seçilimden ziyade mutasyon tarafından yönlendiriliyor gibi görünmektedir.[40]
Poliovirüsün üç serotipi olan PV-1, PV-2 ve PV-3'ün her biri biraz farklı bir kapsit proteinine sahiptir. Kapsit proteinleri hücresel reseptör özgüllüğünü ve virüs antijenitesini tanımlar. PV-1 doğada en sık rastlanan formdur, ancak her üç form da son derece bulaşıcıdır.[4] Mart 2020 itibarıyla, vahşi PV-1 Pakistan ve Afganistan'daki bölgelerde oldukça lokalize olmuştur. En son 1999'da tespit edilen yabani PV-2 için Eylül 2015'te[41] ve en son 2012'de tespit edilen yabani PV-3 için Ekim 2019'da yerel bulaşmanın ortadan kaldırıldığının belgelendirilmesi gerçekleşmiştir.[42]
Çocuk felcine karşı aşı hazırlamak için her serotipin spesifik suşları kullanılmaktadır. İnaktif çocuk felci aşısı, Mahoney veya Brunenders (PV-1), MEF-1/Lansing (PV-2) ve Saukett/Leon (PV-3) olmak üzere üç vahşi, virülan referans suşun formalin ile inaktive edilmesiyle hazırlanır. Oral polio aşısı, üç poliovirüs serotipinin canlı zayıflatılmış suşlarını içerir. Virüs suşlarının maymun böbrek epitel hücrelerinde pasajlanması, viral IRES'te mutasyonlar meydana getirir ve virüsün sinir dokusunu enfekte etme yeteneğini engeller (veya zayıflatır).[33]
Poliovirüsler eskiden Picornaviridae familyasındaki Enterovirüs cinsine ait ayrı bir tür olarak sınıflandırılmaktaydı. 2008 yılında Poliovirüs türü ortadan kaldırılmış ve üç serotip, Picornaviridae familyasındaki Enterovirüs cinsinde yer alan İnsan enterovirüs C (daha sonra Enterovirüs C olarak yeniden adlandırılmıştır) türüne atanmıştır. Enterovirüs cinsinin tip türü Poliovirüs'ten (İnsan) Enterovirüs C olarak değiştirilmiştir.[43]
Patogenez
[değiştir | kaynağı değiştir]
Herhangi bir virüs için enfeksiyonun birincil belirleyicisi, bir hücreye girme ve ek bulaşıcı partiküller üretme yeteneğidir. CD155'in varlığının poliovirüs tarafından enfekte edilebilecek hayvan ve dokuları tanımladığı düşünülmektedir. CD155 (laboratuvarlar dışında) sadece insanların, yüksek primatların ve Eski Dünya maymunlarının hücrelerinde bulunur. Bununla birlikte, poliovirüs kesinlikle bir insan patojenidir ve doğal olarak başka hiçbir türü enfekte etmez (şempanzeler ve Eski Dünya maymunları deneysel olarak enfekte edilebilmesine rağmen).[44]
CD155 geni pozitif seçilime maruz kalmış gibi görünmektedir.[45] Protein, D1 alanının polio virüsü bağlanma bölgesini içerdiği birkaç alana sahiptir. Bu alan içerisinde 37 amino asit virüsün bağlanmasından sorumludur.
Poliovirüs bir enterovirüstür. Enfeksiyon fekal-oral yolla gerçekleşir, yani kişi virüsü yutar ve viral replikasyon gastrointestinal sistemde gerçekleşir.[46] Virüs, enfekte bireylerin dışkısıyla atılır. Vakaların %95'inde sadece birincil, geçici bir viremi (kan dolaşımında virüs) varlığı meydana gelir ve poliovirüs enfeksiyonu asemptomatiktir. Vakaların yaklaşık %5'inde virüs kahverengi yağ, retiküloendotelyal doku ve kas gibi diğer bölgelere yayılır ve çoğalır. Devam eden viral replikasyon sekonder viremiye neden olur ve ateş, baş ağrısı ve boğaz ağrısı gibi minör semptomların gelişmesine yol açar.[47]
Paralitik poliomyelit, poliovirüs enfeksiyonlarının %1'inden daha azında görülür. Paralitik hastalık, virüs merkezi sinir sistemine (MSS) girdiğinde ve omurilik, beyinsapı veya motor korteks içindeki motor nöronlarda çoğaldığında ortaya çıkar ve motor nöronların seçici olarak tahrip olmasına neden olarak geçici veya kalıcı felce yol açar. Bu, annelerinden edindikleri anti-poliovirüs antikorlarına hala sahip olan bebeklerde çok nadir görülen bir olaydır.[48]
Nadir durumlarda, paralitik poliomyelit solunum durmasına ve ölüme yol açar. Paralitik hastalık vakalarında, güçsüzlük ve felç başlamadan önce sıklıkla kas ağrısı ve spazmlar görülür. Felç tipik olarak iyileşmeden önce günlerden haftalara kadar devam eder.[49]
Birçok açıdan, enfeksiyonun nörolojik fazının normal gastrointestinal enfeksiyonun tesadüfi bir sapması olduğu düşünülmektedir.[17] Poliovirüsün MSS'ye giriş mekanizmaları tam olarak anlaşılamamıştır. Girişi açıklamak için birbirini dışlamayan üç hipotez öne sürülmüştür. Tüm teoriler primer viremi gerektirmektedir.
İlk hipotez, virionların CD155'ten bağımsız olarak kan-beyin bariyerini geçerek doğrudan kandan merkezi sinir sistemine geçtiğini öngörmektedir.[50] İkinci bir hipotez, virionların viremik kanla yıkanan periferik dokulardan, örneğin kas dokusundan, retrograd aksonal taşıma yoluyla sinir yolları üzerinden omuriliğe taşındığını öne sürer.[51][52][53] Üçüncü bir hipotez ise virüsün enfekte monositler ya da makrofajlar aracılığıyla MSS'ye ithal edildiği yönündedir.[11]
Poliomyelit, merkezi sinir sisteminin bir hastalığıdır. Bununla birlikte, CD155'in çoğu veya tüm insan hücrelerinin yüzeyinde mevcut olduğuna inanılmaktadır. Bu nedenle, reseptör ekspresyonu poliovirüsün neden tercihen belirli dokuları enfekte ettiğini açıklamaz. Bu da doku tropizminin hücresel enfeksiyondan sonra belirlendiğini düşündürmektedir. Son çalışmalar, tip I interferon yanıtının (özellikle interferon alfa ve beta) hangi hücre tiplerinin poliovirüs replikasyonunu desteklediğini tanımlayan önemli bir faktör olduğunu öne sürmüştür.[54] CD155 eksprese eden (genetik mühendisliği yoluyla) ancak tip I interferon reseptörü bulunmayan farelerde, poliovirüs sadece genişletilmiş bir doku tipi repertuarında çoğalmakla kalmaz, aynı zamanda bu fareler virüs ile oral yoldan enfekte olabilir.[55]
Bağışıklık sisteminden kaçınma
[değiştir | kaynağı değiştir]
Poliovirüs bağışıklık sisteminden kaçmak için iki temel mekanizma kullanır. İlk olarak, midenin yüksek asidik koşullarında hayatta kalabilir ve virüsün konakçıya bulaşmasına ve lenfatik sistem yoluyla vücuda yayılmasına izin verir.[3] İkincisi, çok hızlı bir şekilde çoğalabildiği için virüs, bir bağışıklık yanıtı oluşturulamadan konak organları alt eder.[56] Bağlanma aşamasında ayrıntı verilirse virion yüzeyinde kanyonlar bulunan poliovirüs, kanyon tabanlarındaki ceplerde bulunan virüs bağlanma bölgelerine sahiptir. Kanyonlar antikorlar tarafından erişilemeyecek kadar dardır, bu nedenle virüs bağlanma bölgeleri konağın bağışıklık gözetiminden korunurken, viryon yüzeyinin geri kalanı konağın bağışıklık yanıtından kaçınmak için mutasyona uğrayabilir.[57]
Poliovirüse enfeksiyon yoluyla ya da çocuk felci aşısı ile bağışıklık kazanarak maruz kalan bireyler bağışıklık geliştirir. Bağışık bireylerde, poliovirüse karşı antikorlar bademciklerde ve gastrointestinal sistemde bulunur (özellikle IgA antikorları) ve poliovirüs replikasyonunu engelleyebilir; poliovirüse karşı IgG ve IgM antikorları virüsün merkezi sinir sisteminin motor nöronlarına yayılmasını önleyebilir.[33] Bir poliovirüs serotipi ile enfeksiyon diğer serotiplere karşı bağışıklık sağlamaz; ancak aynı bireyde ikinci ataklar son derece nadirdir.[58]
PVR transgenik fare
[değiştir | kaynağı değiştir]İnsanlar poliovirüsün bilinen tek doğal konakçıları olmasına rağmen, maymunlar deneysel olarak enfekte edilebilir ve poliovirüsü incelemek için uzun süredir kullanılmaktadırlar. 1990-91 yıllarında iki laboratuvar tarafından küçük bir hayvan poliomyelit modeli geliştirilmiştir. Fareler, poliovirüse karşı bir insan reseptörü (hPVR) ifade edecek şekilde tasarlandı.[59][60]
Normal farelerin aksine, transgenik poliovirüs reseptörlü (TgPVR) fareler intravenöz veya intramüsküler olarak enjekte edilen poliovirüse ve doğrudan omuriliğe veya beyne enjekte edildiğinde duyarlıdır.[61] Enfeksiyon üzerine, TgPVR fareleri insanlarda ve maymunlarda görülen poliomyelit belirtilerine benzeyen felç belirtileri gösterir ve felçli farelerin merkezi sinir sistemleri histositokimyasal olarak insanların ve maymunlarınkine benzer. İnsan poliovirüs enfeksiyonunun bu fare modelinin poliovirüs biyolojisi ve patojenitesinin anlaşılmasında çok değerli bir araç olduğu kanıtlanmıştır.[62]
Üç farklı TgPVR fare türü iyi çalışılmıştır:[63]
- TgPVR1 farelerinde, insan PVR'sini kodlayan transgen fare kromozomu 4'e dahil edilmiştir. Bu fareler transgenin en yüksek seviyelerini ve poliovirüse karşı en yüksek hassasiyeti ifade eder. TgPVR1 fareleri poliovirüse intraspinal, intraserebral, intramüsküler ve intravenöz yollarla duyarlıdır, ancak oral yolla duyarlı değildir.
- TgPVR21 fareleri insan PVR'sini kromozom 13'e dahil etmiştir. Bu fareler intraserebral yolla poliovirüs enfeksiyonuna daha az duyarlıdır, bunun nedeni muhtemelen hPVR seviyelerinin azalmış olmasıdır. TgPVR21 farelerinin intranazal inokülasyon yoluyla poliovirüs enfeksiyonuna duyarlı olduğu gösterilmiştir ve mukozal enfeksiyon modeli olarak yararlı olabilir.[64]
- TgPVR5 farelerinde, insan transgeni kromozom 12 üzerinde yer almaktadır. Bu fareler en düşük hPVR ekspresyon seviyelerini sergiler ve poliovirüs enfeksiyonuna en az duyarlı olanlardır.
Yakın zamanda dördüncü bir TgPVR fare modeli geliştirilmiştir. Bu "cPVR" fareleri, bir β-aktin promotörü tarafından yönlendirilen hPVR cDNA taşımaktadır ve intraserebral, intramüsküler ve intranazal yollarla poliovirüse duyarlı oldukları kanıtlanmıştır. Ayrıca, bu fareler intranazal aşılamadan sonra çocuk felcinin bulbar formunu geliştirebilmektedir.[64]
TgPVR faresinin geliştirilmesinin oral poliovirüs aşısı (OPV) üretimi üzerinde derin bir etkisi olmuştur. Daha önce OPV'nin güvenliğinin izlenmesi maymunlar kullanılarak yapılmak zorundaydı, çünkü sadece primatlar virüse karşı duyarlıydı. 1999 yılında Dünya Sağlık Örgütü, TgPVR faresinin poliovirüs tip-3'e karşı aşının etkinliğini değerlendirmek için alternatif bir yöntem olarak kullanılmasını onayladı. 2000 yılında fare modeli, tip-1 ve tip-2 poliovirüse karşı aşıların test edilmesi için onaylanmıştır.[65]
Klonlama ve sentez
[değiştir | kaynağı değiştir]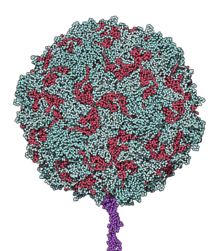
1981 yılında Racaniello ve Baltimore rekombinant DNA teknolojisini kullanarak bir hayvan RNA virüsü olan poliovirüsün ilk bulaşıcı klonunu üretmiştir. Poliovirüsün RNA genomunu kodlayan DNA, kültürlenmiş memeli hücrelerine eklenmiş ve bulaşıcı poliovirüs üretilmiştir.[66] Bulaşıcı klonun oluşturulması, poliovirüs biyolojisinin anlaşılmasını sağladı ve diğer birçok virüsün incelenmesinde kullanılan standart bir teknoloji haline geldi.
2002 yılında Stony Brook Üniversitesinden Eckard Wimmer'in grubu, poliovirüsü kimyasal kodundan sentezlemeyi başararak dünyanın ilk sentetik virüsünü üretti.[67] Bilim insanları ilk olarak poliovirüsün 7741 baz uzunluğundaki yayınlanmış RNA dizisini, DNA'nın sentezlenmesi daha kolay olduğu için bir DNA dizisine dönüştürdü. Bu DNA dizisinin kısa parçaları posta siparişiyle elde edildi ve birleştirildi. Viral genomun tamamı daha sonra bir gen sentez şirketi tarafından bir araya getirildi.
Sentezlenen DNA'ya doğal poliovirüsten ayırt edilebilmesi için on dokuz belirteç eklenmiştir. DNA'yı tekrar doğal hali olan RNA'ya dönüştürmek için enzimler kullanıldı. Daha sonra RNA'yı bir polipeptide çevirmek için başka enzimler kullanıldı ve işlevsel viral partikül üretildi. Tüm bu özenli süreç iki yıl sürdü.
Yeni basılan sentetik virüs, sentetik versiyonun hastalığa neden olup olamayacağını belirlemek için PVR transgenik farelere enjekte edildi. Sentetik virüs farelerde çoğalabildi, enfekte olabildi ve felce ya da ölüme neden olabildi. Bununla birlikte, sentetik versiyon, muhtemelen eklenen belirteçlerden biri nedeniyle orijinal virüsten 1000 ila 10.000 kat daha zayıftı.[68]
Tedaviler için modifikasyon
[değiştir | kaynağı değiştir]Poliovirüsün PVSRIPO adı verilen bir modifikasyonu, kanser için olası bir tedavi olarak erken klinik deneylerde test edilmiştir.[69][güncellenmeli]
Kaynakça
[değiştir | kaynağı değiştir]- ^ Ryan KJ, Ray CG, (Ed.) (2004). Sherris Medical Microbiology (4. bas.). McGraw Hill. ISBN 978-0-8385-8529-0.[sayfa belirt]
- ^ a b Hogle JM (2002). "Poliovirus cell entry: common structural themes in viral cell entry pathways". Annual Review of Microbiology. 56: 677-702. doi:10.1146/annurev.micro.56.012302.160757. PMC 1500891 $2. PMID 12142481.
- ^ a b c Goodsell DS (1998). The machinery of life. New York: Copernicus. ISBN 978-0-387-98273-1.[sayfa belirt]
- ^ a b Paul JR (1971). A History of Poliomyelitis. (Yale studies in the history of science and medicine). New Haven, Conn: Yale University Press. ISBN 978-0-300-01324-5.[sayfa belirt]
- ^ "Behind the picture: Rosalind Franklin and the polio model". Medical Research Council. 14 Mart 2019. 30 Ekim 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Eylül 2019.
- ^ Maddox, Brenda (2003). Rosalind Franklin: The Dark Lady of DNA. Londra: Harper Collins. s. 296. ISBN 0-00-655211-0. 14 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Mayıs 2020.
- ^ Brown, Andrew (2007). J.D. Bernal: The Sage of Science. New York: Oxford University Press. ss. 359-61. ISBN 978-0-19-920565-3.
- ^ Racaniello VR, Baltimore D (August 1981). "Molecular cloning of poliovirus cDNA and determination of the complete nucleotide sequence of the viral genome". Proceedings of the National Academy of Sciences of the United States of America. 78 (8): 4887-91. Bibcode:1981PNAS...78.4887R. doi:10.1073/pnas.78.8.4887. PMC 320284 $2. PMID 6272282.
- ^ Kitamura N, Semler BL, Rothberg PG, Larsen GR, Adler CJ, Dorner AJ, Emini EA, Hanecak R, Lee JJ, van der Werf S, Anderson CW, Wimmer E (June 1981). "Primary structure, gene organization and polypeptide expression of poliovirus RNA". Nature. 291 (5816): 547-53. Bibcode:1981Natur.291..547K. doi:10.1038/291547a0. PMID 6264310.
- ^ Hogle JM, Chow M, Filman DJ (27 Eylül 1985). "Three-dimensional structure of poliovirus at 2.9 A resolution". Science. 229 (4720): 1358-65. doi:10.1126/science.2994218. PMID 2994218.
- ^ a b c d De Jesus NH (July 2007). "Epidemics to eradication: the modern history of poliomyelitis". Virology Journal. 4 (1): 70. doi:10.1186/1743-422X-4-70. PMC 1947962 $2. PMID 17623069.
- ^ Mendelsohn CL, Wimmer E, Racaniello VR (March 1989). "Cellular receptor for poliovirus: molecular cloning, nucleotide sequence, and expression of a new member of the immunoglobulin superfamily". Cell. 56 (5): 855-65. doi:10.1016/0092-8674(89)90690-9. PMID 2538245.
- ^ a b He Y, Mueller S, Chipman PR, Bator CM, Peng X, Bowman VD, Mukhopadhyay S, Wimmer E, Kuhn RJ, Rossmann MG (April 2003). "Complexes of poliovirus serotypes with their common cellular receptor, CD155". Journal of Virology. 77 (8): 4827-35. doi:10.1128/JVI.77.8.4827-4835.2003. PMC 152153 $2. PMID 12663789.
- ^ Dunnebacke TH, Levinthal JD, Williams RC (October 1969). "Entry and release of poliovirus as observed by electron microscopy of cultured cells". Journal of Virology. 4 (4): 505-13. doi:10.1128/JVI.4.4.505-513.1969. PMC 375900 $2. PMID 4309884.
- ^ Kaplan G, Freistadt MS, Racaniello VR (October 1990). "Neutralization of poliovirus by cell receptors expressed in insect cells". Journal of Virology. 64 (10): 4697-702. doi:10.1128/JVI.64.10.4697-4702.1990. PMC 247955 $2. PMID 2168959.
- ^ Gómez Yafal A, Kaplan G, Racaniello VR, Hogle JM (November 1993). "Characterization of poliovirus conformational alteration mediated by soluble cell receptors". Virology. 197 (1): 501-05. doi:10.1006/viro.1993.1621. PMID 8212594.
- ^ a b Mueller S, Wimmer E, Cello J (August 2005). "Poliovirus and poliomyelitis: a tale of guts, brains, and an accidental event". Virus Research. 111 (2): 175-93. doi:10.1016/j.virusres.2005.04.008. PMID 15885840.
- ^ Brandenburg B, Lee LY, Lakadamyali M, Rust MJ, Zhuang X, Hogle JM (July 2007). "Imaging poliovirus entry in live cells". PLOS Biology. 5 (7): e183. doi:10.1371/journal.pbio.0050183. PMC 1914398 $2. PMID 17622193.
- ^ Attardi G, Smith J (1962). "Virus specific protein and a ribo-nucleic acid associated with ribosomes in poliovirus infected HeLa cells". Cold Spring Harbor Symposia on Quantitative Biology. 27: 271-92. doi:10.1101/SQB.1962.027.001.026. PMID 13965389.
- ^ Lozano G, Fernandez N, Martinez-Salas E (February 2016). "Modeling Three-Dimensional Structural Motifs of Viral IRES". Journal of Molecular Biology. 428 (5 Pt A): 767-76. doi:10.1016/j.jmb.2016.01.005. PMID 26778619.
- ^ Chen CY, Sarnow P (April 1995). "Initiation of protein synthesis by the eukaryotic translational apparatus on circular RNAs". Science. 268 (5209): 415-17. Bibcode:1995Sci...268..415C. doi:10.1126/science.7536344. PMID 7536344.
- ^ Pelletier J, Sonenberg N (July 1988). "Internal initiation of translation of eukaryotic mRNA directed by a sequence derived from poliovirus RNA". Nature. 334 (6180): 320-25. Bibcode:1988Natur.334..320P. doi:10.1038/334320a0. PMID 2839775.
- ^ Jang SK, Kräusslich HG, Nicklin MJ, Duke GM, Palmenberg AC, Wimmer E (August 1988). "A segment of the 5' nontranslated region of encephalomyocarditis virus RNA directs internal entry of ribosomes during in vitro translation". Journal of Virology. 62 (8): 2636-43. doi:10.1128/JVI.62.8.2636-2643.1988. PMC 253694 $2. PMID 2839690.
- ^ Carter, John; Saunders, Venetia A. (2007). Virology: Principles and Applications. John Wiley & Sons. s. 4. ISBN 978-0-470-02386-0.
- ^ a b Carter, John; Saunders, Venetia A. (2007). Virology: Principles and Applications. John Wiley & Sons. s. 165. ISBN 978-0-470-02386-0. 14 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 Ekim 2016.
- ^ Harper, David R. (2012). Viruses: Biology, Applications, and Control. The United States of America: Garland Science. ISBN 978-0-8153-4150-5.[sayfa belirt]
- ^ "Poliomyelitis". Brown University. 22 Şubat 2007 tarihinde kaynağından arşivlendi.
- ^ Murray KE, Barton DJ (April 2003). "Poliovirus CRE-dependent VPg uridylylation is required for positive-strand RNA synthesis but not for negative-strand RNA synthesis". Journal of Virology. 77 (8): 4739-50. doi:10.1128/JVI.77.8.4739-4750.2003. PMC 152113 $2. PMID 12663781.
- ^ Louten, Jennifer (2016). "Poliovirus". Essential Human Virology. Elsevier. ss. 257-71. doi:10.1016/b978-0-12-800947-5.00014-4. ISBN 978-0-12-800947-5.
- ^ Goodfellow IG, Kerrigan D, Evans DJ (January 2003). "Structure and function analysis of the poliovirus cis-acting replication element (CRE)". RNA. 9 (1): 124-37. doi:10.1261/rna.2950603. PMC 1370376 $2. PMID 12554882.
- ^ Carter, John; Saunders, Venetia A. (2007). Virology: Principles and Applications. John Wiley & Sons. ss. 161, 165. ISBN 978-0-470-02386-0. 14 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 Ekim 2016.
- ^ Carter, John; Saunders, Venetia A. (2007). Virology: Principles and Applications. John Wiley & Sons. s. 166. ISBN 978-0-470-02386-0.
- ^ a b c d Kew OM, Sutter RW, de Gourville EM, Dowdle WR, Pallansch MA (2005). "Vaccine-derived polioviruses and the endgame strategy for global polio eradication". Annual Review of Microbiology. 59: 587-635. doi:10.1146/annurev.micro.58.030603.123625. PMID 16153180. 9 Temmuz 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Ekim 2018.
- ^ a b Drake JW (August 1958). "Interference and multiplicity reactivation in polioviruses". Virology. 6 (1): 244-64. doi:10.1016/0042-6822(58)90073-4. PMID 13581529.
- ^ Bernstein H, Bernstein C, Michod RE (January 2018). "Sex in microbial pathogens". Infection, Genetics and Evolution. 57: 8-25. doi:10.1016/j.meegid.2017.10.024. PMID 29111273.
- ^ Barr JN, Fearns R (June 2010). "How RNA viruses maintain their genome integrity". The Journal of General Virology. 91 (Pt 6): 1373-87. doi:10.1099/vir.0.020818-0. PMID 20335491.
- ^ Jiang P, Faase JA, Toyoda H, Paul A, Wimmer E, Gorbalenya AE (May 2007). "Evidence for emergence of diverse polioviruses from C-cluster coxsackie A viruses and implications for global poliovirus eradication". Proceedings of the National Academy of Sciences of the United States of America. 104 (22): 9457-62. Bibcode:2007PNAS..104.9457J. doi:10.1073/pnas.0700451104. PMC 1874223 $2. PMID 17517601.
- ^ Jorba J, Campagnoli R, De L, Kew O (May 2008). "Calibration of multiple poliovirus molecular clocks covering an extended evolutionary range". Journal of Virology. 82 (9): 4429-40. doi:10.1128/JVI.02354-07. PMC 2293050 $2. PMID 18287242.
- ^ Rothberg PG, Wimmer E (December 1981). "Mononucleotide and dinucleotide frequencies, and codon usage in poliovirion RNA". Nucleic Acids Research. 9 (23): 6221-29. doi:10.1093/nar/9.23.6221. PMC 327599 $2. PMID 6275352.
- ^ Zhang J, Wang M, Liu WQ, Zhou JH, Chen HT, Ma LN, Ding YZ, Gu YX, Liu YS (March 2011). "Analysis of codon usage and nucleotide composition bias in polioviruses". Virology Journal. 8: 146. doi:10.1186/1743-422X-8-146. PMC 3079669 $2. PMID 21450075.
- ^ "Global eradication of wild poliovirus type 2 declared". Global Polio Eradication Initiative. 20 Eylül 2015. 28 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Eylül 2015.
- ^ "GPEI-Two out of three wild poliovirus strains eradicated" (İngilizce). 7 Kasım 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Kasım 2019.
- ^ Carstens EB, Ball LA (July 2009). "Ratification vote on taxonomic proposals to the International Committee on Taxonomy of Viruses (2008)". Archives of Virology. 154 (7): 1181-88. doi:10.1007/s00705-009-0400-2. PMC 7086627 $2. PMID 19495937.
- ^ Mueller S, Wimmer E (August 2003). "Recruitment of nectin-3 to cell-cell junctions through trans-heterophilic interaction with CD155, a vitronectin and poliovirus receptor that localizes to alpha(v)beta3 integrin-containing membrane microdomains". The Journal of Biological Chemistry. 278 (33): 31251-60. doi:10.1074/jbc.M304166200. PMID 12759359.
- ^ Suzuki Y (May 2006). "Ancient positive selection on CD155 as a possible cause for susceptibility to poliovirus infection in simians". Gene. 373: 16-22. doi:10.1016/j.gene.2005.12.016. PMID 16500041.
- ^ Bodian D, Horstmann DH (1969). Polioviruse. Philadelphia, Penn: Lippincott. ss. 430-73.
- ^ Sabin AB (June 1956). "Pathogenesis of poliomyelitis; reappraisal in the light of new data". Science. 123 (3209): 1151-57. Bibcode:1956Sci...123.1151S. doi:10.1126/science.123.3209.1151. PMID 13337331.
- ^ Carter, John B.; Saunders, Venetia A. (2007). Virology: Principles and Applications (1. bas.). Chichester, England: John Wiley & Sons. ISBN 978-0-470-02386-0. OCLC 124160564.[sayfa belirt]
- ^ eMedicine'de Acute PoliomyelitiseMedicine'de Pediatric Poliomyelitis
- ^ Yang WX, Terasaki T, Shiroki K, Ohka S, Aoki J, Tanabe S, Nomura T, Terada E, Sugiyama Y, Nomoto A (March 1997). "Efficient delivery of circulating poliovirus to the central nervous system independently of poliovirus receptor". Virology. 229 (2): 421-28. doi:10.1006/viro.1997.8450. PMID 9126254.
- ^ Ohka S, Yang WX, Terada E, Iwasaki K, Nomoto A (October 1998). "Retrograde transport of intact poliovirus through the axon via the fast transport system". Virology. 250 (1): 67-75. doi:10.1006/viro.1998.9360. PMID 9770421.
- ^ Ren R, Racaniello VR (October 1992). "Poliovirus spreads from muscle to the central nervous system by neural pathways". The Journal of Infectious Diseases. 166 (4): 747-52. doi:10.1093/infdis/166.4.747. PMID 1326581.
- ^ Lancaster KZ, Pfeiffer JK (March 2010). Gale Jr M (Ed.). "Limited trafficking of a neurotropic virus through inefficient retrograde axonal transport and the type I interferon response". PLOS Pathogens. 6 (3): e1000791. doi:10.1371/journal.ppat.1000791. PMC 2832671 $2. PMID 20221252.
- ^ Ida-Hosonuma M, Iwasaki T, Yoshikawa T, Nagata N, Sato Y, Sata T, Yoneyama M, Fujita T, Taya C, Yonekawa H, Koike S (April 2005). "The alpha/beta interferon response controls tissue tropism and pathogenicity of poliovirus". Journal of Virology. 79 (7): 4460-69. doi:10.1128/JVI.79.7.4460-4469.2005. PMC 1061561 $2. PMID 15767446.
- ^ Ohka S, Igarashi H, Nagata N, Sakai M, Koike S, Nochi T, Kiyono H, Nomoto A (August 2007). "Establishment of a poliovirus oral infection system in human poliovirus receptor-expressing transgenic mice that are deficient in alpha/beta interferon receptor". Journal of Virology. 81 (15): 7902-12. doi:10.1128/JVI.02675-06. PMC 1951287 $2. PMID 17507470.
- ^ Racaniello VR (January 2006). "One hundred years of poliovirus pathogenesis". Virology. 344 (1): 9-16. doi:10.1016/j.virol.2005.09.015. PMID 16364730.
- ^ Carter, John B.; Saunders, Venetia A. (2007). Virology: Principles and Applications. Liverpool John Moores University, UK: John Wiley & Sons. ISBN 978-0-470-02386-0.[sayfa belirt]
- ^ "WHO | Poliomyelitis". 17 Mayıs 2014 tarihinde kaynağından arşivlendi.
- ^ Koike S, Taya C, Kurata T, Abe S, Ise I, Yonekawa H, Nomoto A (February 1991). "Transgenic mice susceptible to poliovirus". Proceedings of the National Academy of Sciences of the United States of America. 88 (3): 951-55. Bibcode:1991PNAS...88..951K. doi:10.1073/pnas.88.3.951. PMC 50932 $2. PMID 1846972.
- ^ Ren RB, Costantini F, Gorgacz EJ, Lee JJ, Racaniello VR (October 1990). "Transgenic mice expressing a human poliovirus receptor: a new model for poliomyelitis". Cell. 63 (2): 353-62. doi:10.1016/0092-8674(90)90168-E. PMID 2170026.
- ^ Horie H, Koike S, Kurata T, Sato-Yoshida Y, Ise I, Ota Y, Abe S, Hioki K, Kato H, Taya C (February 1994). "Transgenic mice carrying the human poliovirus receptor: new animal models for study of poliovirus neurovirulence". Journal of Virology. 68 (2): 681-88. doi:10.1128/JVI.68.2.681-688.1994. PMC 236503 $2. PMID 8289371.
- ^ Ohka S, Nomoto A (October 2001). "Recent insights into poliovirus pathogenesis". Trends in Microbiology. 9 (10): 501-06. doi:10.1016/S0966-842X(01)02200-4. PMID 11597452.
- ^ Koike S, Taya C, Aoki J, Matsuda Y, Ise I, Takeda H, Matsuzaki T, Amanuma H, Yonekawa H, Nomoto A (1994). "Characterization of three different transgenic mouse lines that carry human poliovirus receptor gene--influence of the transgene expression on pathogenesis". Archives of Virology. 139 (3–4): 351-63. doi:10.1007/BF01310797. PMID 7832641.
- ^ a b Nagata N, Iwasaki T, Ami Y, Sato Y, Hatano I, Harashima A, Suzaki Y, Yoshii T, Hashikawa T, Sata T, Horiuchi Y, Koike S, Kurata T, Nomoto A (March 2004). "A poliomyelitis model through mucosal infection in transgenic mice bearing human poliovirus receptor, TgPVR21". Virology. 321 (1): 87-100. doi:10.1016/j.virol.2003.12.008. PMID 15033568.
- ^ Dragunsky E, Nomura T, Karpinski K, Furesz J, Wood DJ, Pervikov Y, Abe S, Kurata T, Vanloocke O, Karganova G, Taffs R, Heath A, Ivshina A, Levenbook I (2003). "Transgenic mice as an alternative to monkeys for neurovirulence testing of live oral poliovirus vaccine: validation by a WHO collaborative study". Bulletin of the World Health Organization. 81 (4): 251-60. PMC 2572431 $2. PMID 12764491. 24 Şubat 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 1 Nisan 2022.
- ^ Racaniello VR, Baltimore D (November 1981). "Cloned poliovirus complementary DNA is infectious in mammalian cells". Science. 214 (4523): 916-19. Bibcode:1981Sci...214..916R. doi:10.1126/science.6272391. PMID 6272391.
- ^ Cello J, Paul AV, Wimmer E (August 2002). "Chemical synthesis of poliovirus cDNA: generation of infectious virus in the absence of natural template". Science. 297 (5583): 1016-18. Bibcode:2002Sci...297.1016C. doi:10.1126/science.1072266. PMID 12114528.
- ^ Couzin J (July 2002). "Virology. Active poliovirus baked from scratch". Science. 297 (5579): 174-75. doi:10.1126/science.297.5579.174b. PMID 12114601. 9 Ağustos 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Aralık 2019.
- ^ Brown MC, Dobrikova EY, Dobrikov MI, Walton RW, Gemberling SL, Nair SK, Desjardins A, Sampson JH, Friedman HS, Friedman AH, Tyler DS, Bigner DD, Gromeier M (November 2014). "Oncolytic polio virotherapy of cancer". Cancer. 120 (21): 3277-86. doi:10.1002/cncr.28862. PMC 4205207 $2. PMID 24939611.
Dış bağlantılar
[değiştir | kaynağı değiştir]- ICTVdb virüs sınıflandırması 2006
- Home of Picornaviruses (türlerin, serotiplerin ve önerilen değişikliklerin son güncellemeleri) 4 Kasım 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- Goodsell, David. "Poliovirus and Rhinovirus". August 2001 Molecule of the Month. 3 Mart 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ocak 2010.
- EM Veri Bankasında (EMDB) arşivlenen Poliovirüsün 3D makromoleküler yapıları
- "Human poliovirus 1". NCBI Taxonomy Browser. 12080. 10 Mayıs 2024 tarihinde kaynağından arşivlendi.
- "Human poliovirus 3". NCBI Taxonomy Browser. 12086. 11 Kasım 2020 tarihinde kaynağından arşivlendi.
