Bor
Bor (bắt nguồn từ từ tiếng Pháp bore /bɔʁ/)[6] là một nguyên tố hóa học trong bảng tuần hoàn nguyên tố có ký hiệu B và số hiệu nguyên tử bằng 5, nguyên tử khối bằng 11.
| Bor, 5B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất chung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tên, ký hiệu | Bor, B | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phiên âm | /ˈbɔːrɒn/ (BOR-on) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hình dạng | Đen nâu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bor trong bảng tuần hoàn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số nguyên tử (Z) | 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Khối lượng nguyên tử chuẩn (±) (Ar) | 10,811(7) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phân loại | á kim | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhóm, phân lớp | 13, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chu kỳ | Chu kỳ 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu hình electron | [He] 2s2 2p1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
mỗi lớp | 2, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất vật lý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Màu sắc | Đen nâu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái vật chất | Chất rắn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ nóng chảy | 2349 K (2076 °C, 3769 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ sôi | 4200 K (3927 °C, 7101 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ ở thể lỏng | ở nhiệt độ nóng chảy: 2,08 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt lượng nóng chảy | 50,2 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt bay hơi | 480 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt dung | 11,087 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Áp suất hơi
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất nguyên tử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái oxy hóa | 3, 2, 1[1], 0, -1, -5 Acid nhẹ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ âm điện | 2.04 (Thang Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Năng lượng ion hóa | Thứ nhất: 800,6 kJ·mol−1 Thứ hai: 2427,1 kJ·mol−1 Thứ ba: 3659,7 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính cộng hoá trị | thực nghiệm: 90 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính liên kết cộng hóa trị | 84±3 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính van der Waals | 192 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thông tin khác | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu trúc tinh thể | 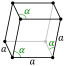 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vận tốc âm thanh | que mỏng: 16,200 m·s−1 (ở 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ giãn nở nhiệt | (ß form) 5–7 [2] µm·m−1·K−1 (ở 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | 27.4 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điện trở suất | ở 20 °C: ~106 Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất từ | Nghịch từ[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Mohs | ~9,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số đăng ký CAS | 7440-42-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đồng vị ổn định nhất | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bài chính: Đồng vị của Bor | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Thuộc tính
sửaBo là nguyên tố thiếu hụt điện tử, có quỹ đạo p trống. Các hợp chất của bo thông thường có tính chất như các acid Lewis, sẵn sàng liên kết với các chất giàu điện tử.
Các đặc trưng quang học của nguyên tố này bao gồm khả năng truyền tia hồng ngoại. Ở nhiệt độ phòng Bo là một chất dẫn điện kém nhưng là chất dẫn điện tốt ở nhiệt độ cao.
Bo là nguyên tố có sức chịu kéo giãn cao nhất.
Nitride bo (BN) có thể sử dụng để chế tạo vật liệu có độ cứng như kim cương. Nó có tính chất của một chất cách điện nhưng dẫn nhiệt giống như kim loại. Nguyên tố này cũng có các độ nhớt giống như than chì. Bo cũng giống như cacbon về khả năng của nó tạo ra các liên kết phân tử cộng hóa trị ổn định.
Là một nguyên tố á kim hóa trị +3, bo xuất hiện chủ yếu trong quặng borax. Có hai dạng thù hình của bo; bo vô định hình là chất bột màu nâu, nhưng bo kim loại thì có màu đen. Dạng thù hình kim loại rất cứng (9,3 trong thangon Mohs) và là chất dẫn điện kém ở nhiệt độ phòng. Không tìm thấy bo tự do trong tự nhiên.
Ứng dụng
sửaHợp chất có giá trị kinh tế nhất của bo là tetraborat decahydrat natri Na2B4O7·10H2O, hay borax, được sử dụng để làm lớp vỏ cách nhiệt cho cáp quang hay chất tẩy trắng perborat natri. Các ứng dụng khác là:
- Vì ngọn lửa màu lục đặc biệt của nó, bo vô định hình được sử dụng trong pháo hoa.
- Acid boric là hợp chất quan trọng sử dụng trong các sản phẩm may mặc.
- Các hợp chất của bo được sử dụng nhiều trong tổng hợp các chất hữu cơ và sản xuất các thủy tinh borosilicat.
- Các hợp chất khác được sử dụng như là chất bảo quản gỗ được ưa thích do có độc tính thấp.
- Bo10 được sử dụng để hỗ trợ kiểm soát của các lò phản ứng hạt nhân, là lá chắn chống bức xạ và phát hiện neutron.
- Các sợi bo là vật liệu nhẹ có độ cứng cao, được sử dụng chủ yếu trong các kết cấu tàu vũ trụ.
- Borohydrit natri (NaBH4), là chất khử hóa học thông dụng, được sử dụng (ví dụ) trong khử các aldehyde và keton thành rượu.
- Các hợp chất bo được sử dụng như thành phần trong các màng thấm đường, phần tử nhạy cacbonhiđrat và tiếp hợp sinh học. Các ứng dụng sinh học được nghiên cứu bao gồm liệu pháp giữ neutron bằng bo và phân phối thuốc trong cơ thể. Các hợp chất khác của bo có hứa hẹn trong điều trị bệnh viêm khớp, ung thư..
Hydride bo là một chất bị oxy hóa dễ dàng giải phóng ra một lượng đáng kể năng lượng. Vì thế nó được nghiên cứu để sử dụng làm nhiên liệu cho tên lửa.
Lịch sử
sửaCác hợp chất của bo (tiếng Ả Rập buraq từ tiếng Ba Tư burah) đã được biết đến từ hàng nghìn năm trước. Ở Ai Cập cổ đại, việc ướp xác phụ thuộc vào quặng được biết đến như là natron, nó chứa muối borat cũng như một số muối phổ biến khác. Các loại men sứ từ borax đã được sử dụng ở Trung Quốc từ năm 300, các hợp chất của bo được sử dụng trong sản xuất thủy tinh ở La Mã cổ đại.
Nguyên tố này được phân lập năm 1808 bởi Sir Humphry Davy, Joseph Louis Gay-Lussac và Louis Jacques Thénard, với độ tinh khiết khoảng 50%. Những người này không biết chất tạo thành như là một nguyên tố. Năm 1824 Jöns Jakob Berzelius đã xác nhận bo như là một nguyên tố; ông gọi nó là boron, một từ tiếng Latin có nguồn gốc là burah trong tiếng Ba Tư. Bo nguyên chất được sản xuất lần đầu tiên bởi nhà hóa học người Mỹ W. Weintraub năm 1909.
Sự phổ biến
sửaMỹ và Thổ Nhĩ Kỳ là hai nước sản xuất Bo lớn nhất thế giới. Bo trong tự nhiên tìm thấy ở dạng muối borat, acid boric, colemanit, kernit, ulexit. Acid boric đôi khi tìm thấy trong nước suối có nguồn gốc núi lửa. Ulexit là khoáng chất borat tự nhiên có thuộc tính của cáp quang học.
Nguồn có giá trị kinh tế quan trọng là quặng rasorit (kernit) và tincal (quặng borax), cả hai được tìm thấy ở sa mạc Mojave (California) (với borax là khoáng chất chủ yếu). Thổ Nhĩ Kỳ là nơi mà các khoáng chất borax cũng được tìm thấy nhiều.
Bo tinh khiết không dễ điều chế. Phương pháp sớm nhất được sử dụng là khử oxide bo với các kim loại như magiê hay nhôm. Tuy nhiên sản phẩm thu được hầu như có chứa borua kim loại. Bo nguyên chất có thể được điều chế bằng việc khử các hợp chất của bo với các halôgen dễ bay hơi bằng hiđrô ở nhiệt độ cao.
Năm 1997 bo kết tinh (99% nguyên chất) có giá khoảng USD 5 cho 1 gam và bo vô định hình giá USD 2 cho 1 gam.
Đồng vị
sửaBo có 2 đồng vị tự nhiên ổn định là 11B (80,1%) và 10B (19,9%). Sự sai khác về khối lượng tạo ra một khoảng rộng của các giá trị δB-11 trong các loại nước tự nhiên, dao động từ -16 đến +59. Có 13 đồng vị đã biết của bo, chu kỳ bán rã ngắn nhất là 7B, nó phân rã bởi bức xạ proton và phóng xạ alpha. Chu kỳ bán rã của nó là 3,26500x10−22 s. Sự phân đoạn đồng vị của bo được kiểm soát bởi các phản ứng trao đổi của các chất B(OH)3 và B(OH)4. Các đồng vị của bo cũng phân đoạn trong sự kết tinh khoáng chất, trong các thay đổi pha của H2O trong hệ thống thủy phân, cũng như trong phong hóa các loại đá bởi nước. Hiệu ứng cuối cùng chuyển đổi các ion B10(OH)4 trong đất sét thành B11(OH)3 có thể là nguyên nhân của lượng lớn B11 trong nước biển, điều này có liên quan tới các lớp vỏ của các đại dương và lục địa.
Cảnh báo
sửaBo nguyên tố và các borat là không độc vì thế không có yêu cầu đặc biệt nào khi làm việc với chúng. Tuy nhiên, một số hợp chất chứa hydro của bo là độc và có yêu cầu đặc biệt khi tiếp xúc. Natri orthoborat có thể gây hại cho gan.
Xem thêm
sửaTham khảo
sửa- ^ Zhang, K.Q.; Guo, B.; Braun, V.; Dulick, M.; Bernath, P.F. (1995). “Infrared Emission Spectroscopy of BF and AIF” (PDF). J. Molecular Spectroscopy. 170: 82. doi:10.1006/jmsp.1995.1058. Bản gốc (PDF) lưu trữ ngày 11 tháng 1 năm 2012. Truy cập ngày 13 tháng 7 năm 2011.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Holcombe Jr., C. E.; Smith, D. D.; Lorc, J. D.; Duerlesen, W. K.; Carpenter; D. A. (tháng 10 năm 1973). “Physical-Chemical Properties of beta-Rhombohedral Boron”. High Temp. Sci. 5 (5): 349–57.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Lide, David R. (ed.) (2000). Magnetic susceptibility of the elements and inorganic compounds, in Handbook of Chemistry and Physics (PDF). CRC press. ISBN 0849304814. Bản gốc (PDF) lưu trữ ngày 12 tháng 1 năm 2012. Truy cập ngày 13 tháng 7 năm 2011.Quản lý CS1: văn bản dư: danh sách tác giả (liên kết)
- ^ a b “Atomic Weights and Isotopic Compositions for All Elements”. National Institute of Standards and Technology. Truy cập ngày 21 tháng 9 năm 2008.
- ^ Szegedi, S.; Váradi, M.; Buczkó, Cs. M.; Várnagy, M.; Sztaricskai, T. (1990). “Determination of boron in glass by neutron transmission method”. Journal of Radioanalytical and Nuclear Chemistry Letters. 146: 177. doi:10.1007/BF02165219.
- ^ Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d’origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 63.
Liên kết ngoài
sửa- Bor tại Từ điển bách khoa Việt Nam
- Los Alamos National Laboratory – Boron Lưu trữ 2006-02-04 tại Wayback Machine
- Boron (chemical element) tại Encyclopædia Britannica (tiếng Anh)
| Boron | Nhôm | Gali | Indi | Tali | Nihoni |
|---|---|---|---|---|---|
| (chất phóng xạ) |