Cyclo-octatetraeen
| Cyclo-octatetraeen | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
| |||||
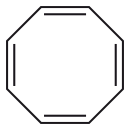
Structuurformule van cyclo-octatetraeen
| |||||
| |||||
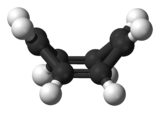
Molecuulmodel van cyclo-octatetraeen
| |||||

| |||||
Ruimtelijke structuurformule van cyclo-octatetraeen (de zogenaamde badkuipconformatie)
| |||||
| Algemeen | |||||
| Molecuulformule | C8H8 | ||||
| IUPAC-naam | 1,3,5,7-cyclo-octatetraeen | ||||
| Andere namen | COT, [8]-annuleen | ||||
| Molmassa | 104,15 g/mol | ||||
| SMILES | C1=C/C=C\C=C/C=C\1
| ||||
| CAS-nummer | 629-20-9 | ||||
| Wikidata | Q900926 | ||||
| Beschrijving | Heldere gele vloeistof | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H225 - H304 - H315 - H319 - H335 | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P210 - P261 - P301+P310 - P305+P351+P338 - P331 | ||||
| Fysische eigenschappen | |||||
| Aggregatietoestand | vloeibaar | ||||
| Kleur | geel | ||||
| Dichtheid | 0,925 g/cm³ | ||||
| Smeltpunt | −4 °C | ||||
| Kookpunt | 142 °C | ||||
| Vlampunt | −11 °C | ||||
| Zelfontbrandings- temperatuur | 561 °C | ||||
| Onoplosbaar in | water | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
1,3,5,7-cyclo-octatetraeen, doorgaans afgekort tot cyclo-octatetraeen of COT, is een onverzadigd derivaat van cyclo-octaan met als brutoformule C8H8. In de rij van monocyclische geconjugeerde systemen (de annulenen) wordt het ook aangeduid als [8]annuleen. De meervoudig onverzadigde koolwaterstof komt bij kamertemperatuur voor als een kleurloze tot lichtgele ontvlambare olieachtige vloeistof.
In tegenstelling tot benzeen (C6H6) is cyclo-octatetraeen niet aromatisch. De reactiviteit komt overeen met die van een gewone meervoudig onverzadigde verbinding: zo kunnen additiereacties gewoon uitgevoerd worden.
Geschiedenis
[bewerken | brontekst bewerken]Cyclo-octatetraeen werd voor het eerst in 1905 gesynthetiseerd door Richard Willstätter door middel van successieve Hofmann-eliminaties:[1][2]
De door Willstätter verwachte aromaticiteit werd niet aangetroffen. Tussen 1939 en 1943 heeft een aantal Amerikaanse onderzoekers tevergeefs geprobeerd cyclo-octatetraeen te synthetiseren. Als verklaring voor de mislukking werd aangevoerd dat Willstätter niet cyclo-octatetraeen, maar een isomeer ervan, styreen gemaakt had. In zijn autobiografie merkte Willstätter op dat de reductie van de door hem gemaakte verbinding tot cyclo-octaan (een onmogelijke reactie voor styreen) voor de Amerikanen blijkbaar geen probleem was. In 1947 werd de synthese van cyclo-octatetraeen door Walter Reppe via een andere route (uitgaande van ethyn, in aanwezigheid van een warm mengsel van nikkelcyanide en calciumcarbide) gerealiseerd, waarmee het oorspronkelijke werk van Willstätter bevestigd werd:[3]
De oorspronkelijke synthese van Richard Willstätter gaf een relatief lage opbrengst. Reppes synthese van cyclo-octatetraeen, startend vanuit ethyn, was met bijna 90% veel beter.[3]
Structuur en eigenschappen
[bewerken | brontekst bewerken]Al vroeg was aangetoond dat cyclo-octatetraeen geen aromaticiteit vertoonde,[4] maar aan de andere kant wezen elektrondiffractie-experimenten in de richting van identieke bindingen tussen de koolstofatomen.[5] Röntgendiffractie, uitgevoerd door H.S. Kaufman, maakte echter duidelijk dat er twee verschillende koolstof-koolstof-afstanden in cyclo-octatetraeen voorkomen.[6] Dit resultaat toonde ondubbelzinnig aan dat cyclo-octatetraeen een annuleen is met gefixeerde, alternerende enkele en dubbele bindingen. De standaardvorm van cyclo-octatetraeen is een niet-vlakke, badkuipachtige vorm, met hoeken van 126,1° tussen de koolstofatomen. De hoek tussen de dubbele binding en het waterstofatoom bedraagt 117,6°.[7]
Reacties
[bewerken | brontekst bewerken]Omdat cyclo-octatetraeen instabiel is en makkelijk explosieve peroxiden vormt, wordt vaak een kleine hoeveelheid hydrochinon aan commercieel verkrijgbare preparaten toegevoegd. Bij het openen van een recipiënt dient eerst te worden gecontroleerd op aanwezigheid van peroxiden. Witte kristallen rond de hals van de fles wijzen op de aanwezigheid van deze peroxiden. Zij kunnen bij mechanische verstoring exploderen.
De dubbele bindingen in cyclo-octatetraeen vertonen eenzelfde reactiviteit als die in alkenen. Mono- en polyepoxiden kunnen eenvoudig door reactie met peroxycarbonzuren of dimethyldioxiraan bereid worden. Een aantal additiereacties is ook beschreven. Via ringopeningpolymerisatie zijn uit alkylgesubstitueerd cyclo-octatetraeen stabiele polyacetylenen bereid, die potentiële organische geleiders zijn.[8] cyclo-octatetraeen en derivaten zijn gebruikt als liganden in metaalcomplexen en sandwichverbindingen.
Cyclo-octatetraenide-anion
[bewerken | brontekst bewerken]
Cyclo-octatetraeen reageert snel met metallisch kalium tot het zout K2COT. Hierin komt het dianion C8H82− voor.[9][10] Het dianion is vlak en aromatisch, omdat het aantal elektronen in het π-systeem 10 bedraagt. Hiermee wordt voldaan aan de regel van Hückel.
Cyclo-octatetraeen vormt complexen met een aantal metalen, waaronder yttrium en lanthaniden. Eéndimensionale Eu-COT-sandwichverbindingen worden als nanovezels gebruikt.[11] De sandwichverbindingen U(COT)2 of uranoceen en Fe(COT)2 zijn bekend en beschreven.
Als Fe(COT)2 vijf dagen in een mengsel van tolueen, DMSO en 1,2-dimethoxyethaan gerefluxed wordt, ontstaat magnetiet en kristallijne koolstof waarin ook nanotubes voorkomen.[12]
Omdat cyclo-octatetraeen van zijn badkuipvorm overgaat in een vlakke vorm bij de opname van elektronen zou de verbinding in principe gebruikt kunnen worden als spiervervanger. Voor dit soort toepassingen zou cyclo-octatetraeen gekoppeld moeten worden aan de keten van een geleidend polymeer waarmee de elektronen aan- en afgevoerd zouden kunnen worden.[13]
Voorkomen in de natuur
[bewerken | brontekst bewerken]Cyclo-octatetraeen is geïsoleerd uit sommige schimmels.[14]
Zie ook
[bewerken | brontekst bewerken]Externe link
[bewerken | brontekst bewerken]- ↑ Mason, S. "The Science and Humanism of Linus Pauling (1901-1994)", Chemical Society Reviews 26, 1 (February 1997).
- ↑ Richard Willstätter, Ernst Waser (1911). Über Cyclo-octatetraen. Berichte der deutschen chemischen Gesellschaft 44 (3): 3423–3445. DOI: 10.1002/cber.191104403216.
- ↑ a b Walter Reppe, Otto Schlichting, Karl Klager, Tim Toepel (1948). Cyclisierende Polymerisation von Acetylen I Über Cyclooctatetraen. Justus Liebigs Annalen der Chemie 560 (1): 1–92. DOI: 10.1002/jlac.19485600102.
- ↑ Johnson, A.W., Sci. Progress; 506; 1947; 35.
- ↑ Bastiensen, O.; Hassel, O.; Langseth, A. (1947). The ‘Octa-Benzene’, Cyclo-octatetraene (C8H8). Nature 160 (4056): 128. DOI: 10.1038/160128a0.
- ↑ Kaufman, H. S.; Fankuchen, I.; Mark, H. (1948). Structure of Cyclo-octatetraene. Nature 161 (4083): 165. DOI: 10.1038/161165a0.
- ↑ Thomas, P. M.; Weber, A. (1978). High resolution Raman spectroscopy of gases with laser sources. XIII - the pure rotational spectra of 1,3,5,7-cyclooctatetraene and 1,5-cyclooctadiene. Journal of Raman Spectroscopy 7 (6): 353–357. DOI: 10.1002/jrs.1250070614.
- ↑ U.S. Patent 5198153
- ↑ Thomas J. Katz (1960) - The cyclooctatetraenyl dianion, J. Am. Chem. Soc., 82 (14), pp. 3784-3785
- ↑ G. Connors, X. Wu & A.J. Fry (2007) - Experimental/Computational Study of the Electrochemical Oxidation of Cyclooctatetraene in Protic Media. Solvent Effects, J. Am. Chem. Soc.
- ↑ JST Nanostructed Materials Project Highlights- Prof. Nakajima's Presentation
- ↑ Crystalline Graphite from an Organometallic Solution-Phase Reaction Erich C. Walter, Tobias Beetz, Matthew Y. Sfeir, Louis E. Brus, and Michael L. Steigerwald J. Am. Chem. Soc.; 2006; 128(49) pp 15590 - 15591; (Communication) DOI: 10.1021/ja0666203
- ↑ UCR Fiat Lux: Muscle building - UCR researchers hope to create artificial muscles
- ↑ Stinson, M.; Ezra, D.; Hess, W. M.; Sears, J.; Strobel, G. “An endophytic Gliocladium sp. of Eucryphia cordifolia producing selective volatile antimicrobial compounds” Plant Science 2003, volume 165, pp. 913-922. DOI:10.1016/S0168-9452(03)00299-1





