Alkaner
Alkaner er hydrokarboner, det vil si at de er molekyler som består av bare hydrogen og karbon. De er også mettede forbindelser, altså forbindelser som bare har enkeltbindinger mellom karbonatomene og derfor ikke opptar hydrogen eller andre atomer ved enkle addisjonsreaksjoner, det vil si reaksjoner hvor to molekyler binder seg sammen til ett molekyl. De kan bestå av et eller flere karbonatomer i en rekke, noe som kalles alifatiske forbindelser. Generell formel for alkaner er C n H 2 n + 2.
Den enkleste alkanen er metan med ett karbonatom. Den neste i rekka er etan, med to karbonatomer. Antallet karbonatomer som kan bindes sammen på denne måten er nesten uendelig. Alkaner ligner på alkener, som har minst en dobbelbinding; og alkyner, som har minst en trippelbinding. Alkaner er også kjent under navnet parafiner, det kan skape forvekslinger med andre forbindelser med samme navn.
Oversikt
-
Metan C H 4
-
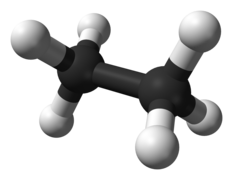
Etan C 2 H 6
-
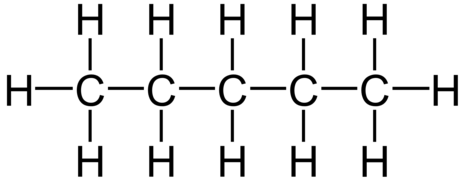
Pentan C 5 H 12
-
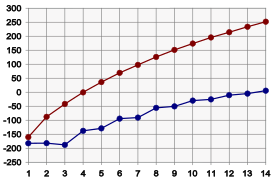
Smeltepunkt (blå linje) og kokepunkt (rød linje) for de 14 første alkanene.
Alkaner er hydrokarboner som er alifatiske, det vil si at de ikke er ordnet i en ringstruktur (sykliske). Strukturen kan være med eller uten grener.[1] De er mettede forbindelser, noe som betyr at de bare har enkeltbindinger mellom karbonatomene.[2] De enkleste alkanene er metan, som har ett karbonatom og fire hydrogenatomer (C H 4) og etan, som har to karbonatomer og seks hydrogenatomer (C 2 H 6)
Alle molekylene lages på den generelle formelen C n H 2 n + 2.[1] De fire første har egennavn, videre oppover brukes greske tall som forstavelse og -an som ending, for eksempel: penta, «fem», blir pentan, med en kjede som inneholder fem karbonatomer (C 5 H 12 )
Isomeri
Når en alkan har mer enn tre karbonatomer, kan det dannes sidegrener. Disse kalles isomerer. Alkaner hvor alle karbonatomene står på rekke kalles ofte normalalkaner. Antallet isomerer øker kraftig med antallet karbonatomer. De ti første alkanene har dette antallet isomerer:
- C1: 1 isomer
- C2: 1 isomer
- C3: 1 isomer
- C4: 2 isomerer
- C5: 3 isomerer
- C6: 5 isomerer
- C7: 9 isomerer
- C8: 18 isomerer
- C9: 35 isomerer
- C10: 75 isomerer
I tillegg til disse isomerene finnes det også sykliske forbindelser som ikke er regnet med her.
Referanser
- ^ a b IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Samlet av A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). Nettversjon (2019-) opprettet av S. J. Chalk. ISBN 0-9678550-9-8. Doi: 10.1351/goldbook.a00222
- ^ mettede forbindelser i Store norske leksikon på snl.no. Besøkt den 26. oktober 2021
Litteratur
- Klein, David R. (2012). Organic Chemistry. Hoboken, N.J. John Wiley. ISBN 9780471756149.
- Bruice, Paula Yurkanis (2010). Essential Organic Chemistry (2 utg.). Boston. Prentice Hall. ISBN 9780321644169.
- McMurry, John; McMurry, Susan (2012). Organic Chemistry (8 utg.). Belmont, CA. Brooks/Cole. ISBN 0840054556.
- Chang, Raymond (2008). General chemistry : the essential concepts (5 utg.). Boston. McGraw-Hill. ISBN 9780071102261.
- Chang, Raymond; Goldsby, Kenneth A. (2014). General chemistry : the essential concepts (7 utg.). New York. McGraw-Hill. ISBN 9781259060427.
| Alkaner | |||||
| Metan CH4 |
Etan C2H6 |
Propan C3H8 |
Butan C4H10 |
Pentan C5H12 |
Heksan C6H14 |
| Heptan C7H16 |
Oktan C8H18 |
Nonan C9H20 |
Dekan C10H22 |
Undekan C11H24 |
Dodekan C12H26 |
| Tridekan C13H28 |
Tetradekan C14H30 |
Pentadekan C15H32 |
Heksadekan C16H34 |
Heptadekan C17H36 |
Oktadekan C18H38 |
| Nonadekan C19H40 |
Ikosan C20H42 |
Henikosann C21H44 |
Dokosan C22H46 |
Trikosan C23H48 |
Tetrakosan C24H50 |
| Pentakosan C25H52 |
Heksakosan C26H54 |
Heptakosan C27H56 |
Oktakosan C28H58 |
Nonakosan C29H60 |
Triakontan C30H62 |
| Hentriakontan C31H64 |
Dotriakontan C32H66 |
Tritriakontan C33H68 |
Tetratriakontan C34H70 |
Pentatriakontan C35H72 |
Heksatriakontan C36H74 |